Formula za izgaranje prirodnog plina. Prirodni gas. proces sagorijevanja
A. S. Isserlin
Proces izgaranja temelji se na kemijske reakcije kombinacija goriva i oksidansa. Da bi se odvijao proces izgaranja, mora se stvoriti plin posebni uvjeti. Najprije je potrebno u zapaljivi plin unijeti dovoljnu količinu oksidansa (najčešće zraka) i pomiješati ih. Drugo, mješavina plina i zraka mora imati granice koncentracije mora se osigurati zapaljivost i izvor paljenja. Treće, potrebno je stvoriti uvjete za razvoj procesa izgaranja, odnosno određenu razinu temperature.
Miješanje (ravnomjerno miješanje plina sa zrakom) jedna je od glavnih faza cjelokupnog procesa izgaranja. Svi daljnji stupnjevi kroz koje prolazi gorivo tijekom pretvorbe kemijske energije u toplinsku uvelike ovise o procesu nastanka smjese. Budući da se u zoni izgaranja uvijek uspostavlja visoka temperatura, vrijeme utrošeno na kemijske reakcije izgaranja uvijek je znatno manje od vremena potrebnog za proces stvaranja smjese.
Gori plinsko gorivo, kao i svaki drugi, u struji zraka, u skladu s modernim pogledima, moguće je na temelju kinetičkih i difuzijskih načela.
Ukupno vrijeme izgaranja plina, koje određuje brzinu izgaranja,
TP TS~1"~X1
Gdje je tc vrijeme miješanja potrebno za miješanje plina s oksidansom; tx je vrijeme kemijskih reakcija.
Ako ts<Стх, то практически тп«т*. В этом случае процесс протекает в кинетической области. Если же, наоборот, Тс^-Тх, то Тп»тс и, следовательно, процесс протекает в диффузионной области.
Kada se proces izgaranja odvija u kinetičkom području, brzina izgaranja ovisi o svojstvima dane zapaljive smjese, temperaturi u reakcijskom volumenu i koncentraciji reagensa u zoni izgaranja, tj. regulirana je kemijskim zakonima kinetika. Istodobno, brzina procesa u kinetičkom području ne ovisi o hidrodinamičkim čimbenicima, tj. o brzini protoka, geometrijskim dimenzijama reakcijske komore itd.
Naprotiv, u difuzijskom području brzina procesa određena je hidrodinamičkim čimbenicima i ne ovisi o kinetičkim. U ovom području svojstva zapaljive smjese i faktor temperature prestaju igrati odlučujuću ulogu. Relativno jednostavnim hidrodinamičkim sredstvima može se utjecati na intenzitet miješanja, što će dovesti do promjene karakteristika difuzijskog plamena.
S kinetičkim principom, u plameniku se prethodno stvara homogena smjesa plina i zraka, koja se dovodi u komoru za izgaranje. Stoga se izgaranje takve smjese odvija uz konstantnu vrijednost svih glavnih karakteristika (toplinski stres, višak zraka itd.). Čisto kinetičko izgaranje događa se samo ako je uvjet A^1,0. Kad<1 кинетическое горение протекает лишь на первой стадии, т. е. до тех пор, пока не израсходован весь кислород смеси. Остаток горючих компонентов, разбавленных продуктами сгорания, может быть сожжен только при условии подвода дополнительного окислителя (воздуха).
Difuzijski princip izgaranja podrazumijeva stvaranje takvih uvjeta za nastanak procesa pri kojima smjesa izgara odmah pri samom nastanku, tj. kada gorivo i oksidans dođu u dodir u odgovarajućim količinskim omjerima. Procesom difuzijskog izgaranja upravlja se promjenom intenziteta stvaranja smjese mijenjanjem konstrukcijskih i radnih parametara plamenika. Time je, ovisno o tehnološkim zahtjevima, moguće postići skraćenje zone miješanja ili njezino produljenje.
U praksi se često koristi spaljivanje plina na baklji, kombinirajući oba gore navedena principa. U tom slučaju, dio zraka se prethodno miješa s plinom u plameniku, a ostatak, neophodan za potpuno izgaranje, dovodi se izravno u zonu izgaranja. Promjenom ovog omjera moguće je utjecati na duljinu plinske baklje. U većini plamenika plin se dovodi pod određenim kutom u odnosu na protok zraka.
Puno je rada posvećeno proučavanju procesa stvaranja smjese. To nam omogućuje da formuliramo neke općenite obrasce.
Kod plinskih plamenika s izravnim protokom, što je miješanje bolje, to je veći presjek plamenika pokriven plinskim mlazovima, odnosno veći je domet plinskih mlaznica. U plamenicima s jako vrtložnim strujanjem ne treba težiti velikom rasponu plinskih mlaznica.
Povećanje uvijanja protoka zraka dovodi do preraspodjele plina i zraka po presjeku plamenika, povećanja intenziteta miješanja plina sa zrakom i povećanja središnje zone obrnutih struja u plameniku.
Priroda utjecaja zaokreta strujanja zraka na proces stvaranja smjese je različita ovisno o drugim determinirajućim parametrima. Dakle, kada se plin dovodi u periferne zone plamenika (bez obzira na njegovu vrstu), povećanje uvijanja protoka dovodi do značajnog poboljšanja u formiranju smjese. Naprotiv, kada se plin dovodi u središnju zonu plamenika, povećanje uvijanja u pravilu ne dovodi do poboljšanja procesa, „rješenje.
Cjelokupnost pojava koje nazivamo izgaranjem može se odvijati samo određenim slijedom, od jedne do druge faze. G. F. Knorre daje sljedeće sheme za ustaljeni proces izgaranja plina i tekućih goriva s fiksnim ložištem, koje on naziva in-line (sl. 1). Najjednostavnija shema toka događa se tijekom izgaranja plinovitog goriva koje se sastoji od jednostavnih molekula (na primjer, vodika) koje ne zahtijevaju preliminarnu složenu pirogenu razgradnju (Sl. 1, ALI). Kada se izgara plin ili tekuća ugljikovodična goriva, A 6
Tok procesa izgaranja je kompliciran: postoji još jedan srednji stadij - pirogena razgradnja. Za tekuća goriva ovoj fazi prethodi faza isparavanja (slika 1.6). Za provedbu sheme protoka potrebna je dovoljna razina temperature u komori za izgaranje, u koju se gorivo i oksidans dovode u kontinuiranim tokovima. Produkti izgaranja nakon završetka reakcija također se kontinuirano ispuštaju iz izvora izgaranja.
Poznato je da se plinsko-zračne smjese zapale samo kada je sadržaj plina u zraku unutar određenih (za svaki plin) granica. Pri niskom sadržaju plina količina topline koja se oslobađa tijekom izgaranja nije dovoljna da susjedne slojeve smjese dovede do temperature paljenja. Isto se opaža kada je sadržaj plina u mješavini plina i zraka previsok. Nedostatak kisika u zraku za izgaranje dovodi do pada razine temperature, zbog čega se susjedni slojevi smjese ne zagrijavaju do
Temperature paljenja. Ova dva slučaja odgovaraju donjoj i gornjoj granici zapaljivosti (Tablica 1). Dakle, osim miješanja plina sa zrakom u određenim omjerima, potrebno je stvoriti početne uvjete za paljenje smjese.
|
stol / Granice zapaljivosti i temperature paljenja raznih plinova u zraku
|
Oksidacija zapaljivih plinova moguća je pri niskim temperaturama, ali tada teče izuzetno sporo zbog neznatne brzine reakcija. S porastom temperature, brzina reakcije oksidacije raste sve dok ne dođe do samozapaljenja (umjesto spore oksidacije, počinje proces spontanog izgaranja). To znači da zapaljiva smjesa zagrijana na temperaturu paljenja ima takvu energiju koja ne samo da nadoknađuje gubitak topline u okolinu, već također osigurava zagrijavanje i pripremu smjese plina i zraka koja ulazi u zonu izgaranja za paljenje.
Temperatura paljenja plina ovisi o nizu čimbenika, uključujući sadržaj zapaljivog plina u mješavini plina i zraka, tlaku, načinu zagrijavanja smjese itd., te stoga nije točna vrijednost. U tablici. 1 prikazuje temperature paljenja nekih zapaljivih plinova u zraku.
U praksi postoje dva načina paljenja zapaljivih smjesa: samozapaljenje i paljenje.
Na Samozapaljivost cjelokupni volumen zapaljive smjese plina i zraka postupno se dovodi do temperature paljenja, nakon čega se smjesa zapali bez vanjskog toplinskog utjecaja.
U tehnologiji se naširoko koristi druga metoda, tzv paljenje. Kod ove metode nije potrebno cijelu smjesu plina i zraka zagrijavati do temperature paljenja, dovoljno je hladnu smjesu zapaliti u jednoj točki volumena nekim izvorom visoke temperature (iskra, vruće tijelo, pilot plamen, itd.). Kao rezultat toga, paljenje se spontano prenosi na cijeli volumen smjese širenjem plamena, što se ne događa trenutno, već određenom prostornom brzinom. Ova brzina se zove Brzina širenja plamena u smjesi plin-zrak i najvažnija je karakteristika koja određuje uvjete za tok i stabilizaciju izgaranja. Stabilnost plamenika, kao što će biti prikazano u nastavku, povezana je s brzinom širenja plamena.
Dakle, proces izgaranja plinovitog goriva sastoji se od miješanja plina sa zrakom, zagrijavanja dobivene smjese do temperature paljenja, njenog paljenja i nastanka reakcija izgaranja popraćenih oslobađanjem topline. Štoviše, miješanje plina sa zrakom i zagrijavanje smjese oduzima većinu vremena u procesu izgaranja, budući da se reakcije izgaranja odvijaju gotovo trenutno.
Ovisno o tehnološkom procesu (dobivanje pare i tople vode u kotlovskoj jedinici, zagrijavanje produkata u ložišnoj instalaciji i sl.), postaje potrebno utjecati na proces izgaranja mijenjanjem njegovih konačnih karakteristika. To se postiže različitim konstruktivnim tehnikama, koje su opisane u pogl. III.
Indikativno je usporediti temperaturna polja u volumenu baklje tijekom izgaranja plina s različitim koeficijentima viška zraka. Primjer takve usporedbe dan je na sl. 2 za plamenik s promjerom izlazne mlaznice od 35 mm kao funkciju
|
|
Gdje I- trenutna vrijednost temperature u plamenu, °C; tmax - maksimalna temperatura u plamenu (mjerena), °S; x- udaljenost od mjerne točke do početka baklje, m; Na- udaljenost od mjerne točke do osi baklje, m; Y- promjer mlaznice plamenika, m.
Na sl. Slika 2 prikazuje grafikone raspodjele temperature za tri koeficijenta viška zraka. Štoviše, koordinata X / g\u003d O odgovara izlaznom dijelu mlaznice plamenika, a koordinata g/g=0 - os plamena.
Kao što se vidi sa slike, raspodjela temperature u slobodnom plamenu je neravnomjerna. S malim viškom primarnog zraka, na primjer, a = 0,5, prisutnost unutarnje jezgre u plamenu uvelike iskrivljuje temperaturno polje i ono se izjednačava samo na udaljenosti od x / c / = 10, dok pri a = 0,75, izjednačenje se događa već kod X / g=2,5, a pri a=1,0 još ranije - pri X/d=1,0.
Najviše temperature u otvorenom plamenu opažene su u početnim dijelovima na udaljenosti od osi plamena Y / Y \u003d 0,5, a zatim u središte baklje. Štoviše, s povećanjem koeficijenta viška zraka, maksimalna temperatura se pomiče prema ušću plamenika. Tako je najviša temperatura pri a = 0,75 izmjerena na daljinu X / g\u003d 2,5, a na \u003d 1,0 - na udaljenosti X/d=1,0.
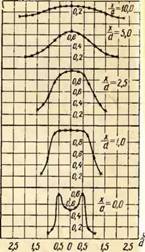 Kada se zajedno promatra raspodjela temperatura i koncentracija CO2 u oblaku, maksimumi se poklapaju
Kada se zajedno promatra raspodjela temperatura i koncentracija CO2 u oblaku, maksimumi se poklapaju
Temperatura i sadržaj CO2. Posljedično, maksimalna razina temperature u plameniku također odgovara maksimalnoj vrijednosti stupnja izgaranja zapaljivog materijala.
Gubitak dijela topline koja se oslobađa kao rezultat izgaranja plina je neizbježan. Međutim, oni se mogu svesti na minimum pravilnim upravljanjem procesom izgaranja. Razmotrimo koje. komponente zbrajaju te gubitke.
Pri izgaranju plinovitih goriva dolazi do sljedećih gubitaka topline: ispušnim plinovima, kemijskim nepotpunim izgaranjem iu okoliš. Na temelju određivanja pojedinačnih gubitaka topline inverznom ravnotežom, može se izračunati učinkovitost jedinice, ° / o:
Gdje<72 - потери тепла с уходящими газами, %; - потери тепла
Od kemijske nepotpunosti izgaranja, %; P5- gubitak topline u okoliš, %.
Gubitak topline s dimnim plinovima- fizička toplina produkata izgaranja koji napuštaju jedinicu - glavni su. Nemoguće ih je potpuno eliminirati, ali je potrebno težiti njihovom smanjenju. Toplinski gubici s dimnim plinovima ovise o temperaturi plinova i njihovoj količini. Što je niža temperatura ispušnih plinova, manje će se gubiti toplina, stoga treba težiti smanjenju temperature ispušnih plinova u razumnim granicama. Utjecaj temperature dimnih plinova na toplinske gubitke vidljiv je iz tablice. 2.
tablica 2
|
Gubitak topline s dimnim plinovima pri izgaranju prirodnog plina, %
|
Gubitak topline s ispušnim plinovima obično se izražava kao postotak ukupne raspoložive topline, tj. topline izgaranja goriva. Na primjer, ako je gubitak topline 700 kcal/m3 pri izgaranju prirodnog plina, tada
700-100 ___ „ 24°/
Količina plinova koji izlaze iz jedinice ovisi o omjeru viška zraka plamenika i usisnih čašica.
Propuštanje zraka u jedinici. Što je veći koeficijent viška zraka na izlazu iz plamenika i usisa zraka u uređaj, to je veći gubitak topline s ispušnim plinovima. Iz tablice. 2 vidljivo je da promjena koeficijenta ukupnog viška zraka u produktima izgaranja od aa = 1,2-5-1,6 povećava gubitak topline s dimnim plinovima od 10,5 do 13,2% (pri konstantnoj temperaturi dimnih plinova od 240°C) .
Dakle, da bi se smanjili gubici topline s ispušnim plinovima, potrebno je proces izgaranja provoditi s najmanjim dopuštenim koeficijentom viška zraka, osigurati najveću gustoću uređaja i postići smanjenje temperature ispušnih plinova.
Gubici topline od kemijskog nepotpunog izgaranja plina nastaju pri nedostatku zraka, lošem miješanju u plinskom plameniku i oštrom padu razine temperature u zoni izgaranja. Zbog toga se izgaranje plina odvija nepotpuno, a zapaljive komponente (na primjer, vodik, ugljični monoksid itd.) odlaze s produktima izgaranja. To dovodi do nedovoljnog iskorištenja kemijske energije goriva i smanjenja učinkovitosti jedinice. Čak i mali sadržaj zapaljivih komponenti u produktima izgaranja dovodi do značajnih gubitaka topline od kemijskog nepotpunog izgaranja. Pretpostavimo da su produkti izgaranja sadržavali 0,7% vodika i 0,5% ugljičnog monoksida. Prirodni plin je spaljivan u jedinici s koeficijentom viška zraka nizvodno od instalacije a» = 1,5. Toplinski gubici kemijskom nepotpunošću izgaranja iznosili su ~450 kcal/m3 odn.
A___ 450-100 poo/
Dakle, iz razmatranog primjera može se vidjeti da zapaljive komponente u produktima izgaranja trebaju biti potpuno odsutne ili biti minimalne.
Gubitak topline u okoliš nastaje zbog činjenice da zidovi jedinice imaju višu temperaturu od okolnog zraka. Veličina tih gubitaka ovisi uglavnom o razlici temperature između vanjskih zidova jedinice i okolnog zraka, veličini površine zida, toplinskoj vodljivosti zidanog materijala i njegovoj debljini. Gubici u okoliš izračunavaju se teoretski ili uzimaju iz normi toplinskog proračuna, ovisno o izvedbi i izvedbi jedinice.
Ako zbrojimo sve gubitke topline koji nastaju izgaranjem plina u uređaju, i oduzmemo ih od 100, dobivamo učinkovitost uređaja. Na primjer, korištenjem gornjih brojeva, uz pretpostavku<75 равным 3,60%, тогда к. п. д. агрегата
T]= 100-(8,24+5,28+3,60)=82,88%*
8.1. REAKCIJE IZGARANJA
Izgaranje je brza kemijska reakcija spajanja zapaljivih komponenti s kisikom, praćena intenzivnim oslobađanjem topline i naglim porastom temperature produkata izgaranja. Reakcije izgaranja opisuju se tzv. stehiometrijske jednadžbe koje kvalitativno i kvantitativno karakteriziraju tvari koje ulaze u reakciju i iz nje proizlaze (Stehiometrijski sastav zapaljive smjese (od grčkog stoicheion - baza, element i grčkog metreo - mjerim) - sastav smjese u kojoj je oksidansa točno onoliko koliko je potrebno za potpunu oksidaciju goriva. ). Opća jednadžba za reakciju izgaranja bilo kojeg ugljikovodika
C m H n + (m + n/4) O 2 = mCO 2 + (n/2) H 2 O + Q(8.1)
gdje je m, n broj atoma ugljika i vodika u molekuli; Q je toplinski učinak reakcije, odnosno toplina izgaranja.
Reakcije izgaranja nekih plinova dane su u tablici. 8.1. Ove su jednadžbe ravnoteže i iz njih je nemoguće prosuditi ni brzinu reakcija ni mehanizam kemijskih transformacija.
Tablica 8.1. Reakcije izgaranja i kalorična vrijednost suhih plinova (na 0°S i 101,3 kPa)
| Plin | Reakcija izgaranja | Toplina izgaranja | |||||
|---|---|---|---|---|---|---|---|
| Molar, kJ/kmol | Masa, kJ/kg | Volumetrijski, kJ / m 3 | |||||
| viši | inferioran | viši | inferioran | viši | inferioran | ||
| Vodik | H 2 + 0,5 O 2 \u003d H 2 0 | 286,06 | 242,90 | 141 900 | 120 080 | 12 750 | 10 790 |
| ugljični monoksid | CO + 0,5 O 2 \u003d CO 2 | 283,17 | 283,17 | 10 090 | 10 090 | 12 640 | 12 640 |
| Metan | CH 4 + 2O 2 \u003d CO 2 + 2H 2 O | 880,90 | 800,90 | 55 546 | 49 933 | 39 820 | 35 880 |
| Etan | C 2 H 6 + 0,5 O 2 \u003d 2CO 2 + 3 H 2 O | 1560,90 | 1425,70 | 52 019 | 47 415 | 70 310 | 64 360 |
| Propan | C3H8 + 5H2O \u003d 3CO2 + 4H2O | 2221,40 | 2041,40 | 50 385 | 46 302 | 101 210 | 93 180 |
| n-butan | 2880,40 | 2655,00 | 51 344 | 47 327 | 133 800 | 123 570 | |
| izobutan | C 4 H 10 + 6,5 O 2 \u003d 4CO 2 + 5 H 2 O | 2873,50 | 2648,30 | 51 222 | 47 208 | 132 960 | 122 780 |
| n-pentan | C 5 H 12 + 8 O 2 \u003d 5 CO 2 + 6 H 2 O | 3539,10 | 3274,40 | 49 052 | 45 383 | 169 270 | 156 630 |
| Etilen | C 2 H 4 + 3 O 2 \u003d 2 CO 2 + 2 H 2 O | 1412,00 | 1333,50 | 50 341 | 47 540 | 63 039 | 59 532 |
| propilen | C 3 H 6 + 4,5 O 2 \u003d 3 CO 2 + 3 H 2 O | 2059,50 | 1937,40 | 48 944 | 46 042 | 91 945 | 88 493 |
| Butilen | C 4 H 8 + 6O 2 \u003d 4CO 2 + 4H 2 O | 2720,00 | 2549,70 | 48 487 | 45 450 | 121 434 | 113 830 |
Toplinski učinak (ogrjevna vrijednost) Q - količina topline koja se oslobađa tijekom potpunog izgaranja 1 kmol, 1 kg ili 1 m 3 plina u normalnim fizikalnim uvjetima. Postoje viša Q in i niža Q n kalorična vrijednost: viša kalorična vrijednost uključuje toplinu kondenzacije vodene pare tijekom izgaranja (u stvarnosti, kada plin izgara, vodena para se ne kondenzira, već se uklanja zajedno s ostalim produktima izgaranja) . Tipično, tehnički proračuni se obično provode prema nižoj kalorijskoj vrijednosti, bez uzimanja u obzir topline kondenzacije vodene pare (≈2400 kJ / kg).
Učinkovitost izračunata prema nižoj ogrjevnoj vrijednosti je formalno veća, ali je toplina kondenzacije vodene pare prilično visoka, te je njegova uporaba više nego razumna. To potvrđuje aktivna uporaba kontaktnih izmjenjivača topline u tehnici grijanja, koji su vrlo raznoliki u dizajnu.
Za smjesu zapaljivih plinova viša (i niža) kalorična vrijednost plinova određena je omjerom
Q = r 1 Q 1 + r 2 Q 2 + ... + r n Q n (8.2)
gdje r 1 , r 2 , ..., r n - volumni (molarni, maseni) udjeli komponenata uključenih u smjesu; Q 1 , Q 2 , …, Q n - ogrjevna vrijednost komponenata.
Korištenje tablice. 8.1, viša i niža kalorična vrijednost, kJ / m 3, složenog plina može se odrediti prema sljedećim formulama:
Q u \u003d 127,5 H2 + 126,4 CO + 398 CH4 + 703 C2H6 + 1012 C8H8 + 1338 C4H10 + 1329 C4H10 +
+ 1693 C5H12 + 630 C2H4 + 919 C3H6 +1214 C4H8 (8,3)
Q n \u003d 107,9 H2 + 126,4 CO + 358,8 CH4 + 643 C2H6 + 931,8 C8H8 + 1235 C4H10 + 1227 C4H10 +
+ 1566 C5H12 + 595 C2H4 + 884 C8H6 + 1138 C4H8 (8,4)
gdje su H2, CO, CH4 itd. - sadržaj pojedinih komponenti u plinskom gorivu, vol. %.
Proces izgaranja je mnogo složeniji nego prema formuli (8.1), jer zajedno s grananjem lanaca dolazi do njihovog pucanja zbog stvaranja srednje stabilnih spojeva, koji se dalje transformiraju na visokim temperaturama. Uz dovoljnu koncentraciju kisika nastaju krajnji produkti: vodena para H 2 O i ugljikov dioksid CO 2. Uz nedostatak oksidirajućeg sredstva, kao i kada se reakcijska zona hladi, intermedijarni spojevi se mogu stabilizirati i ući u okoliš.
Intenzitet oslobađanja topline i porast temperature dovode do povećanja aktivnih čestica u sustavu koji reagira. Takav odnos lančane reakcije i temperature, karakterističan za gotovo sve procese izgaranja, doveo je do uvođenja pojma lančane toplinske eksplozije - same kemijske reakcije izgaranja su lančane prirode, a njihovo ubrzanje nastaje zbog oslobađanje topline i povećanje temperature u sustavu koji reagira.
Brzina kemijske reakcije u homogenoj smjesi proporcionalna je umnošku koncentracija reaktanata:
w = kS 1 S 2 (8,5)
gdje su C1 i C2 koncentracije reagirajućih komponenata, kmol/m3; k - konstanta brzine reakcije, ovisno o prirodi reaktanata i temperaturi.
Kada se plin sagorijeva, koncentracije reaktanata mogu se uvjetno smatrati nepromijenjenima, budući da se u zoni izgaranja događa kontinuirani priljev svježih komponenti jednoznačnog sastava.
Konstanta brzine reakcije (prema Arrheniusovoj jednadžbi):
K \u003d K 0 e -E / RT (8,6)
gdje je K 0 - predeksponencijalni faktor uzet za biometrijske homogene smjese, ≈1,0; E - energija aktivacije, kJ/kmol; R je univerzalna plinska konstanta, J/(kg K); T - apsolutna temperatura, K (°C); e je baza prirodnih logaritama.
Predeksponencijalni faktor K 0 može se tumačiti kao konstanta koja odražava potpunost sudara molekula, a E - kao minimalna energija za kidanje veza molekula i stvaranje aktivnih čestica koje osiguravaju učinkovitost sudara. Za uobičajene zapaljive smjese, to je unutar (80÷150) 10 3 kJ/kmol.
Jednadžba (8.6) pokazuje da se brzina kemijskih reakcija naglo povećava s porastom temperature: na primjer, povećanje temperature od 500 do 1000 K povlači za sobom povećanje brzine reakcije izgaranja za faktor od 2 10 4 ÷5 10 8 puta (ovisno o energiji aktivacije).
Na brzinu reakcija izgaranja utječe njihova lančana priroda. U početku, atomi i radikali nastali reakcijom ulaze u spojeve s početnim tvarima i međusobno, tvoreći konačne produkte i nove čestice koje ponavljaju isti lanac reakcija. Sve veće stvaranje takvih čestica dovodi do "ubrzanja" kemijskih reakcija - zapravo, eksplozije cijele smjese.
Visokotemperaturno izgaranje ugljikovodika je složeno i povezano je sa stvaranjem aktivnih čestica u obliku atoma i radikala, kao i međumolekularnih spojeva. Kao primjer navedene su reakcije izgaranja najjednostavnijeg ugljikovodika - metana:
- H + O 2 -> OH + O
CH 4 + OH -> CH 3 + H 2 O
CH 4 + O -› CH 2 + H 2 O - CH 3 + O 2 -› HCNO + OH
CH 2 + O 2 -> HCNO + O - HCHO + OH -> HCO + H 2 O
HCNO + O -› CO + H 2 O
HCO + O 2 -› CO + O + OH - CO + O -› CO 2
CO + OH -› CO 2 + H
Rezultat jednog ciklusa:
2CH 4 + 4O 2 -> 2CO 2 + 4H 2 O
8.2. PRORAČUNI IZGARANJA
Kisik za izgaranje dolazi iz zraka kao njegov sastavni dio. Za izračune se pretpostavlja da je volumetrijski sastav suhog zraka sljedeći:
kisik - 21,0%, dušik - 79,0%.
Prema navedenim podacima, 1 m 3 kisika sadrži 100/21 = 4,76 m 3 zraka, odnosno 79/21 = 3,76 m 3 dušika po 1 m 3 kisika. Uzimajući u obzir da 1 kmol plina u normalnim uvjetima zauzima volumen od 22,4 litre, reakcija izgaranja (vidi jednadžbu 8.1) bilo kojeg ugljikovodika u zraku može se napisati u općenitom obliku:
C m H n + (t + n/4) (O 2 + 3,76 N 2) = tCO 2 + (n/2) H 2 O + (t + n/4) 3,76 N 2
Zahtjevi za kisikom i zrakom tijekom izgaranja različitih plinova, izračunati iz zadanih reakcija izgaranja, prikazani su u tablici. 8.2.
Tablica 8.2. Teoretska potreba za suhim kisikom i zrakom, m 3, i volumen produkata izgaranja plina pri izgaranju 1 m 3 plina
| Plin | Teorijska potreba | produkti izgaranja | ||||
|---|---|---|---|---|---|---|
| kisik | zrak | ugljični dioksid | vodena para | dušik | Ukupno | |
| Vodik H 2 | 0,5 | 2,38 | – | 1,0 | 1,88 | 2,88 |
| Ugljični monoksid CO | 0,5 | 2,38 | 1,0 | – | 1,88 | 2,88 |
| Metan CH 4 | 2,0 | 9,52 | 1,0 | 2,0 | 7,52 | 10,52 |
| Etan C2H6 | 3,5 | 16,66 | 2,0 | 3,0 | 13,16 | 18,16 |
| Propan C3H8 | 5,0 | 23,80 | 3,0 | 4,0 | 18,80 | 25,80 |
| Butan C4H10 | 6,5 | 30,94 | 4,0 | 5,0 | 24,44 | 33,44 |
| Pentan C 5 H 12 | 8,0 | 38,08 | 5,0 | 6,0 | 30,08 | 41,08 |
| Etilen C2H4 | 3,0 | 14,28 | 2,0 | 2,0 | 11,28 | 15,28 |
| Propilen C3H6 | 4,5 | 21,42 | 3,0 | 3,0 | 16,92 | 22,92 |
| Butilen C4H8 | 6,0 | 28,56 | 4,0 | 4,0 | 22,56 | 30,56 |
| Pentilen C 5 H 10 | 7,5 | 35,70 | 5,0 | 5,0 | 28,20 | 38,20 |
| Acetilen C2H2 | 2,5 | 11,90 | 2,0 | 1,0 | 9,40 | 12,40 |
Za složeni plin, potrošnja suhog zraka V c, m 3 / m 3, izračunava se prema formuli koja uzima u obzir potrebu za kisikom pojedinačnih komponenti smjese:
V c \u003d 4,76 / 100 (0,5H2 + 0,5CO + 2CH4 + 3,5C2H6 + 5C3H8 + 6,5C4H10 + 3C2H4 + 4,5C3H6 +6C4H8 -O 2) (8,7)
Teorijski protok vlažnog zraka V vl, m 3 / m 3, više određen formulom (8.7) prema volumenu sadržane vodene pare:
V ow \u003d V s + 0,001244d u V s (8,8)
gdje d in - vlažnost zraka, g / m 3.
S nepoznatim kemijskim sastavom plinova, ali poznatom nižom ogrjevnom vrijednošću Q n, kJ / m 3, teoretski utrošak zraka V t, m 3 / m 3,
V t ≈ Q n / 3770 (8,9)
Stvarna potrošnja zraka V dv, m 3 / m 3, uvijek se uzima nešto veća:
V motor \u003d V t α (8.10)
gdje je α koeficijent viška zraka, koji odgovara zahtjevima GOST-a. Za potpuno izgaranje goriva vrijednost α mora biti veća od 1. Sastav i volumen produkata izgaranja, izračunat iz reakcija izgaranja nekih plinova u suhom zraku, dani su u tablici. 8.2.
8.3. TEMPERATURA GORENJA
U toplinskoj tehnici razlikuju se sljedeće temperature izgaranja plinova: izlazna toplina, kalorimetrijska, teorijska i stvarna (izračunata). Kapacitet grijanja t w - maksimalna temperatura proizvoda potpunog izgaranja plina u adijabatskim uvjetima s koeficijentom viška zraka α = 1,0 i pri temperaturi plina i zraka jednakoj 0 ° C:
t W = Q n /(∑Vc p)(8.11)
gdje je Q n - donja ogrjevna vrijednost plina, kJ / m 3; ∑ Vc p - zbroj umnožaka volumena ugljičnog dioksida, vodene pare i dušika nastalih izgaranjem 1 m 3 plina (m 3 / m 3), i njihovih prosječnih volumetrijskih toplinskih kapaciteta pri konstantnom tlaku unutar temperatura od 0 °C do t w (kJ /(m 3 o °C).
Zbog promjenjivosti toplinskog kapaciteta plinova, toplinski učinak se određuje metodom uzastopnih aproksimacija. Kao početni parametar uzima se njegova vrijednost za prirodni plin (≈2000°C), a pri α = 1,0 određuju se volumeni komponenata produkata izgaranja prema tablici. 8.3 nalazi se njihov prosječni toplinski kapacitet, a zatim se prema formuli (8.11) izračunava toplinska snaga plina. Ako se kao rezultat izračuna pokaže da je niža ili viša od prihvaćene, tada se postavlja druga temperatura i izračun se ponavlja.
Tablica 8.3. Prosječni volumetrijski toplinski kapacitet plinova, kJ / (m 3 ° S)
Temperatura, °S |
CO2 | N 2 | O2 | CO | CH 4 | H2 | H 2 O (vodena para) | zrak | |
|---|---|---|---|---|---|---|---|---|---|
| suha | mokro po 1 m 3 suhi plin |
||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | – | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | – | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | – | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | – | – | – | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | – | – | – | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | – | – | – | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | – | – | – | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | – | – | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | – | – | – | 1,9891 | – | – |
| 2200 | 2,4725 | 1,5011 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2300 | 2,4860 | 1,5070 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2400 | 2,4977 | 1,5166 | 1,6002 | – | – | – | 2,0389 | – | – |
| 2500 | 2,5091 | 1,5175 | 1,6045 | – | – | – | 2,0593 | – | – |
Toplinski učinak uobičajenih jednostavnih i složenih plinova pri njihovom izgaranju u suhom zraku dan je u tablici. 8.4. Kada se plin sagorijeva u atmosferskom zraku koji sadrži oko 1 mas. % vlage, toplinska snaga se smanjuje za 25-30°C.
Tablica 8.4. Toplinski učinak plinova u suhom zraku
| jednostavni plin | Toplinski učinak, °C | Složeni plin prosječan sastav |
Približni toplinski učinak, °C |
|---|---|---|---|
| Vodik | 2235 | polja prirodnog plina |
2040 |
| ugljični monoksid | 2370 | prirodna naftna polja |
2080 |
| Metan | 2043 | Koks |
2120 |
| Etan | 2097 | Visokotemperaturna destilacija škriljevca |
1980 |
| Propan | 2110 | Puhanje pare i kisika pod pritiskom |
2050 |
| Butan | 2118 | Generator od masnog ugljena |
1750 |
| Pentan | 2119 | Udar pare i zraka generatora iz siromašnih goriva |
1670 |
| Etilen | 2284 | Ukapljeni (50% C3H4 + 50% C4H10) |
2115 |
| Acetilen | 2620 | 2210 |
Kalorimetrijska temperatura izgaranja t do - temperatura određena bez uzimanja u obzir disocijacije vodene pare i ugljičnog dioksida, ali uzimajući u obzir stvarnu početnu temperaturu plina i zraka. Razlikuje se od toplinskog učina t po tome što se temperatura plina i zraka, kao i koeficijent viška zraka α, uzimaju prema njihovim stvarnim vrijednostima. Možete odrediti t k formulom:
t k \u003d (Q n + q fizički) / (ΣVc p) (8.12)
gdje je q fizički - sadržaj topline (fizička toplina) plina i zraka, mjeren od 0 ° C, kJ / m 3.
Prirodni i ukapljeni ugljikovodični plinovi obično se ne zagrijavaju prije izgaranja, a njihov je volumen malen u usporedbi s volumenom zraka za izgaranje. Stoga se pri određivanju kalorimetrijske temperature toplinski sadržaj plinova može zanemariti. Kada se izgaraju plinovi s niskom ogrjevnom vrijednošću (generator, visoka peć itd.), njihov toplinski sadržaj (osobito onih zagrijanih prije izgaranja) ima vrlo značajan utjecaj na kalorimetrijsku temperaturu.
Ovisnost kalorimetrijske temperature prirodnog plina srednjeg sastava u zraku s temperaturom 0°C i vlagom 1% o koeficijentu viška zraka α dana je u tablici. 8.5, za ukapljeni plin ugljikovodika kada se spaljuje na suhom zraku - u tablici. 8.7. Tablični podaci. 8.5–8.7, može se voditi s dovoljnom točnošću u određivanju kalorimetrijske temperature izgaranja drugih prirodnih plinova, relativno sličnog sastava, i ugljikovodičnih plinova gotovo bilo kojeg sastava. Ako je potrebno postići visoku temperaturu pri izgaranju plinova s niskim koeficijentima viška zraka, kao i povećati učinkovitost peći, u praksi se zagrijava zrak, što dovodi do povećanja kalorimetrijske temperature (vidi tablicu 8.6).
Tablica 8.5. Kalorimetrijske i teorijske temperature izgaranja prirodnog plina u zraku s t = 0°C i 1% vlažnosti ovisno o koeficijentu viška zraka α
| Teoretska temperatura izgaranja t t, ° S | Koeficijent viška zraka α | Kalorimetrijska temperatura izgaranja t k, °S | ||
|---|---|---|---|---|
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | – | 1,82 | 1260 |
| 1,25 | 1700 | – | 1,87 | 1230 |
| 1,28 | 1670 | – | 1,94 | 1200 |
| 1,30 | 1650 | – | 2,00 | 1170 |
Tablica 8.6. Kalorimetrijska temperatura izgaranja prirodnog plina t k, ° S, ovisno o koeficijentu viška suhog zraka i njegovoj temperaturi (zaokružene vrijednosti)
| Koeficijent viška zraka α | Temperatura suhog zraka, °C | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Tablica 8.7. Kalorimetrijska temperatura izgaranja t do tehničkog propana u suhom zraku s t = 0°C ovisno o koeficijentu viška zraka α
| Koeficijent viška zraka α | Kalorimetrijska temperatura izgaranja t k, °S | Koeficijent viška zraka α | Kalorimetrijska temperatura izgaranja t k, °S |
|---|---|---|---|
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
Teoretska temperatura izgaranja t T - maksimalna temperatura, određena slično kalorimetrijskom t k, ali prilagođena za endotermne (zahtijevaju toplinu) reakcije disocijacije ugljičnog dioksida i vodene pare, koje se odvijaju s povećanjem volumena:
CO 2 ‹–› CO + 0,5O 2 - 283 mJ / mol (8.13)
H 2 O ‹–› H 2 + 0,5 O 2 - 242 mJ / mol (8.14)
Na visokim temperaturama disocijacija može dovesti do stvaranja atomskog vodika, kisika i OH hidroksilnih skupina. Osim toga, kada se plin sagorijeva, uvijek se stvara nešto dušikovog oksida. Sve ove reakcije su endotermne i dovode do smanjenja temperature izgaranja.
Teorijska temperatura izgaranja može se odrediti sljedećom formulom:
t T \u003d (Q n + q fizički - q dis) / (ΣVc p) (8.15)
gdje je q dis - ukupni trošak topline za disocijaciju CO 2 i H 2 O u produktima izgaranja, kJ / m 3; ΣVc p je zbroj umnoška volumena i prosječnog toplinskog kapaciteta produkata izgaranja, uzimajući u obzir disocijaciju po 1 m 3 plina.
Tablica 8.8. Stupanj disocijacije vodene pare H 2 O i ugljičnog dioksida CO 2 ovisno o parcijalnom tlaku
| Temperatura, °S | Parcijalni tlak, MPa | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,004 | 0,006 | 0,008 | 0,010 | 0,012 | 0,014 | 0,016 | 0,018 | 0,020 | 0,025 | 0,030 | 0,040 | |
| Vodena para H2O | ||||||||||||
| 1600 | 0,85 | 0,75 | 0,65 | 0,60 | 0,58 | 0,56 | 0,54 | 0,52 | 0,50 | 0,48 | 0,46 | 0,42 |
| 1700 | 1,45 | 1,27 | 1,16 | 1,08 | 1,02 | 0,95 | 0,90 | 0,85 | 0,8 | 0,76 | 0,73 | 0,67 |
| 1800 | 2,40 | 2,10 | 1,90 | 1,80 | 1,70 | 1,60 | 1,53 | 1,46 | 1,40 | 1,30 | 1,25 | 1,15 |
| 1900 | 4,05 | 3,60 | 3,25 | 3,0 | 2,85 | 2,70 | 2,65 | 2,50 | 2,40 | 2,20 | 2,10 | 1,9 |
| 2000 | 5,75 | 5,05 | 4,60 | 4,30 | 4,0 | 3,80 | 3,55 | 3,50 | 3,40 | 3,15 | 2,95 | 2,65 |
| 2100 | 8,55 | 7,50 | 6,80 | 6,35 | 6,0 | 5,70 | 5,45 | 5,25 | 5,10 | 4,80 | 4,55 | 4,10 |
| 2200 | 12,3 | 10,8 | 9,90 | 9,90 | 8,80 | 8,35 | 7,95 | 7,65 | 7,40 | 6,90 | 6,50 | 5,90 |
| 2300 | 16,0 | 15,0 | 13,7 | 12,9 | 12,2 | 11,6 | 11,1 | 10,7 | 10,4 | 9,6 | 9,1 | 8,4 |
| 2400 | 22,5 | 20,0 | 18,4 | 17,2 | 16,3 | 15,6 | 15,0 | 14,4 | 13,9 | 13,0 | 12,2 | 11,2 |
| 2500 | 28,5 | 25,6 | 23,5 | 22,1 | 20,9 | 20,0 | 19,3 | 18,6 | 18,0 | 16,8 | 15,9 | 14,6 |
| 3000 | 70,6 | 66,7 | 63,8 | 61,6 | 59,6 | 58,0 | 56,5 | 55,4 | 54,3 | 51,9 | 50,0 | 47,0 |
| Ugljični dioksid CO2 | ||||||||||||
| 1500 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,4 | 0,4 | 0,4 | 0,4 | 0,4 | – |
| 1600 | 2,0 | 1,8 | 1,6 | 1,5 | 1,45 | 1,4 | 1,35 | 1,3 | 1,25 | 1,2 | 1,1 | |
| 1700 | 3,8 | 3,3 | 3,0 | 2,8 | 2,6 | 2,5 | 2,4 | 2,3 | 2,2 | 2,0 | 1,9 | |
| 1800 | 6,3 | 5,5 | 5,0 | 4,6 | 4,4 | 4,2 | 4,0 | 3,8 | 3,7 | 3,5 | 3,3 | |
| 1900 | 10,1 | 8,9 | 8,1 | 7,6 | 7,2 | 6,8 | 6,5 | 6,3 | 6,1 | 5,6 | 5,3 | |
| 2000 | 16,5 | 14,6 | 13,4 | 12,5 | 11,8 | 11,2 | 10,8 | 10,4 | 10,0 | 9,4 | 8,8 | |
| 2100 | 23,9 | 21,3 | 19,6 | 18,3 | 17,3 | 16,5 | 15,9 | 15,3 | 14,9 | 13,9 | 13,1 | |
| 2200 | 35,1 | 31,5 | 29,2 | 27,5 | 26,1 | 25,0 | 24,1 | 23,3 | 22,6 | 21,2 | 20,1 | |
| 2300 | 44,7 | 40,7 | 37,9 | 35,9 | 34,3 | 32,9 | 31,8 | 30,9 | 30,0 | 28,2 | 26,9 | |
| 2400 | 56,0 | 51,8 | 48,8 | 46,5 | 44,6 | 43,1 | 41,8 | 40,6 | 39,6 | 37,5 | 35,8 | |
| 2500 | 66,3 | 62,2 | 59,3 | 56,9 | 55,0 | 53,4 | 52,0 | 50,7 | 49,7 | 47,3 | 45,4 | |
| 3000 | 94,9 | 93,9 | 93,1 | 92,3 | 91,7 | 90,6 | 90,1 | 89,6 | 88,5 | 87,6 | 86,8 | |
Kao što se vidi iz tablice. 8.8, na temperaturama do 1600 ° C, stupanj disocijacije se ne može uzeti u obzir, a teorijska temperatura izgaranja može se uzeti jednaka kalorimetrijskoj. Pri višim temperaturama stupanj disocijacije može znatno smanjiti temperaturu u radnom prostoru. U praksi za tim nema posebne potrebe, teoretsku temperaturu izgaranja potrebno je odrediti samo za visokotemperaturne peći koje rade na prethodno zagrijani zrak (npr. martenske peći). Za instalacije kotlova to nije potrebno.
Tablica 8.9. Maksimum
nastale temperature
u slobodnom plamenu, ° S
Stvarna (izračunata) temperatura produkata izgaranja t d- temperatura, koja se u stvarnim uvjetima postiže na najtoplijoj točki baklje. Ona je manja od teorijske i ovisi o gubitku topline u okolinu, stupnju prijelaza topline iz zone izgaranja zračenjem, duljini procesa izgaranja u vremenu itd. Stvarne prosječne temperature u ložištima i kotlovima su određena toplinskom bilancom ili približno teoretskom ili kalorimetrijskom temperaturom izgaranja, ovisno o temperaturi u ložištima uz uvođenje u njih eksperimentalno utvrđenih korekcijskih faktora:
t d = t t η(8.16)
gdje je η- tzv. pirometrijski koeficijent u granicama:
- za dobro izrađene toplinske i grijaće peći s toplinskom izolacijom - 0,75–0,85;
- za zatvorene peći bez toplinske izolacije - 0,70–0,75;
- za oklopljene peći kotlova - 0,60–0,75.
U praksi je potrebno poznavati ne samo gornje adijabatske temperature izgaranja, već i maksimalne temperature koje se javljaju u plamenu. Njihove približne vrijednosti obično se utvrđuju eksperimentalno spektrografskim metodama. Maksimalne temperature koje se javljaju u slobodnom plamenu na udaljenosti od 5-10 mm od vrha stožaste fronte izgaranja dane su u tablici. 8.9. Analiza navedenih podataka pokazuje da su maksimalne temperature u plamenu manje od toplinskog učinka (zbog troška topline za disocijaciju H 2 O i CO 2 i odvođenje topline iz zone plamena).
8.4. TEMPERATURA SAMOPALJENJA
Za pokretanje reakcija izgaranja potrebni su uvjeti za paljenje smjese goriva s oksidansom. Paljenje može biti spontano i prisilno (paljenje).
Temperatura samozapaljenja- minimalna temperatura pri kojoj počinje proces spontanog (tj. bez vanjskog dovoda topline) izgaranja u zagrijanoj smjesi plina i zraka, zbog oslobađanja topline izgaranjem čestica plina.
Temperatura samozapaljenja nije fiksna za određeni plin i ovisi o mnogim parametrima: njegovom sadržaju u smjesi plina i zraka, stupnju homogenosti smjese, obliku i veličini posude u kojoj se smjesa zagrijava, brzini i način njegova zagrijavanja, katalitički učinak stijenki posude, tlak pod kojim se smjesa. Točno razmatranje ovih čimbenika je vrlo teško, stoga se u praksi, na primjer, pri procjeni eksplozivnosti koriste eksperimentalni podaci (vidi tablicu 8.10).
Tablica 8.10. Najniže izmjerene temperature samozapaljenja nekih plinova i para pomiješanih sa zrakom pri atmosferskom tlaku
Temperature samozapaljenja zapaljivih plinova u kisiku su nešto niže nego u zraku. Uvođenjem balastnih nečistoća (dušik i ugljični dioksid) u sastav plina dolazi do povećanja temperature samozapaljenja. Prisutnost komponenti s niskom temperaturom samozapaljenja u složenim plinovima dovodi do smanjenja temperature samozapaljenja smjese.
Prisilno paljenje (paljenje) provodi se paljenjem smjese na jednoj ili više točaka izvorom visoke temperature - otvorenim plamenom ili električnom iskrom na mjestu gdje plin izlazi iz kanala izgaranja plamenika u prostor ložišta. . Paljenje se razlikuje od samozapaljenja po tome što se zapaljiva smjesa dovodi do pojave plamena ne u cijelom volumenu, već samo u malom dijelu. Odvođenje topline iz grijane zone zahtijeva da brzina otpuštanja topline izvora paljenja premašuje ovo odvođenje topline. Nakon paljenja, izvor paljenja se uklanja i dolazi do izgaranja širenjem fronte plamena.
8.5. GRANICE ZAPALJIVOSTI I EKSPLOZIRNOSTI
Smjese plina i zraka mogu se zapaliti (eksplodirati) samo kada je sadržaj plina u smjesi unutar određenih (za svaki plin) granica. S tim u vezi postoje donja i gornja koncentracijska granica zapaljivosti. Donja granica odgovara minimalnoj, a gornja - maksimalnoj količini plina u smjesi, pri kojoj se zapale (tijekom paljenja) i spontano (bez dotoka topline izvana) širenje plamena (samozapaljenje). Iste granice odgovaraju uvjetima eksplozivnosti smjesa plina i zraka.
Ako je sadržaj plina u smjesi plin-zrak manji od donje granice zapaljivosti, takva smjesa ne može gorjeti i eksplodirati, jer toplina koja se oslobađa u blizini izvora paljenja nije dovoljna da zagrije smjesu do temperature paljenja. Ako je sadržaj plina u smjesi između donje i gornje granice zapaljivosti, zapaljena smjesa se zapali i gori i u blizini izvora paljenja i kada se on ukloni. Ova smjesa je eksplozivna. Što je širi raspon granica zapaljivosti (koje se nazivaju i granice eksplozivnosti) i što je niža donja granica, to je plin eksplozivniji. I na kraju, ako sadržaj plina u smjesi prelazi gornju granicu zapaljivosti, tada je količina zraka u smjesi nedovoljna za potpuno izgaranje plina.
Postojanje granica zapaljivosti uzrokovano je gubitkom topline tijekom izgaranja. Kada se zapaljiva smjesa razrijedi zrakom, kisikom ili plinom, gubici topline se povećavaju, brzina širenja plamena se smanjuje, a izgaranje prestaje nakon uklanjanja izvora paljenja.
Tablica 8.11. Granice zapaljivosti plinova pomiješanih sa zrakom (pri t = 20°C i p = 101,3 kPa)
| Plin | Sadržaj plina u smjesi plin-zrak, vol. % | Maksimum |
Koeficijent zraka α na granicama zapaljivosti | ||||
|---|---|---|---|---|---|---|---|
| U granicama zapaljivosti | Uz stehiometrijski sastav smjese | Sa sastavom smjese koja daje maksimalni tlak eksplozije | |||||
| niži | vrh | niži | vrh | ||||
| Vodik | 4,0 | 75,0 | 29,5 | 32,3 | 0,739 | 9,8 | 0,15 |
| ugljični monoksid | 12,5 | 74,0 | 29,5 | – | – | 2,9 | 0,15 |
| Metan | 5,0 | 15,0 | 9,5 | 9,8 | 0,717 | 1,8 | 0,65 |
| Etan | 3,2 | 12,5 | 5,68 | 6,28 | 0,725 | 1,9 | 0,42 |
| Propan | 2,3 | 9,5 | 4,04 | 4,60 | 0,858 | 1,7 | 0,40 |
| n-butan | 1,7 | 8,5 | 3,14 | 3,6 | 0,858 | 1,7 | 0,35 |
| izobutan | 1,8 | 8,4 | 3,14 | – | – | ~1,8 | 0,35 |
| n-pentan | 1,4 | 7,8 | 2,56 | 3,0 | 0,865 | 1,8 | 0,31 |
| Etilen | 3,0 | 16,0 | 6,5 | 8,0 | 0,886 | 2,2 | 0,17 |
| propilen | 2,4 | 10,0 | 4,5 | ~5,1 | ~0,89 | 1,9 | 0,37 |
| Butilen | 1,7 | 9,0 | 3,4 | ~4,0 | ~0,88 | 1,7 | 0,35 |
| Acetilen | 2,5 | 80,0 | 7,75 | 14,5 | 1,03 | 3,3 | 0,019 |
Tablica 8.12. Granice zapaljivosti plinova pomiješanih s kisikom (pri t = 20°C i p = 101,3 kPa)
Granice zapaljivosti uobičajenih plinova u smjesama sa zrakom i kisikom dane su u tablici. 8.11–8.12. S porastom temperature smjese, granice zapaljivosti se šire, a na temperaturi višoj od temperature samozapaljenja, smjese plina sa zrakom ili kisikom gore u bilo kojem omjeru volumena.
Granice zapaljivosti ovise ne samo o vrstama zapaljivih plinova, već i o uvjetima pokusa (kapacitet posude, toplinska snaga izvora paljenja, temperatura smjese, širenje plamena gore, dolje, vodoravno itd.). To objašnjava donekle različite vrijednosti ovih granica u različitim literarnim izvorima. U tablici. Slike 8.11–8.12 prikazuju relativno pouzdane podatke dobivene pri sobnoj temperaturi i atmosferskom tlaku tijekom širenja plamena odozdo prema gore u cijevi promjera 50 mm ili više. Kada se plamen širi odozgo prema dolje ili vodoravno, donje granice se lagano povećavaju, a gornje smanjuju. Granice zapaljivosti složenih zapaljivih plinova koji ne sadrže balastne nečistoće određene su pravilom aditivnosti:
L g \u003d (r 1 + r 2 + ... + r n) / (r 1 / l 1 + r 2 / l 2 + ... + r n / l n) (8.17)
gdje je L g donja ili gornja granica zapaljivosti složenog plina u smjesi plin-zrak ili plin-kisik, vol. %; r 1 , r 2 , …, r n - sadržaj pojedinih komponenti u složenom plinu, vol. %; r 1 + r 2 + ... + r n \u003d 100%; l 1, l 2, ..., l n - donje ili gornje granice zapaljivosti pojedinih komponenti u smjesi plin-zrak ili plin-kisik prema tablici. 8,11 ili 8,12, sv. %.
U prisutnosti balastnih nečistoća u plinu, granice zapaljivosti mogu se odrediti formulom:
L b \u003d L g / (8,18)
gdje L b - gornja i donja granica zapaljivosti smjese s balastnim nečistoćama, vol. %; L g - gornja i donja granica zapaljivosti zapaljive smjese, vol. %; B - količina balastnih nečistoća, udjeli jedinice.
Pri proračunu je često potrebno znati koeficijent viška zraka α za različite granice zapaljivosti (vidi tablicu 8.11), kao i tlak koji nastaje tijekom eksplozije smjese plina i zraka. Koeficijent viška zraka koji odgovara gornjoj ili donjoj granici zapaljivosti može se odrediti formulom
α = (100/L – 1) (1/V T)(8,19)
Tlak koji proizlazi iz eksplozije smjese plina i zraka može se odrediti s dovoljnom aproksimacijom prema sljedećim formulama:
za stehiometrijski omjer jednostavnog plina i zraka:
P vz \u003d P n (1 + βt k) (m / n) (8,20)
za bilo koji omjer složenog plina i zraka:
R vz \u003d R n (1 + βt k) V vlps / (1 + αV m) (8.21)
gdje je P vz - tlak koji proizlazi iz eksplozije, MPa; p n - početni tlak (prije eksplozije), MPa; β - koeficijent volumetrijske ekspanzije plinova, brojčano jednak koeficijentu tlaka (1/273); t K - kalorimetrijska temperatura izgaranja, °S; m je broj molova nakon eksplozije, određen reakcijom izgaranja plina u zraku; n je broj molova prije eksplozije uključenih u reakciju izgaranja; V vlps - volumen mokrih proizvoda izgaranja po 1 m 3 plina, m 3; V t - teoretska potrošnja zraka, m 3 / m 3.
Tablica 8.13. Tlak koji proizlazi iz eksplozije smjese propan-zrak, ovisno o koeficijentu pražnjenja k sb i vrsti zaštitnog uređaja
| Vrsta zaštitnog uređaja | Koeficijent protoka k sb, m 2 / m 3 | ||
|---|---|---|---|
| 0,063 | 0,033 | 0,019 | |
| Jednostruko fiksno ostakljenje s vanjskim pričvršćivanjem stakla debljine 3 mm | 0,005 | 0,009 | 0,019 |
| Dvostruko fiksno staklo s vanjskim pričvršćivanjem stakla debljine 3 mm | 0,007 | 0,015 | 0,029 |
| Okretni jednostruki prozorski okvir s velikom šarkom i opružnom bravom za opterećenje od 5 MPa / m 2 | 0,002 | – | – |
| Okretni jednostruki prozorski okvir s gornjom šarkom i opružnom bravom za opterećenje od 5 MPa / m 2 | 0,003 | – | – |
| Ploče koje slobodno leže na podu s masom, kg / m 2: | |||
| 0,023 | |||
| 0,005 | |||
| 0,018 | |||
Tlakovi eksplozije navedeni u tablici. 8.13 ili određeno formulama može se dogoditi samo ako je plin potpuno izgorio unutar spremnika i ako su njegovi zidovi dizajnirani za te tlakove. Inače su ograničeni čvrstoćom stijenki ili njihovih dijelova koji se najlakše uništavaju - impulsi tlaka šire se kroz nezapaljeni volumen smjese brzinom zvuka i stižu do ograde mnogo brže od fronte plamena.
Ova značajka - razlika u brzinama širenja plamena i impulsima tlaka (udarni val) - naširoko se koristi u praksi za zaštitu plinskih uređaja i prostorija od uništenja tijekom eksplozije. Da biste to učinili, u otvore zidova i stropova postavljaju se lako otvarajuće ili sklopive krmenice, okviri, ploče, ventili itd. Tlak koji proizlazi iz eksplozije ovisi o značajkama dizajna zaštitnih uređaja i koeficijentu pražnjenja k sb, što je omjer površine zaštitnih uređaja i volumena prostorije.
8.6. IZGARANJE U MIRNOJ OKRUŽINI
Pomicanje zone plamena - fronta plamena, - područje koje odvaja neizreagiranu zapaljivu smjesu od produkata izgaranja, uzrokovano je činjenicom da se hladna zapaljiva smjesa ispred sebe zagrijava do temperature paljenja zbog toplinske vodljivosti i difuzije. toplih produkata izgaranja u hladnu smjesu. Linearna brzina kojom se fronta plamena kreće kroz homogenu zapaljivu smjesu naziva se jednolika brzina širenja plamena ovisno i o vrsti plina i njegovom sadržaju u plinsko-zračnoj smjesi. Minimalna brzina za sve vrste zapaljivih plinova odgovara donjoj i gornjoj granici paljenja, a maksimalna - omjeru plinova i zraka.
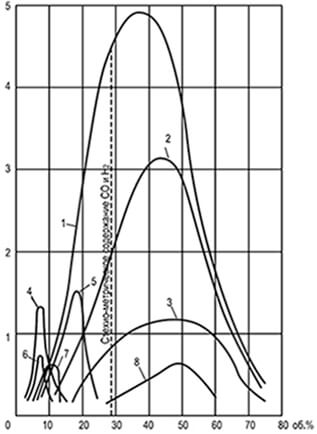
Riža. 8.1. Krivulje jednolikih brzina
širenje plamena u n, definirano
u cijevi promjera 25,4 mm
1-vodik; 2-vodeni plin; 3-ugljični monoksid;
4-etilen; 5-koksni plin; 6-etan; 7-metan;
8-generator parno-zrak udarni plin
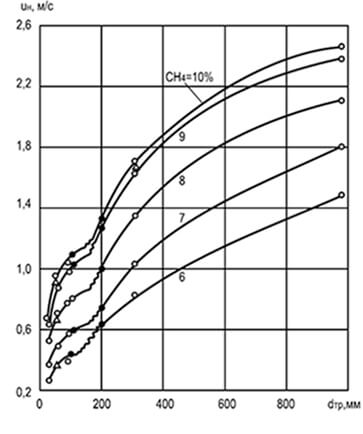
Riža. 8.2. Utjecaj promjera d tr i koncentracije
metan pomiješan sa zrakom promijeniti
jednolika brzina širenja plamena u n
Pokusima je utvrđeno da brzina širenja plamena ovisi o promjeru cilindrične cijevi kroz koju se širi: što je veći promjer, to je veća brzina širenja. Povećanje promjera cijevi smanjuje utjecaj stijenki na proces izgaranja i pokretnu frontu plamena te pridonosi povećanju konvekcije (slika 8.2). Analiza podataka grafikona pokazuje da je s vrlo malim veličinama cijevi širenje plamena općenito nemoguće (zbog snažnog relativnog odvođenja topline). Veličine cijevi, kanala i proreza kod kojih se plamen ne širi nazivaju se kritičnim.
Oni su različiti za različite plinove:
- hladna mješavina metana sa zrakom - 3 mm;
- smjesa vodik-zrak - 0,9 mm;
- zagrijana smjesa metana sa zrakom - 1,2 mm.
Gašenje u kanalima malog presjeka koristi se u praksi za izradu hvatača požara: rešetke za hvatanje plamena, keramičke porozne pločice, pločice od prešanih metalnih kuglica, posude punjene sitnozrnatim materijalima i dr.); požarni kanali u dizajnu plamenika koji rade na mješavinama plina i zraka.
Za usporednu karakteristiku zapaljivih svojstava plinova (bez obzira na veličinu cijevi), koncept "normalna brzina širenja plamena"- ovo je brzina, koja se odnosi na hladnu (još nezapaljenu) smjesu, kojom se plamen kreće po normali na svoju površinu. Pretpostavlja se da je fronta plamena ravna i jednaka promjeru cijevi:
u n \u003d w p πr 2 / S (8,22)
gdje je u n normalna brzina širenja plamena, m/s; w p - izmjerena jednolika brzina širenja plamena, m/s; r - radijus cijevi, m; S je površina fronte plamena, m 2.
Tablica 8.14. Brzine širenja plamena u raznim smjesama plina i zraka (pri t=20°C i p=103,3 kPa), m/s
| Plin | Smjesa s maksimalnim normalnim brzina širenja plamena |
Stehiometrijska smjesa | ||||
|---|---|---|---|---|---|---|
| Sadržaj u smjesi, vol. % | Maksimum normalan ubrzati širenje |
Sadržaj u smjesi, vol. % | Normalan ubrzati širenje plamen |
|||
| plin | zrak | plin | zrak | |||
| Vodik | 42,0 | 58,0 | 2,67 | 29,5 | 70,5 | 1,6 |
| ugljični monoksid | 43,0 | 57,0 | 0,42 | 29,5 | 70,5 | 0,30 |
| Metan | 10,5 | 89,0 | 0,37 | 9,5 | 90,5 | 0,28 |
| Etan | 6,3 | 93,7 | 0,40 | 5,7 | 94,3 | 0,32 |
| Propan | 4,3 | 95,7 | 0,38 | 4,04 | 95,96 | 0,31 |
| n-butan | 3,3 | 96,7 | 0,37 | 3,14 | 96,86 | 0,30 |
| Etilen | 7,0 | 93,0 | 0,63 | 6,5 | 93,5 | 0,5 |
| propilen | 4,8 | 95,2 | 0,44 | 4,5 | 95,5 | 0,37 |
| Butilen | 3,7 | 96,3 | 0,43 | 3,4 | 96,6 | 0,38 |
| Acetilen | 10,0 | 90,0 | 1,35 | 7,75 | 92,25 | 1,0 |
Kao što je vidljivo iz podataka u tablici. 8.14, najveća brzina širenja plamena odgovara smjesama plina i zraka s nedostatkom oksidatora (nije stehiometrijski). S viškom goriva povećava se učinkovitost sudara čestica koje reagiraju i povećava se brzina kemijskih reakcija.
Brzine širenja plamena za smjese plina i kisika su za red veličine veće nego za smjese plina i zraka. Tako je najveća normalna brzina širenja plamena za smjesu metana i kisika 3,3 m/s, a za smjesu propana i butana s kisikom 3,5–3,6 m/s.
Najveća normalna brzina širenja plamena u smjesi složenog plina sa zrakom, m/s, određena je formulom:
u n max \u003d (r 1 u 1 + r 2 u 2 + ... + r n u n) / (r 1 + r 2 + ... + r n) (8.23)
gdje je r 1 , r 2 ,…r n sadržaj pojedinačnih komponenti u složenom plinu, vol. %; u 1 , u 2 ,...u n su maksimalne normalne brzine širenja plamena složenih komponenti plina pomiješanih sa zrakom, m/s.
Dani omjeri prikladni su za plinove koji imaju bliske normalne brzine širenja plamena, na primjer za prirodne i ukapljene ugljikovodične plinove. Za plinske smjese s dramatično različitim brzinama širenja plamena (npr. mješavine prirodnih i umjetnih plinova, smjese s visokim udjelom vodika) daju samo približne vrijednosti.
Ako smjesa sadrži balastne nečistoće (dušik i ugljični dioksid), tada za približni izračun brzine širenja plamena treba koristiti sljedeću formulu:
u b \u003d u n max (1 - 0,01N 2 - 0,012CO 2) (8,24)
Značajno povećava brzinu širenja plamena zagrijavanjem mješavine plina i zraka:
u‘ n \u003d u n (T‘ / T) (8,25)
gdje su u‘ n brzine širenja plamena u zagrijanoj smjesi s apsolutnom temperaturom T‘, K; i n - isto, u hladnoj smjesi s temperaturom T, K.
Prethodno zagrijavanje smjese mijenja njezinu gustoću obrnuto proporcionalno apsolutnoj temperaturi, pa se stoga i brzine širenja plamena povećavaju proporcionalno toj temperaturi. Ovu činjenicu treba uzeti u obzir u proračunima, posebno u onim slučajevima kada su kanali za paljenje plamenika smješteni u grijanom zidu ili kada su pod utjecajem zračenja peći, vrućih plinova itd.
Ujednačenost širenja plamena moguća je pod sljedećim uvjetima:
- vatrena cijev je kratka;
- izgaranje se širi pri konstantnom tlaku bliskom atmosferskom.
Ako je duljina cijevi značajna, tada jednoliko širenje plamena za neke smjese može prijeći u vibracijsko, a zatim u detonacijsko s nadzvučnom brzinom gorenja (2000 m/s ili više), kada se smjesa zapali. zbog udarnog vala koji zagrijava smjesu na temperature iznad temperature paljenja. Detonacija se javlja u smjesama s velikim brzinama širenja plamena. Granice detonacijske koncentracije su uže od granica zapaljivosti smjesa plin-zrak i plin-kisik, vol. %: propan - 3,2–37, izobutan - 2,8–31, vodik - 15–90. Tlak koji nastaje tijekom detonacijskog izgaranja može desetke puta premašiti početni tlak i dovesti do uništenja cijevi i drugih posuda dizajniranih za visoke tlakove.
8.7. IZGARANJE U LAMINARNOM I TURBULENTNOM STRUJANJU

Riža. 8.3. fronta izgaranja
mješavina plina i zraka u
laminarno kretanje
Fronta plamena može se zaustaviti stvaranjem nadolazećeg kretanja zapaljive smjese brzinom koja je jednaka normalnoj brzini širenja plamena. Dobar primjer je površina unutarnjeg konusa Bunsenovog plamenika. Podešavanjem sastava mješavine plina i zraka koja istječe iz plamenika u laminarnom načinu gibanja, moguće je postići izgled stabilnog i oštro definiranog konusa izgaranja (slika 8.3). Bočna površina konusa (fronta plamena), koja je nepomična u odnosu na rub paljenja kanala plamenika, pomiče se prema izlaznoj smjesi plina i zraka, a plamen se u ovom slučaju širi duž normale na površinu paljenja na svakoj od njegove točke. Na površini konusne fronte plamena očuvana je jednakost brzina - projekcije brzine strujanja smjese plina i zraka na normalu wn na tvornicu stošca i normalnu brzinu širenja plamena ne poštuju Michelsonov zakon:
w n \u003d w znoj cosφ \u003d u n (8.26)
gdje je φ kut između smjera strujanja i normale na površinu konusne fronte plamena; w znoj - prosječna brzina protoka mješavine plina i zraka koja prolazi kroz plamenik po jedinici vremena, m/s.
Konstantnost normalne brzine širenja plamena vrijedi samo za glavni dio bočne površine stožaste fronte plamena. Na vrhu konusa brzina se povećava zbog zagrijavanja smjese plina i zraka usko razmaknutim dijelovima stožaste površine fronte plamena, a na dnu stošca se smanjuje zbog učinka hlađenja kraja dio vatrogasnog kanala plamenika.
Za praktične proračune ta se razlika obično zanemaruje i pretpostavlja se da je brzina prolaska smjese kroz frontu plamena konstantna na cijeloj površini stošca i jednaka u n.
Prosječna normalna brzina širenja plamena je
u n \u003d V cm / S (8,27)
gdje je V cm volumen mješavine plina i zraka koja prolazi kroz plamenik, S je površina konusnog fronta plamena.
U praksi, stožasta fronta plamena nema pravilan geometrijski oblik, stoga, za točno određivanje S, plamen se fotografira, fronta plamena je podijeljena u niz krnjih stožaca. Zbroj bočnih površina je ukupna površina stožaste fronte plamena. Vrijednosti normalnih brzina širenja plamena, određene metodom Bunsenovog plamenika i drugim metodama, iste su i jednake normalnim brzinama navedenim u tablici. 8.14.
Visina konusne fronte plamena ovisi uglavnom o veličini kanala izgaranja plamenika. Smanjenje visine plamena može se postići drobljenjem velikih vatrenih kanala u nekoliko malih. Za smjese plina i zraka istog sastava, visina stožastih fronti plamena malih kanala h može se približno odrediti iz visine fronte plamena jednog kanala H:
h = H/ √n(8.28)
gdje je n broj malih kanala.
Za plamenike visoke toplinske snage (plamenici industrijskih kotlova, peći itd.), Izgaranje se u pravilu odvija u turbulentnom toku - glatka stožasta fronta plamena je zamagljena i gubi svoj jasan konusni oblik zbog vrtložnog gibanja i pulsiranja. U ovom slučaju uočavaju se dva karakteristična tipa izgaranja, koja odgovaraju turbulenciji malih i velikih razmjera.
Na skalama turbulencije koje ne prelaze debljinu laminarne zone izgaranja, stožasta fronta plamena zadržava svoj oblik i ostaje glatka, iako se zona izgaranja povećava. Ako razmjeri turbulencije premašuju debljinu zone normalnog izgaranja, površina stožaste fronte plamena postaje neravna. To dovodi do povećanja ukupne površine fronte izgaranja i izgaranja veće količine gorive smjese po jedinici protočnog presjeka.
U slučaju turbulencije velikih razmjera, koja je mnogo veća od debljine laminarne zone izgaranja, poremećaj površine fronte plamena dovodi do odvajanja pojedinačnih čestica vruće smjese, koje se usitnjavaju naknadnim pulsacijama. Fronta plamena gubi cjelovitost i pretvara se u sustav odvojenih žarišta izgaranja u obliku jednakih čestica zapaljive smjese koje se dijele i izgaraju u struji.

Riža. 8.4. Relativna promjena brzine
širenje plamena koksnog plina
pomiješan sa zrakom ovisno o broju
Reynolds i način kretanja smjese
S turbulencijama velikih razmjera povećava se površina fronte plamena, koja se sastoji od površina svih gorućih čestica, što dovodi do naglog povećanja brzine širenja plamena (slika 8.4). U ovom slučaju može doći ne samo do frontalnog izgaranja, koje se širi normalnom brzinom v n , već i do volumetrijskog izgaranja koje nastaje zbog turbulentnih pulsacija vrućih proizvoda izgaranja u svježu smjesu. Posljedično, ukupna brzina širenja plamena tijekom turbulencije velikih razmjera određena je jednom ili drugom kombinacijom elemenata frontalnog i volumetrijskog izgaranja.
U nedostatku pulsiranja, turbulentna brzina izgaranja postaje jednaka normalnoj brzini širenja plamena. Naprotiv, ako je pulsirajuća brzina puno veća od normalne, turbulentna brzina izgaranja postaje malo ovisna o fizikalno-kemijskim svojstvima zapaljive smjese. Pokusi su pokazali malu ovisnost brzine izgaranja raznih homogenih plinsko-zračnih smjesa s α>1 u industrijskim pećima o normalnoj brzini širenja plamena.
8.8. STABILNOST GORENJA
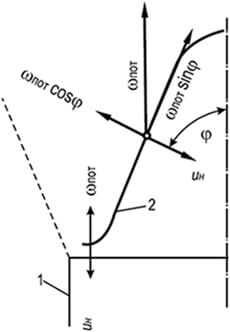
Riža. 8.5. Shema izravne naknade
u n \u003d w znoj tijekom laminarnog kretanja
smjesa plin-zrak
1 – stijenka plamenika;
2 - fronta plamena
Glavni čimbenici koji utječu na stabilnost izgaranja su brzina istjecanja smjese plina i zraka i širenje plamena. Pri izgaranju plinsko-zračnih smjesa u laminarnom strujanju stabilni dio stožaste fronte plamena je njezin donji dio. U tom trenutku se fronta plamena, zbog širenja smjese plina i zraka koja struji u atmosferu i efekta usporavanja stijenke kanala, okreće vodoravno i izdiže iznad ruba kanala za debljinu fronte plamena (sl. 8.5).
U ovom dijelu fronte dolazi do potpune kompenzacije brzine strujanja plin-zrak brzinom širenja plamena u n = w znoj . Na ostatku stožastog presjeka fronte plamena kompenzacija je djelomična i provodi se samo u smjeru normalnom na frontu izgaranja: u n = w znoj cosφ . Komponenta w sweat sinφ ostaje neuravnotežena i nosi točku paljenja od baze stošca do njegovog vrha. Stabilnost konusne fronte plamena objašnjava se činjenicom da prstenasti pojas u podnožju služi kao izvor paljenja, bez kojeg bi ostatak fronte bio odnesen strujanjem mješavine plina i zraka.
Ako brzina protoka smjese premašuje brzinu širenja plamena, širina trake za paljenje se smanjuje dok ne postane zanemariva. U tom slučaju je slomljena stabilnost fronte plamena i dolazi do odvajanja od plamenika. Ako brzina širenja plamena u prstenastom prizidnom području (ne na zidu) premašuje brzinu istjecanja smjese plina i zraka, plamen se uvlači u mješalicu plamenika (prekoračenje).
Kada su odvojeni, postoje:
- nestanak plamena iz plamenika i njegovo gašenje;
- odvajanje od ruba vatrenog kanala, kada plamen dosegne novu, prilično stabilnu poziciju u toku iznad plamenika;
- slom podignutog plamena i njegovo gašenje;
- izbacivanje podignute baklje do ruba vatrenog kanala plamenika;
- stvarajući suspendirani plamen kada se mlaz zapali na određenoj udaljenosti od plamenika.
Sve ove pojave su neprihvatljive, jer dovode do nakupljanja neizgorenog plina u okolnoj atmosferi ili u peći.
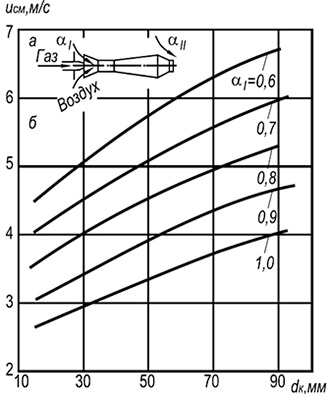
Riža. 8.6. Ovisnost brzine odvajanja pojedin
plamenovi u otvorenoj atmosferi mješavine prirodnih
plin sa zrakom na veličinu požarnog kanala i
sadržaj primarnog zraka.
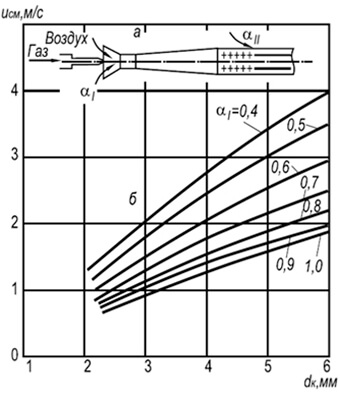
Riža. 8.7. Ovisnost o brzini odvajanja
multiflare plamen u otvorenoj atmosferi
smjese prirodnog plina sa zrakom na vel
požarni kanal i sadržaj primarnog zraka.
a - dijagram plamenika; b – krivulje odvajanja plamena
Na sl. Slika 8.6 prikazuje eksperimentalne krivulje odvajanja plamena od rubova vatrenih kanala injekcijskih plamenika s jednim plamenikom koji rade na mješavinu hladnog plina i zraka. Na granici i iznad ovih krivulja počinje odvajanje plamena, a ispod krivulja počinje stabilno izgaranje.
U praksi su rasprostranjeni plamenici za ubrizgavanje s više baklji i plamenim kanalima promjera 2–6 mm (slika 8.7). Određivanje brzina odvajanja plamena w ref za takve plamenike može se izvršiti prema sljedećoj formuli:
w neg = 3,5 10 -3 d k T 2 (1 + V t) / (1 + α 1 V t) (8,29)
gdje je d k promjer kanala za paljenje, m; α 1 - koeficijent viška primarnog zraka; T je apsolutna temperatura smjese plina i zraka, K.
Iz formule je vidljivo da se stabilnost izgaranja povećava s povećanjem promjera požarnih kanala i temperature, a smanjuje s povećanjem koeficijenta viška primarnog zraka. Stabilnost izgaranja također je povećana zbog međusobnog utjecaja plamena.
Do odvajanja plamena od kanala požara može doći i iz drugih razloga. Ako plamenik i dimni plinovi nisu pravilno postavljeni, mogu dospjeti u injektor plamenika i dovesti do odvajanja plamena (smanjenjem brzine širenja plamena u smjesi plin-zrak razrijeđenoj inertnim plinovima). Također, uzrok odvajanja može biti velika brzina sekundarnog zraka koji ispuhuje plamen iz kanala požara.
Tablica 8.15. Stopa homogene smjese prirodnih
plin sa zrakom, pri čemu dolazi do proboja
plamen, m/s (temperatura smjese 20°C)
| Promjeri pucajući kanala |
Omjer primarnog zraka | |||||
|---|---|---|---|---|---|---|
| 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | 1,1 | |
| 3,5 | 0,05 | 0,10 | 0,18 | 0,22 | 0,23 | 0,21 |
| 4,0 | 0,08 | 0,12 | 0,22 | 0,25 | 0,26 | 0,20 |
| 5,0 | 0,09 | 0,16 | 0,27 | 0,31 | 0,31 | 2,23 |
| 6,0 | 0,11 | 0,18 | 0,32 | 0,38 | 0,39 | 0,26 |
| 7,0 | 0,13 | 0,22 | 0,38 | 0,44 | 0,45 | 0,30 |
| 8,0 | 0,15 | 0,25 | 0,43 | 0,50 | 0,52 | 0,35 |
| 9,0 | 0,17 | 0,28 | 0,48 | 0,57 | 0,58 | 0,39 |
| 10,0 | 0,20 | 0,30 | 0,54 | 0,64 | 0,65 | 0,43 |
Također je neprihvatljivo da plamen treperi unutar miješalice plamenika, obično popraćeno pucanjem. Klizanje dovodi ili do gašenja plamena i izbacivanja neizgorene smjese u prostoriju ili ložište ili do izgaranja smjese unutar plamenika. Sklonost plamena bljeskanju ovisi o vrsti plina, normalnoj brzini širenja plamena, sadržaju primarnog zraka u mješavini plina i zraka, dimenzijama požarnih kanala, temperaturi smjese ili stijenki kanali. Na proboj plamena utječe i toplinska vodljivost materijala od kojih su izrađeni požarni kanali, njihov oblik, dubina i izrada, prisutnost neravnina, odlomljenih rubova itd.
Dano u tablici. 8.15 vrijednosti brzina homogenih smjesa prirodnih plinova sa zrakom, pri kojima dolazi do proboja, mogu se koristiti i za druge plinove, uz ispravke:
w" inc \u003d w inc u" n / u n (8.30)
gdje je w‘ pr brzina bljeskanja plamena za drugi plin, m / s; w pr - brzina klizanja za prirodni plin (prema tablici 8.15), m / s; u‘ n - normalna brzina širenja plamena za drugi plin, m/s; u n - brzina širenja plamena u metanu, m/s.
Maksimalna brzina klizanja može se izračunati pomoću približne formule:
w pr \u003d 0,73 10 -3 d k T 2 (8,31)
Ista se formula, s aproksimacijom dovoljnom za praksu, može koristiti i za druge plinove uz uvođenje korekcije za promjenu normalne brzine širenja plamena. Na temelju brojnih eksperimenata može se izvesti sljedeći zaključak: granice stabilnog rada plamenika ograničene su brzinama odvajanja i povratnog plamena.
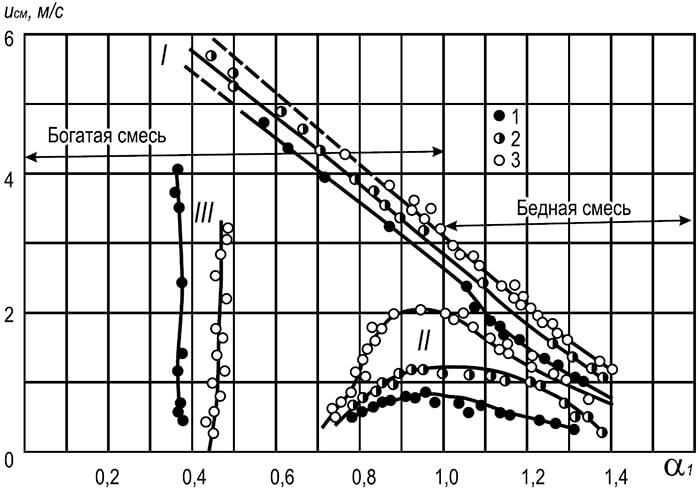
Riža. 8.8. Ovisnost brzine mješavine plina i zraka, pri kojoj dolazi do odvajanja i povratnog plamena, o koeficijentu viška primarnog zraka
I - odvajanje plamena; II - proboj plamena; III - žuti rubovi plamena;
1–3 promjera vatrenih kanala plamenika, mm: 1 – 25, 2 – 25, 3 – 32
Na sl. Slika 8.8 prikazuje krivulje koje karakteriziraju protoke mješavine prirodnog plina i zraka, pri kojima dolazi do odvajanja i povratnog plamena. Priroda krivulja ukazuje na oštro smanjenje stabilnosti plamena kako se sadržaj primarnog zraka u smjesi povećava. Povećanje stabilnosti plamena događa se smanjenjem udjela primarnog zraka i doseže maksimum kada se smanji na nulu (difuzijsko izgaranje). Međutim, takvo izgaranje ugljikovodičnih plinova u mnogim je slučajevima neprihvatljivo, jer dovodi do pojave žutih plamenova, koji karakteriziraju pojavu čestica čađe u njemu.
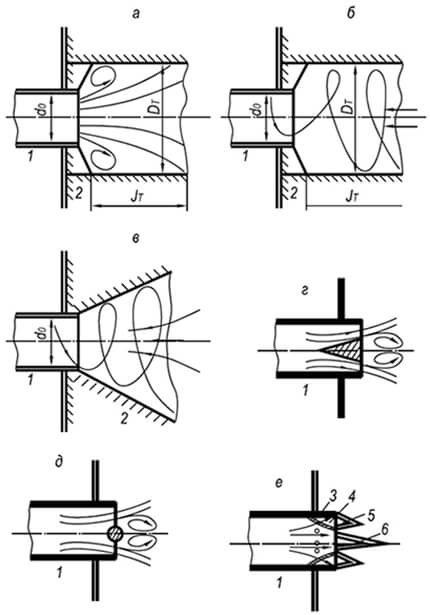
Riža. 8.9. Uobičajeni usporivači plamena
a - cilindrični tunel s naglim širenjem presjeka;
b - isto, s vrtložnim tokom;
c – stožasti tunel s vrtložnim strujanjem;
d - stabilizator u obliku stožastog tijela;
e - isto, u obliku okrugle šipke;
e - isto, u obliku stabilnog prstenastog plamena
1 - mlaznica plamenika; 2 - tunel; 3 - bočna rupa;
4 – prstenasti kanal; 5 - prstenasti plamen;
6 - plamen glavnog toka mješavine plina i zraka
U praksi, da bi se proširio raspon stabilnosti izgaranja bilo koje zapaljive smjese plina i zraka, pretpostavlja se da je brzina protoka nekoliko puta veća od brzine odvajanja. Sprječavanje odvajanja plamena postiže se upotrebom stabilizatora plamena (slika 8.9).
Za stabilizaciju plamena injekcijskih i drugih plamenika koji stvaraju osnosimetrične plinsko-zračne mlazove koriste se vatrostalni cilindrični tuneli s naglim širenjem poprečnog presjeka. Rad takvog tunela temelji se na perifernoj cirkulaciji dijela vrućih produkata izgaranja, do čega dolazi zbog razrijeđenosti koju stvara mlaz.
Za stabilizaciju plamena plamenika koji proizvode vrtložnu smjesu plina i zraka koriste se i cilindrični i konusni tuneli s kutom otvaranja od 30–60°. Kod vrtložnog strujanja veći tlak nastaje na periferiji tunela nego u njegovom središnjem dijelu. To dovodi do paraksijalne recirkulacije nekih vrućih produkata izgaranja i paljenja hladne smjese plina i zraka koja ulazi u tunel iznutra.
Kada ugradnja tunela nije moguća, za stabilizaciju plamena koriste se tijela slabo aerodinamičnog oblika koja se postavljaju u strujanje plinsko-zračne smjese na izlazu iz vatrenog kanala plamenika. U ovom slučaju, paljenje smjese događa se na obodu stabilizatora, iza kojeg postoji djelomična recirkulacija vrućih plinova koji pale zapaljivu smjesu iznutra. Stabilizirajući učinak takvih uređaja manji je od učinka tunela.
U plamenicima s jednim i više plamenika za ubrizgavanje, stabilizatori izgaranja naširoko se koriste u obliku posebne plamene mlaznice. Stabilizacijski učinak ovog uređaja temelji se na sprječavanju razrjeđivanja glavnog toka u korijenu plamena viškom zraka, čime se sužavaju granice njegove stabilnosti, kao i na zagrijavanju i paljenju glavnog toka prstenastim plamenom po cijeloj periferiji. . Stabilnost prstenastog plamena tijekom odvajanja postiže se takvim omjerom presjeka vatrenog prstena i bočnih rupa, u kojima brzina smjese plina i zraka u prstenastoj šupljini ne prelazi normalnu brzinu širenja plamena. Kako bi se spriječilo bljeskanje plamena u mješalicu plamenika, dimenzije bočnih rupa koje tvore prstenasti plamen uzimaju se manje od kritičnih.
8.9. ŠEME ZAŠTITNIKA PLAMENA
Zrak ili kisik koji ulaze u plinovod mogu stvoriti eksplozivnu smjesu, stoga je nužno zaštititi cjevovode od prodiranja zraka ili kisika u njih. U svim eksplozivnim industrijama moraju se stvoriti uvjeti koji isključuju mogućnost zapaljivih impulsa. Izvori paljenja koji uzrokuju eksploziju smjese plina i zraka su:
- otvoreni plamen;
- električna pražnjenja radne električne opreme;
- kratki spoj u električnim žicama;
- iskre u električnim uređajima;
- pregorjeli otvoreni osigurači;
- pražnjenja statičkog elektriciteta.
Sigurnost od eksplozije osiguravaju različiti hvatači plamena. ugrađeni u cjevovode, na spremnike, na vodove za pročišćavanje plina, svijeće i druge sustave gdje postoji opasnost od eksplozije.
Gašenje plamena u kanalu ispunjenom zapaljivom smjesom događa se samo pri minimalnom promjeru kanala, što ovisi o kemijskom sastavu i tlaku smjese, a objašnjava se gubitkom topline iz reakcijske zone na stijenke kanala. Sa smanjenjem promjera kanala povećava se njegova površina po jedinici mase reakcijske smjese, tj. gubici topline se povećavaju. Kada dosegnu kritičnu vrijednost, brzina reakcije izgaranja toliko se smanjuje da daljnje širenje plamena postaje nemoguće.
Sposobnost gašenja plamena odvodnika plamena ovisi uglavnom o promjeru kanala za gašenje, a znatno manje o njihovoj duljini, a mogućnost prodora plamena kroz kanale za gašenje ovisi uglavnom o svojstvima i sastavu gorive smjese i tlaku. Normalna brzina širenja plamena glavna je veličina koja određuje veličinu kanala za gašenje i izbor vrste plamenika: što je veća, to je manji kanal potreban za gašenje plamena. Također, dimenzije kanala za gašenje ovise o početnom tlaku zapaljive smjese. Za ocjenu vatrootporne sposobnosti hvatača plamena, tzv. Peclet Re kriterij:
Pe \u003d w cm dc p p / (RT 0 λ 0) (8.32)
U granici gašenja plamena formula Pecletovog kriterija ima oblik:
Re cr = w cm d cr c p p cr /(RT 0 λ 0) (8.33)
gdje je w cm normalna brzina širenja plamena; d je promjer prigušnog kanala; d kp - kritični promjer kanala za gašenje; c p je specifični toplinski kapacitet plina pri 0°C i konstantnom tlaku; p - tlak plina; p cr - kritični tlak plina; R je univerzalna plinska konstanta; T 0 - apsolutna temperatura plina; λ 0 - toplinska vodljivost početne smjese.
Dakle, za izračunavanje sposobnosti zaustavljanja plamena odvodnika plamena potrebni su sljedeći početni podaci:
- normalne brzine širenja plamena zapaljivih plinskih smjesa;
- stvarna veličina maksimalnih kanala za gašenje danog plamenika.
Ako je dobivena vrijednost veća od Re cr = 65, plamenik neće odgoditi širenje plamena ove zapaljive smjese, i obrnuto, ako je Re< 65, огнепреградитель задержит распространение пламени. Запас надежности огнепреградителя, который находят из отношения Ре кр к вычисленному значению Ре, должен составлять не менее 2:
P \u003d Re cr / Re \u003d 65 / Re\u003e 2,0 (8,34)
Koristeći činjenicu da je Pe cr konstantan na granici gašenja plamena, moguće je izračunati približni kritični promjer kanala za bilo koju zapaljivu smjesu, ako je poznata brzina širenja plamena, kao i toplinski kapacitet i toplinska vodljivost plinski sustav. Preporučuju se sljedeći kritični promjeri kanala za gašenje, mm:
- pri izgaranju mješavine plina i zraka - 2,9 za metan i 2,2 za propan i etan;
- pri izgaranju smjesa kisika u cijevima (pri apsolutnom tlaku od 0,1 MPa u uvjetima slobodnog širenja produkata izgaranja) - 1,66 za metan i 0,39 za propan i etan.
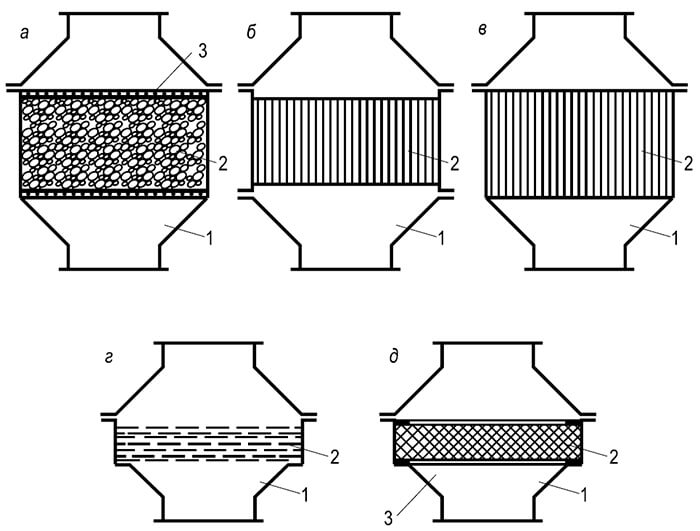
Riža. 8.10. Vrste odvodnika plamena:
a - pakirano; b - kazeta; c - lamelarni; g - mreža; e - kermet
Strukturno, odvodnici plamena podijeljeni su u četiri tipa (Sl. 8.10):
- s mlaznicom od zrnatih materijala;
- s izravnim kanalima;
- od kermeta ili metalnih vlakana;
- mreža.
Prema načinu ugradnje - u tri vrste: na cijevima za izbacivanje plinova u atmosferu ili na plameniku; o komunikacijama; ispred plinskih plamenika.
U tijelu montiranog odvodnika plamena, između rešetki, nalazi se mlaznica s punilom (staklene ili porculanske kuglice, šljunak, korund i druge granule od izdržljivog materijala). Kazetni odvodnik požara je kućište u koje je ugrađena kazeta za gašenje požara od rebrastih i ravnih metalnih traka čvrsto smotanih u rolu. U slučaju pločastog odvodnika plamena - paket ravnih paralelnih metalnih ploča sa strogo određenim razmakom između njih. Kod mrežastog odvodnika plamena u tijelu nalazi se paket čvrsto stisnutih metalnih mreža. Keramičko-metalni odvodnik plamena je kućište unutar kojeg je ugrađena porozna metal-keramička ploča u obliku ravnog diska ili cijevi.
Najčešće se koriste mrežasti hvatači plamena (početkom 19. stoljeća počeli su se ugrađivati u rudarske svjetiljke (Devi lampe) za sprječavanje eksplozije ložišta). Ovi hvatači plamena preporučuju se za zaštitu instalacija koje izgaraju plinovita goriva. Zaštitnik plamena sastoji se od nekoliko slojeva mjedene mreže s veličinom oka od 0,25 mm, smještenih između dvije perforirane ploče. Mrežasti paket je ojačan u odvojivom kavezu.
Tijelo odvodnika plamena izrađeno je od lijevanog željeza ili legure aluminija i sastoji se od dva identična dijela spojena vijcima s uklonjivom kopčom koja se nalazi između njih. Osim razmatranih suhih odvodnika plamena, tekući sigurnosni zatvarači naširoko se koriste za zaštitu plinovoda od prodora eksplozivnog vala i plamena tijekom plinsko-plamenske obrade metala, kao i cjevovoda i uređaja napunjenih plinom od prodiranja kisika i zraka u njih.
Tekuće brtve moraju:
- za sprječavanje širenja eksplozivnog vala tijekom obrnutih udara i tijekom paljenja plinova;
- zaštititi plinovod od ulaska kisika i zraka u njega;
- osigurati minimalni hidraulički otpor prolazu protoka plina. Osim toga, tekućina iz zatvarača ne smije se odnijeti u obliku kapljica u značajnijim količinama.
8.10. NAČELA IZGARANJA
Procesi izgaranja plinova temelje se na principima koji se konvencionalno nazivaju kinetički i difuzijski. Kod kinetičkog principa, prije početka izgaranja stvara se homogena smjesa s nešto viška zraka. Izgaranje takve smjese odvija se u kratkom prozirnom plamenu bez stvaranja čestica čađe u plamenu. Za izgaranje plina prema kinetičkom principu koriste se posebni mješači ili injekcijski plamenici koji pripremaju homogenu plinsko-zračnu smjesu s omjerom viška primarnog zraka α 1 = 1,02 : 1,05.
S manjim sadržajem primarnog zraka, prema kinetičkom principu, odvija se samo početni stupanj izgaranja, do iskorištenja kisika, koji je u smjesi s plinom. Preostali plinovi i produkti nepotpunog izgaranja izgaraju vanjskom difuzijom kisika (sekundarni zrak), tj. prema d i f u z i o n n o m na principu. Za α 1< 1 у факела есть два видимых фронта горения: внутренний, возникающий за счет первичного воздуха, и наружный, образующийся за счет диффузии кислорода из окружающей среды. Общая высота пламени при таком горении возрастает, а температура - несколько снижается. Устойчивость пламени и его прозрачность зависят от содержания первичного воздуха в смеси: чем оно выше, тем ниже устойчивость пламени, больше его прозрачность, и наоборот.
Princip izgaranja plina s α 1< 1,0 является п р о м е ж у т о ч н ы м (между кинетическим и диффузионным). С учетом этого принципа конструируются все газовые аппараты с инжекционными горелками. В таких горелках содержание первичного воздуха в смеси принимается в зависимости от вида газа таким, чтобы:
- u plamenu nije bilo čestica čađe;
- stabilnost izgaranja je osigurana s promjenama toplinske snage u svim granicama potrebnim u praksi.
Po principu difuzije (α 1 = 0) procesi izgaranja i miješanja odvijaju se paralelno. Budući da se procesi miješanja odvijaju znatno sporije od procesa izgaranja, brzina i potpunost izgaranja određena je brzinom i potpunošću miješanja plina i zraka. Miješanje plina sa zrakom u ovom slučaju može se dogoditi difuzijom (bilo sporom molekularnom ili turbulentnom, uključujući molekularnu kao završnu fazu). Sukladno tome razlikuju se brzina gorenja i struktura difuzijskog plamena.
Značajke takvog spaljivanja:
- stabilnost plamena kada se toplinska snaga mijenja od nule do najveće moguće prema uvjetima odvajanja;
- postojanost temperature po cijeloj visini plamena;
- mogućnost raspodjele na velikim proizvoljnim površinama;
- kompaktnost plamenika i jednostavnost njihove izrade;
- značajna visina plamena i neizbježnost pirolitičkih procesa koji dovode do stvaranja svijetlog čađavog plamena.
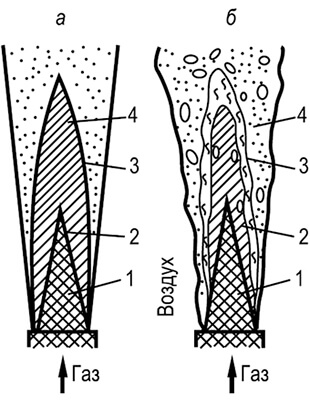
Riža. 8.11. Struktura slobodnih plamenova:
a - laminarni plamen; b - turbulentni plamen
Difuzijsko izgaranje može se pretvoriti u kinetičko ili srednje izgaranje ako je miješanje ispred procesa izgaranja. U praksi se to može postići prisilnim dovodom zraka, što dovodi do stvaranja kvazihomogene plinsko-zračne smjese s α 1 > 1,0, koja gori u prozirnom plamenu.
Za ilustraciju principa izgaranja na sl. 8.11. date su sheme slobodnih plamenova: laminarni i turbulentni. Laminarna baklja nastaje zbog međusobne molekularne difuzije plina i zraka. Unutar konusne jezgre 1 nalazi se čisti plin koji teče iz cijevi pod laminarnim strujanjem. U zoni 2 - mješavina plina i produkata izgaranja, u zoni 3 - mješavina produkata izgaranja i zraka. Granica 4 je glatka stožasta fronta plamena, na koju molekule zraka difundiraju izvana, a molekule plina iznutra. Produkti izgaranja djelomično difundiraju prema plinu, intenzivno ga zagrijavajući u predplamenskoj zoni. To dovodi do pirolize ugljikovodika i stvaranja čađavih čestica, dajući plamenu jarku svjetlost.
Izgaranje se može pojačati turbulentnošću tokova miješanja. Turbulentni plamen nema jasnu konusnu frontu izgaranja, on je "zamućen" i razbijen pulsacijama u zasebne čestice.
Struktura plamena sastoji se od jezgre čistog plina 1, zone relativno sporog izgaranja 2, difuzne zone najintenzivnijeg izgaranja 3 s visokim sadržajem produkata izgaranja i zone izgaranja 4 s prevlašću zraka u njoj. Nema jasno definiranih granica između zona, one se stalno pomiču ovisno o stupnju turbulencije strujanja. Karakteristike turbulentnog plamena su:
- tijek procesa izgaranja gotovo u cijelom volumenu;
- povećanje intenziteta izgaranja;
- visoka transparentnost plamena;
- njegova manja otpornost na odvajanje.
Turbulentno izgaranje plina naširoko se koristi u pećima raznih kotlova i peći. Za intenziviranje procesa izgaranja koriste se prirodne (zbog povećanih brzina) i umjetne turbulencije strujanja, na primjer, vrtloženjem strujanja zraka i dovođenjem tankih mlaznica plina u njega pod različitim kutovima.
8.11. UVJETI ZA STVARANJE PRODUKATA NEPOTPUNOG IZGARANJA I SMANJENJE KONCENTRACIJE ŠTETNIH TVARI U NJIMA
Kod izgaranja zapaljivih plinova produkti izgaranja mogu sadržavati komponente potpunog (ugljični dioksid i vodena para) i nepotpunog izgaranja (ugljični monoksid, vodik, nezasićeni, zasićeni, aromatski ugljikovodici i čestice čađe). Osim toga, u produktima izgaranja uvijek se nalaze dušikovi oksidi. Prisutnost proizvoda nepotpunog izgaranja u značajnim koncentracijama je neprihvatljiva, jer dovodi do onečišćenja zraka otrovnim tvarima i smanjenja učinkovitosti instalacija koje rade na plinsko gorivo.
Glavni razlozi za njihov visok sadržaj:
- goreći plinovi s nedostatkom zraka;
- loše miješanje zapaljivih plinova i zraka prije i tijekom izgaranja;
- prekomjerno hlađenje plamena prije završetka reakcija izgaranja.
Za metan, reakcije izgaranja (ovisno o koncentraciji kisika u reakcijskoj smjesi) mogu se opisati sljedećim jednadžbama:
CH 4 + 2O 2 \u003d CO 2 + 2H 2 O + 800,9 MJ / mol
u stehiometrijskom omjeru ili s viškom oksidacijskog sredstva;
CH 4 + O 2 \u003d CO + H 2 + H 2 O + Q i CH 4 + 0,5 O 2 \u003d CO + 2H 2 O + Q
u nedostatku oksidirajućeg sredstva.

Riža. 8.12. Međuprodukti izgaranja
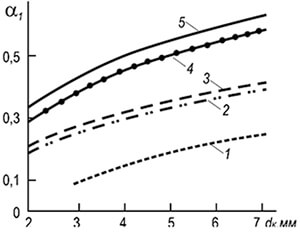
Riža. 8.13. Sadržaj primarnog zraka,
koji sprječava nastanak
žuti jezici u plamenu
Plin: 1 - koks;
2 - polja prirodnog plina;
3 - naftna polja;
4 - propan; 5 - butan
Na sl. 8.12 prikazuje približan prosječni sastav nekih intermedijarnih spojeva - vodika, ugljikovog monoksida, etilena, acetilena i relativno malog broja zasićenih i jednostavnih aromatskih spojeva - i ugljičnog dioksida koji se pojavljuju u plamenu tijekom difuzijskog izgaranja prirodnog plina (97%). Plin je spaljen u laminarnoj baklji, plin je istjecao iz cijevi promjera 12 mm. Ukupna visina plamena 130–140 mm.
Najveća koncentracija vodika i acetilena postiže se približno na istoj visini plamena; nestaju gotovo istodobno na vrhu svjetleće zone plamena. Od svih međuspojeva koji nastaju u plamenu (isključujući čađave čestice), ugljični monoksid posljednji nestaje. To daje osnovu da se njegovim indeksom ocijeni potpunost izgaranja plina. U produktima izgaranja uvijek su prisutni dušikovi oksidi, čija se maksimalna koncentracija javlja u zonama intenzivnog izgaranja ugljičnog monoksida i vodika.
Izgaranje ugljikovodičnih plinova s nedostatkom oksidansa dovodi do stvaranja čestica čađe, dajući plamenu žutu boju. Proces izgaranja čađe odvija se u fazama i relativno sporo. Ponekad je izgaranje formiranih čestica čađe odgođeno i može potpuno prestati kada uđu u područje niske temperature baklje ili kada se površine za izmjenu topline isperu plamenom. Dakle, prisutnost svjetlećeg plamena uvijek ukazuje na pojavu pirolitičkih procesa i mogućnost kemijske nepotpunosti izgaranja, posebno u malim zaštićenim ložištima kotlova.
Sprječavanje stvaranja čestica čađe postiže se prethodnim miješanjem plinova ugljikovodika s dovoljnom količinom oksidacijskog sredstva. Sadržaj primarnog zraka u smjesi, pri kojem se javlja proziran plamen, ne ovisi samo o vrsti ugljikovodika, već io uvjetima miješanja sa sekundarnim zrakom (promjer kanala izgaranja plamenika) (Sl. 8.13. ). Na rubu i iznad krivina plamen je proziran, a ispod krivina ima žute jezike. Krivulje pokazuju da sadržaj primarnog zraka u smjesi raste s povećanjem broja ugljikovih atoma u molekuli i promjera kanala izgaranja plamenika. Omjer viška primarnog zraka α 1 u smjesi, pri kojem nestaje žuti plamen, ovisno o gore navedenim čimbenicima, može se odrediti za male vatrene kanale plamenika:
α 1 \u003d 0,12 (m + n / 4) 0,5 (d k / d 0) 0,25 (8,35)
gdje su m i n broj atoma ugljika i vodika u molekuli ili njihov prosječni broj za složeni plin; d k - promjer vatrenih kanala plamenika, mm; d 0 - referentni promjer kanala plamenika (1 mm).
Osiguravanje potpunog izgaranja u praktičnim uvjetima prilično je kompliciran zadatak, koji ne ovisi samo o principu izgaranja plina, već io uvjetima za razvoj plamena u volumenu peći. Najviši zahtjevi za potpunost izgaranja postavljaju se na kućanske aparate i druge instalacije koje proizvode izgaranja ispuštaju u atmosferu. Izgaranje plina u takvim instalacijama je najteže, jer je povezano s pranjem hladnih površina za izmjenu topline plamenom. Za izgaranje plina u kućanskim pećima koriste se injekcioni plamenici s više baklji, koji tvore homogenu smjesu s koeficijentom viška primarnog zraka α 1< 1. Недостающий для сгорания газа воздух поступает за счет диффузии из окружающей атмосферы.
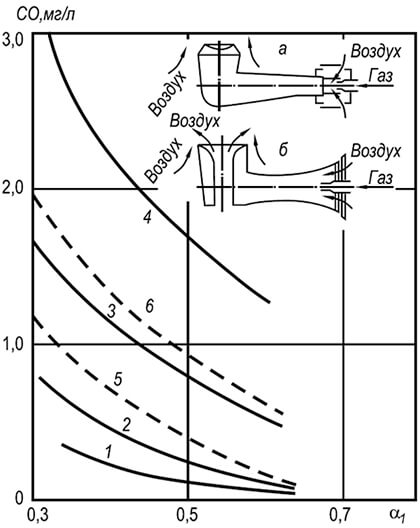
Riža. 8.14. Koncentracija ugljičnog monoksida
u produktima izgaranja u plinskom štednjaku
a – plamenik s perifernim dovodom sekundarnog zraka;
b - sa središnjim i perifernim dovodom sekundarnog zraka
1 - prirodni plin, plamenik s perifernim napajanjem
sekundarni zrak, udaljenost do dna posude 25 mm;
2–4 - prirodni plin, plamenik s perifernim i
centralni dovod sekundarnog zraka, udaljenost
do dna posude, mm: 2 - 25, 3 - 18, 4 - 10;
5 - ukapljeni plin, plamenik sa središnjim i perifernim
dovod sekundarnog zraka, razmak do dna posude 25 mm;
6 - ukapljeni plin, plamenik s perifernim napajanjem
Na sl. 8.14 prikazuje dijagrame plamenika s 2 plamenika za kućanske plinske peći i prosječnu koncentraciju ugljičnog monoksida CO u produktima izgaranja prirodnog metana (95 vol.%) i propana (93 vol.%) kada plamenici rade s nazivnom toplinom izlaz. Razlika između plamenika je u tome što se sekundarni zrak na jedan od njih dovodi samo s periferije, a na drugi - i s periferije i iz središnjeg kanala.
Potpunost izgaranja plina ovisi o koeficijentu viška primarnog zraka u smjesi, udaljenosti od kanala plamenika do dna posude, vrsti zapaljivog plina i načinu dovoda sekundarnog zraka. Istodobno, povećanje sadržaja primarnog zraka u smjesi, kao i povećanje udaljenosti od plamenika do dna posude, dovode do smanjenja koncentracije ugljičnog monoksida u produktima izgaranja. Minimalna koncentracija ugljičnog monoksida odgovara koeficijentu viška primarnog zraka α 1 = 0,6 i više i udaljenosti od plamenika do dna posude 25 mm, a maksimalna - α 1 = 0,3 i niže i udaljenosti od plamenik do dna posude 10 mm. Osim toga, povećanje toplinske snage plamenika za 15–20% zbog povećanja tlaka plina dovodi do povećanja koncentracije ugljičnog monoksida u produktima izgaranja za 1,2–1,3 puta, a zbog topline izgaranja plina, za 1,5–2 puta.
Posebnu pozornost treba obratiti na pojavu aromatskih spojeva tijekom procesa izgaranja - benzena, policikličkog benzpirena, benzantracena i dr., budući da su neki od njih kancerogeni. Proces njihovog nastanka vrlo je složen i odvija se u fazama. U prvoj fazi pojavljuje se acetilen i njegovi derivati. U zoni plamena ove tvari podliježu procesima produljenja lanca s preraspodjelom trostrukih ugljikovih veza u dvostruke. Kao rezultat ciklizacije i dehidracije dolazi do pojave raznih aromatskih spojeva, uključujući policikličke.
Tablica 8.16. Prosječna koncentracija ugljičnog monoksida i benzo(a)pirena u produktima izgaranja ovisno o vrsti plina, vrsti plamenika i koeficijentu viška primarnog zraka (toplinsko opterećenje plamenika - 1600 kcal/h, udaljenost plamenika od dna posude) - 24–26 mm)
| Vrsta plamenika | Prosječna koncentracija | |
|---|---|---|
| ugljikov monoksid, mg/l (u smislu α = 1,0) |
benzo(a)piren, mcg / 100 m 3 |
|
| Prirodni gas | ||
pri α i = 0,60 ÷ 0,70 |
0,10 | Nije pronađeno |
pri α i = 0,30 ÷ 0,35 |
1,20 | Tragovi |
pri α i = 0,60 ÷ 0,70 |
0,50 | Nije pronađeno |
pri α i = 0,30 ÷ 0,35 |
0,12 | Nije pronađeno |
| Ukapljeni naftni plin | ||
| Plamenik s perifernim dovodom sekundarnog zraka: | ||
pri α i = 0,60 ÷ 0,70 |
0,30 | 0,03 |
pri α i = 0,30 ÷ 0,35 |
1,20 | 1,10 |
| Plamenik sa središnjim i perifernim dovodom sekundarnog zraka: | ||
pri α i = 0,60 ÷ 0,70 |
0,07 | 0,02 |
pri α i = 0,30 ÷ 0,35 |
1,00 | 0,045 |
Tablični podaci. 8.16 pokazuju da pri izgaranju prirodnih plinova s koeficijentom viška primarnog zraka α 1 \u003d 0,6 i većim na obje vrste plamenika koncentracija ugljičnog monoksida u produktima izgaranja zadovoljava zahtjeve GOST 5542–87.
Tablica 8.17. Razmak između rubova kanala za paljenje injekcionih jednorednih plamenika, ovisno o njihovim dimenzijama i koeficijentu viška primarnog zraka
| Promjeri požarnog kanala, mm | Razmaci između rubova kanala, mm pri različitim vrijednostima koeficijenta viška primarnog zraka α 1 | ||||
|---|---|---|---|---|---|
| 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | |
| 2,0 | 11 | 8 | 6 | 5 | 4 |
| 3,0 | 15 | 12 | 9 | 7 | 5 |
| 4,0 | 16 | 14 | 11 | 9 | 7 |
| 5,0 | 18 | 15 | 14 | 12 | 10 |
| 6,0 | 20 | 18 | 16 | 14 | 12 |
Istraživanja su pokazala da razmaci između rubova požarnih kanala, koji osiguravaju brzo širenje plamena, sprječavajući njihovo spajanje, ovise o njihovoj veličini i sadržaju primarnog zraka u smjesi, smanjujući se s njegovim povećanjem. Optimalne udaljenosti između rubova kanala, koje osiguravaju dovoljnu potpunost izgaranja plina i brzo širenje plamena, dane su u tablici. 8.17. Kada su kanali za paljenje raspoređeni u dva reda šahovski, razmaci između rubova mogu se uzeti prema istoj tablici. U tom slučaju, udaljenosti između redova trebaju biti 2-3 puta veće od udaljenosti između kanala.
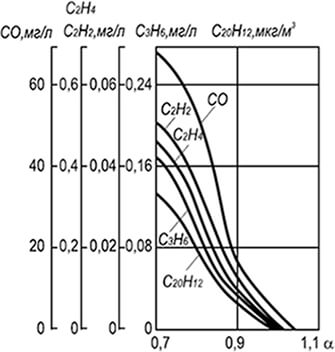
Riža. 8.15. Koncentracija ugljičnog monoksida, acetilena,
etan, etilen i benzo(a)piren u produktima izgaranja
plin srednjeg tlaka u plameniku za ubrizgavanje
Generalizacija brojnih eksperimentalnih podataka omogućila je dobivanje krivulja prosječne koncentracije u produktima izgaranja različitih komponenti, koje kvalitativno i kvantitativno karakteriziraju proces izgaranja (slika 8.15). Potpuno izgaranje homogene plinsko-zračne smjese postiže se samo kada je koeficijent viška primarnog zraka α = 1,05 i veći. Sa smanjenjem udjela zraka u smjesi, posebno na α< 1,0, возрастает концентрация оксида углерода СО, ацетилена С 2 Н 2 , этилена С 2 Н 4 , пропилена С 3 Н 6 и пропана С 3 Н 8 , а также бенз(а)-пирена С 20 Н 9 . Также возрастает концентрация и других компонентов - водорода, бензола и др.
Uz razmatrane produkte nepotpunog izgaranja, izgaranjem plina uvijek nastaje određena količina dušikovih oksida, čije se stvaranje događa u zonama visokih temperatura kako nakon završetka glavnih reakcija izgaranja, tako i tijekom izgaranja. Maksimalna koncentracija NO x javlja se u završnim fazama, što odgovara izgaranju plina i intenzivnom izgaranju međuproizvoda u obliku vodika i ugljikovog monoksida.
Primarni spoj u izgaranju smjesa plina i zraka je dušikov oksid. Početak lančane reakcije povezan je s atomskim kisikom koji nastaje u zonama visoke temperature zbog disocijacije molekularnog kisika:
O 2 -› 2O - 490 kJ / mol (8.36)
O + N 2 -› NO + N - 300 kJ / mol (8.37)
N + O 2 –› 2NO + 145 kJ/mol (8.38)
ravnotežna reakcija
N 2 + O 2 -› 2NO - 177 kJ / mol (8,39)
Stvaranje atomskog kisika također se događa tijekom djelomične disocijacije produkata izgaranja: sniženjem temperature i prisutnošću kisika dio nastalog dušikovog oksida (1–3 vol.%) oksidira se u dušikov dioksid NO 2 . Reakcija se najintenzivnije odvija nakon oslobađanja dušikovog oksida u atmosferu. Glavni čimbenici utjecaja:
- temperatura u reakcijskim zonama;
- omjer viška zraka i vrijeme kontakta komponenti koje reagiraju.
Temperatura plamena ovisi o kemijskom sastavu plina, sadržaju zraka u smjesi plin-zrak, stupnju njegove homogenosti i odvođenju topline iz reakcijske zone. Maksimalna moguća koncentracija dušikovog oksida pri određenoj temperaturi, vol. %, može se izračunati pomoću formule
NO p \u003d 4,6e -2150 / (RT) / √ O 2 N 2 (8,40)
gdje je NO p ravnotežna koncentracija dušikovog oksida, vol. %; R je univerzalna plinska konstanta; T - apsolutna temperatura, K; O 2 i N 2 - koncentracija, vol. % kisika i dušika.
Visoka koncentracija dušikovog oksida, razmjerna ravnotežnoj, nastaje pri izgaranju plina u ložištima snažnih parogeneratora te u visokotemperaturnim ložištima, koksnim i sličnim pećima. U kotlovima male i srednje snage, u malim grijaćim i toplinskim pećima sa značajnim odvođenjem topline i kratkim vremenom zadržavanja komponenti u visokotemperaturnim zonama, izlaz dušikovog oksida je red veličine manji. Osim toga, što je kraće vrijeme zadržavanja komponenti koje reagiraju u zoni visoke temperature, to je manje dušikovog oksida u produktima izgaranja.
Izgaranje plina u radijacijskim plamenicima i u fluidiziranom sloju također je učinkovito: u tim slučajevima dolazi do mikroflakernog izgaranja homogene smjese plina i zraka s koeficijentom viška zraka α = 1,05 s vrlo intenzivnim uklanjanjem topline iz reakcijske zone. Koncentracija dušikovih oksida tijekom izgaranja plina u radijacijskim plamenicima je oko 40, au fluidiziranom sloju - 80–100 mg/m 3 . Smanjenje veličine vatrenih kanala radijacijskih plamenika i vatrostalnih zrnaca u fluidiziranom sloju pomaže u smanjenju izlaza dušikovih oksida.
Prikupljeni podaci omogućili su niz promjena u dizajnu kotla i opreme za grijanje, pružajući ne samo visoku učinkovitost i nisku koncentraciju proizvoda nepotpunog izgaranja, već i smanjene emisije dušikovih oksida u atmosferu. Te promjene uključuju:
- smanjenje duljine visokotemperaturnih tunela i premještanje izgaranja iz njih u peći;
- korištenje stabilizatora izgaranja umjesto keramičkih tunela u obliku blef tijela ili prstenastog plamena;
- organizacija ravnog plamena s povećanom površinom prijenosa topline;
- raspršivanje plamena povećanjem broja plamenika ili korištenjem blok plamenika;
- stepenasti dovod zraka u reakcijsku zonu;
- ravnomjerna raspodjela toplinskih tokova u peći, ekranizacija peći i njihova podjela u odjeljke ekranima;
- primjena difuzijskog principa izgaranja plinova (difuzijsko izgaranje dopušteno je samo u slučajevima kada se može osigurati slobodno razvijanje plamena bez ispiranja površina za izmjenu topline).
Najučinkovitije smanjenje proizvodnje dušikovih oksida postiže se istovremenom primjenom nekoliko metoda.
Izgaranje plina je kombinacija sljedećih procesa:
Miješanje zapaljivog plina sa zrakom
zagrijavanje smjese
toplinska razgradnja zapaljivih komponenti,
Paljenje i kemijsko spajanje zapaljivih komponenti s atmosferskim kisikom, praćeno stvaranjem baklje i intenzivnim oslobađanjem topline.
Sagorijevanje metana odvija se prema reakciji:
CH 4 + 2O 2 \u003d CO 2 + 2H 2 O
Potrebni uvjeti za izgaranje plina:
Osiguravanje potrebnog omjera zapaljivog plina i zraka,
zagrijavanje do temperature paljenja.
Ako je mješavina plina i zraka manja od donje granice zapaljivosti, tada neće izgorjeti.
Ako u smjesi plina i zraka ima više plina od gornje granice zapaljivosti, tada neće izgorjeti u potpunosti.
Sastav proizvoda potpunog izgaranja plina:
CO 2 - ugljikov dioksid
H 2 O - vodena para
* N 2 - dušik (ne reagira s kisikom tijekom izgaranja)
Sastav produkata nepotpunog izgaranja plina:
CO - ugljikov monoksid
C - čađa.
Za izgaranje 1 m 3 prirodnog plina potrebno je 9,5 m 3 zraka. U praksi je potrošnja zraka uvijek veća.
Stav stvarna potrošnja zraka do teoretski potreban protok naziva se koeficijent viška zraka: α = L/L t .,
Gdje: L- stvarni trošak;
L t - teorijski potreban protok.
Koeficijent viška zraka uvijek je veći od jedan. Za prirodni plin to je 1,05 - 1,2.
2. Namjena, uređaj i glavne karakteristike protočnih grijača vode.
Protočni plinski bojleri. Predviđeni su za zagrijavanje vode na određenu temperaturu tijekom istjecanja.Protočni grijači vode dijele se prema opterećenju toplinske snage: 33600, 75600, 105000 kJ, prema stupnju automatizacije - na najviše i prve klase. učinkovitost grijači vode 80%, sadržaj oksida nije veći od 0,05%, temperatura produkata izgaranja iza prekidača propuha nije niža od 180 0 C. Princip se temelji na grijanju vode tijekom razdoblja izvlačenja.
Glavne jedinice protočnih grijača vode su: plinski plamenik, izmjenjivač topline, sustav automatizacije i izlaz plina. Niskotlačni plin dovodi se u plamenik za ubrizgavanje. Produkti izgaranja prolaze kroz izmjenjivač topline i ispuštaju se u dimnjak. Toplina izgaranja prenosi se na vodu koja teče kroz izmjenjivač topline. Za hlađenje vatrogasne komore koristi se zavojnica, kroz koju cirkulira voda, prolazeći kroz grijač. Plinski protočni grijači vode opremljeni su uređajima za odvod plina i prekidačima propuha, koji u slučaju kratkotrajnog prekida propuha sprječavaju gašenje plamena plinskog plamenika. Za spajanje na dimnjak postoji dimovodna cijev.
Plinski protočni bojler - VPG. Na prednjoj stijenci kućišta nalaze se: gumb za upravljanje plinskom slavinom, tipka za uključivanje elektromagnetskog ventila i prozorčić za promatranje plamena pilota i glavnog plamenika. Na vrhu uređaja nalazi se uređaj za odvod dima, na dnu su ogranci za spajanje uređaja na sustave plina i vode. Plin ulazi u solenoidni ventil, plinski zaporni ventil bloka plamenika vode i plina sekvencijalno uključuje pilot plamenik i dovodi plin u glavni plamenik.
Blokiranje protoka plina do glavnog plamenika, uz obavezni rad upaljača, provodi se pomoću elektromagnetskog ventila koji radi iz termoelementa. Blokiranje dovoda plina u glavni plamenik, ovisno o prisutnosti unosa vode, provodi se pomoću ventila koji se pokreće kroz vreteno iz membrane blok ventila za vodu.
Prirodni plin danas je najrasprostranjenije gorivo. Prirodni plin se naziva prirodnim plinom jer se vadi iz same utrobe Zemlje.
Proces izgaranja plina je kemijska reakcija u kojoj prirodni plin stupa u interakciju s kisikom sadržanim u zraku.
U plinovitom gorivu postoji gorivi i negorivi dio.
Glavna zapaljiva komponenta prirodnog plina je metan - CH4. Njegov sadržaj u prirodnom plinu doseže 98%. Metan je bez mirisa, okusa i nije otrovan. Granica zapaljivosti mu je od 5 do 15%. Upravo su te kvalitete omogućile korištenje prirodnog plina kao jedne od glavnih vrsta goriva. Koncentracija metana je više od 10% opasna po život, pa zbog nedostatka kisika može doći do gušenja.
Da bi se otkrilo curenje plina, plin se podvrgava odorizaciji, drugim riječima, dodaje se tvar jakog mirisa (etil merkaptan). U tom slučaju plin se može detektirati već u koncentraciji od 1%.
Osim metana, u prirodnom plinu mogu biti prisutni zapaljivi plinovi poput propana, butana i etana.
Za kvalitetno izgaranje plina potrebno je u zonu izgaranja unijeti dovoljno zraka i postići dobro miješanje plina sa zrakom. Optimalnim se smatra omjer 1: 10. To jest, deset dijelova zraka pada na jedan dio plina. Osim toga, potrebno je stvoriti željeni temperaturni režim. Da bi se plin zapalio, mora se zagrijati na temperaturu paljenja i ubuduće temperatura ne smije pasti ispod temperature paljenja.
Potrebno je organizirati uklanjanje produkata izgaranja u atmosferu.
Potpuno izgaranje je postignuto ako u produktima izgaranja koji se ispuštaju u atmosferu nema zapaljivih tvari. U tom se slučaju ugljik i vodik spajaju i tvore ugljični dioksid i vodenu paru.
Vizualno, s potpunim izgaranjem, plamen je svijetloplav ili plavkasto-ljubičast.
Potpuno izgaranje plina.
metan + kisik = ugljikov dioksid + voda
CH 4 + 2O 2 \u003d CO 2 + 2H 2 O
Osim ovih plinova, dušik i preostali kisik ulaze u atmosferu sa zapaljivim plinovima. N 2 + O 2
Ako izgaranje plina nije potpuno, tada se u atmosferu ispuštaju zapaljive tvari - ugljični monoksid, vodik, čađa.
Do nepotpunog izgaranja plina dolazi zbog nedovoljne količine zraka. Istodobno se u plamenu vizualno pojavljuju jezici čađe.
Opasnost od nepotpunog izgaranja plina je u tome što ugljični monoksid može izazvati trovanje osoblja u kotlovnici. Sadržaj CO u zraku 0,01-0,02% može uzrokovati lakše trovanje. Veće koncentracije mogu dovesti do teškog trovanja i smrti.
Nastala čađa taloži se na zidovima kotlova, čime se pogoršava prijenos topline na rashladnu tekućinu, što smanjuje učinkovitost kotlovnice. Čađa provodi toplinu 200 puta lošije od metana.
Teoretski, za sagorijevanje 1 m3 plina potrebno je 9 m3 zraka. U stvarnim uvjetima potrebno je više zraka.
Odnosno, potrebna je višak zraka. Ova vrijednost, označena kao alfa, pokazuje koliko je puta više zraka potrošeno nego što je teoretski potrebno.
Alfa koeficijent ovisi o vrsti određenog plamenika i obično je propisan u putovnici plamenika ili u skladu s preporukama organizacije za puštanje u rad.
Povećanjem količine viška zraka iznad preporučene povećavaju se gubici topline. Uz značajno povećanje količine zraka, može doći do odvajanja plamena, stvarajući hitan slučaj. Ako je količina zraka manja od preporučene, tada će izgaranje biti nepotpuno, čime se stvara opasnost od trovanja osoblja u kotlovnici.
Za točniju kontrolu kvalitete izgaranja goriva postoje uređaji - analizatori plina koji mjere sadržaj određenih tvari u sastavu ispušnih plinova.
Analizatori plina mogu se isporučiti s kotlovima. Ako nisu dostupni, odgovarajuća mjerenja provodi organizacija za puštanje u rad pomoću prijenosnih analizatora plina. Sastavlja se karta režima u kojoj su propisani potrebni parametri upravljanja. Pridržavajući se njih, možete osigurati normalno potpuno izgaranje goriva.
Glavni parametri za kontrolu izgaranja goriva su:
- omjer plina i zraka koji se dovodi u plamenike.
- omjer viška zraka.
- pukotina u peći.
- Faktor učinkovitosti kotla.
Ujedno, učinkovitost kotla podrazumijeva odnos korisne topline prema vrijednosti ukupno utrošene topline.
Sastav zraka
| Naziv plina | Kemijski element | Sadržaj u zraku |
| Dušik | N2 | 78 % |
| Kisik | O2 | 21 % |
| Argon | Ar | 1 % |
| Ugljični dioksid | CO2 | 0.03 % |
| Helij | On | manje od 0,001% |
| Vodik | H2 | manje od 0,001% |
| Neon | ne | manje od 0,001% |
| Metan | CH4 | manje od 0,001% |
| Kripton | kr | manje od 0,001% |
| Ksenon | Xe | manje od 0,001% |
Izgaranje plinovitog goriva kombinacija je sljedećih fizikalno-kemijskih procesa: miješanje zapaljivog plina sa zrakom, zagrijavanje smjese, toplinska razgradnja zapaljivih komponenti, paljenje i kemijsko spajanje zapaljivih elemenata s atmosferskim kisikom.
Stabilno izgaranje mješavine plina i zraka moguće je kontinuiranim dovodom potrebnih količina zapaljivog plina i zraka na frontu izgaranja, njihovim temeljitim miješanjem i zagrijavanjem do temperature paljenja ili samozapaljenja (tablica 5).
Paljenje smjese plina i zraka može se izvesti:
- zagrijavanje cjelokupnog volumena smjese plina i zraka do temperature samozapaljenja. Ova se metoda koristi u motorima s unutarnjim izgaranjem, gdje se smjesa plina i zraka zagrijava brzom kompresijom do određenog tlaka;
- korištenje stranih izvora paljenja (upaljači i sl.). U tom se slučaju ne zagrijava cijela smjesa plina i zraka do temperature paljenja, već dio nje. Ova metoda se koristi kod izgaranja plinova u plamenicima plinskih uređaja;
- postojeći plamenik kontinuirano u procesu izgaranja.
Za početak reakcije izgaranja plinovitog goriva potrebno je utrošiti određenu količinu energije potrebnu za kidanje molekularnih veza i stvaranje novih.
Kemijska formula za izgaranje plinskog goriva, koja ukazuje na cijeli mehanizam reakcije povezan s pojavom i nestankom velikog broja slobodnih atoma, radikala i drugih aktivnih čestica, složena je. Stoga se radi pojednostavljenja koriste jednadžbe koje izražavaju početna i završna stanja reakcija izgaranja plinova.
Ako ugljikovodične plinove označimo s C m H n, tada će jednadžba kemijske reakcije izgaranja tih plinova u kisiku imati oblik
C m H n + (m + n/4) O 2 = mCO 2 + (n/2) H 2 O,
gdje je m broj ugljikovih atoma u plinu ugljikovodika; n je broj atoma vodika u plinu; (m + n/4) - količina kisika potrebna za potpuno izgaranje plina.
U skladu s formulom izvode se jednadžbe za izgaranje plinova:
- metan CH 4 + 2O 2 \u003d CO 2 + 2H 2 O
- etan C 2 H 6 + 3,5 O 2 \u003d 2CO 2 + ZH 2 O
- butan C 4 H 10 + 6,5 O 2 \u003d 4CO 2 + 5H 2 0
- propan C3H8 + 5O3 \u003d ZSO2 + 4H2O.
U praktičnim uvjetima izgaranja plina kisik se ne uzima u čistom obliku, već je dio zraka. Budući da se zrak sastoji od 79% dušika i 21% kisika po volumenu, za svaki volumen kisika potrebno je 100:21 = 4,76 volumena zraka ili 79:21 = 3,76 volumena dušika. Tada se reakcija izgaranja metana u zraku može napisati na sljedeći način:
CH 4 + 2O 2 + 2 * 3,76 N 2 \u003d CO 2 + 2H 2 O + 7,52 N 2.
Jednadžba pokazuje da je za izgaranje 1 m 3 metana potrebno 1 m 3 kisika i 7,52 m 3 dušika ili 2 + 7,52 = 9,52 m 3 zraka.
Kao rezultat izgaranja 1 m 3 metana dobiva se 1 m 3 ugljičnog dioksida, 2 m 3 vodene pare i 7,52 m 3 dušika. Donja tablica prikazuje ove podatke za najčešće zapaljive plinove.
Za proces izgaranja plinsko-zračne smjese potrebno je da količina plina i zraka u plinsko-zračnoj smjesi bude u određenim granicama. Te se granice nazivaju granicama zapaljivosti ili granicama eksplozivnosti. Postoje donja i gornja granica zapaljivosti. Minimalni sadržaj plina u smjesi plin-zrak, izražen kao postotak po volumenu, pri kojem dolazi do paljenja, naziva se donja granica zapaljivosti. Maksimalni sadržaj plina u smjesi plin-zrak, iznad kojeg se smjesa ne zapali bez dodatnog dovođenja topline, naziva se gornja granica zapaljivosti.
Količina kisika i zraka pri izgaranju pojedinih plinova
|
Za sagorijevanje 1 m 3 plina potrebno je m 3 |
Pri izgaranju 1 m 3 oslobađa se plin, m 3 |
Toplina izgaranja He, kJ / m 3 |
|||||
|
kisik |
dioksid ugljik |
||||||
|
ugljični monoksid |
|||||||
Ako mješavina plina i zraka sadrži plin manje od donje granice zapaljivosti, tada neće gorjeti. Ako u smjesi plina i zraka nema dovoljno zraka, izgaranje se ne odvija u potpunosti.
Inertne nečistoće u plinovima imaju velik utjecaj na veličinu granica eksplozivnosti. Povećanje udjela balasta (N 2 i CO 2 ) u plinu sužava granice zapaljivosti, a kada udio balasta naraste iznad određenih granica, smjesa plina i zraka se ne zapali ni pri jednom omjeru plina i zraka (tablica dolje) .
Broj volumena inertnog plina po 1 volumenu zapaljivog plina pri kojem smjesa plina i zraka prestaje biti eksplozivna
Najmanja količina zraka potrebna za potpuno izgaranje plina naziva se teoretski protok zraka i označava se s Lt, odnosno ako je donja ogrjevna vrijednost plinovitog goriva 33520 kJ/m 3 , zatim teoretski potrebna količina zraka za spaljivanje 1 m 3 plina
L T\u003d (33 520/4190) / 1,1 \u003d 8,8 m 3.
Međutim, stvarni protok zraka uvijek premašuje teoretski. To se objašnjava činjenicom da je vrlo teško postići potpuno izgaranje plina pri teoretskim brzinama protoka zraka. Stoga svako postrojenje za izgaranje plina radi s nešto viška zraka.
Dakle, praktičan protok zraka
L n = αL T,
gdje L n- praktična potrošnja zraka; α - koeficijent viška zraka; L T- teorijska potrošnja zraka.
Koeficijent viška zraka uvijek je veći od jedan. Za prirodni plin jest α = 1,05 - 1,2. Koeficijent α pokazuje koliko puta stvarni protok zraka premašuje teoretski, uzeto kao jedinica. Ako a α = 1, tada se naziva smjesa plin-zrak stehiometrijski.
Na α = 1,2 izgaranje plina provodi se s viškom zraka od 20%. U pravilu se izgaranje plinova treba odvijati uz minimalnu vrijednost a, jer se smanjenjem viška zraka smanjuju gubici topline s ispušnim plinovima. Zrak koji sudjeluje u izgaranju je primarni i sekundarni. Primarni zove se zrak koji ulazi u plamenik za miješanje s plinom u njemu; sekundarni- zrak koji ulazi u zonu izgaranja nije pomiješan s plinom, već odvojeno.






