विमानन में श्रम संरक्षण। स्व-जलने के सिद्धांत के तत्व। स्व-हीटिंग तापमान। स्व-इग्निशन और इग्निशन से स्व-जलने का अंतर - आग बुझाने की रचनाएं
थर्मल सिद्धांत के अनुसार, आत्म-इग्निशन के तापमान के तहत, वे पदार्थ (सामग्री, मिश्रण) के सबसे कम तापमान को समझते हैं, जिस पर अव्यवस्थित प्रतिक्रियाओं की गति में तेज वृद्धि होती है, जो लौ जलने की उपस्थिति के साथ समाप्त होती है। अंजीर में। 2.3 ऐसा तापमान तापमान है टी एस।बिंदु के अनुरूप मेंजिसमें गर्मी सिंक लाइन प्र 2 गर्मी उत्पादन लाइन के बारे में।
तापमान माप टी एस। यह लगभग बहुत मुश्किल है, मिश्रण के तापमान में परिवर्तन की बड़ी गति के कारण जब यह स्व-चरण होता है। इसलिए, आत्म-इग्निशन के तापमान के लिए, पोत की दीवार का सबसे छोटा तापमान लिया जाता है या व्यापकजिसमें इन स्थितियों में पदार्थ की आत्म-इग्निशन है, यानी टी 0।। यह बहुत बड़ी गलतियों को शामिल नहीं करता है।
दहन में तापमान की स्थापना के बाद से समय टी 0। जब तक तापमान तक नहीं पहुंच जाता टी एस। बुला हुआ प्रवेशन अवधि या स्व-इग्निशन देरी का समय। नियोडनेक्स के एक ही पदार्थ के लिए प्रेरण की अवधि और दृढ़ता से दहनशील मिश्रण, तापमान और दबाव की संरचना पर निर्भर करता है। आत्म-इग्निशन के दौरान दहनशील पदार्थ के हीटिंग तापमान को कम करने के लिए, प्रेरण अवधि जितनी अधिक होगी। द्वारा
यह अक्सर आत्म-इग्निशन के तापमान के कारण होता है, पर्यावरण या पोत की दीवारों का तापमान लिया जाता है, जिसमें प्रेरण अवधि सबसे बड़ी होती है।
निम्नलिखित पोत की संरचना और तापमान के आधार पर हवा के साथ मीथेन मिश्रणों की प्रेरण की अवधि में बदलाव दिखाया गया है:
|
के साथ प्रेरण अवधि |
|||
|
775 0 पर .............................................. ....... |
|||
|
825 0 पर .............................................. ..... |
|||
|
875 0 पर .............................................. ..... |
|||
आत्म-इग्निशन के तापमान को निर्धारित करते समय, प्रेरण की अवधि को मापना असंभव है, इसलिए प्रेरण अवधि के दौरान जब तक कि लौ प्रकट होने तक पदार्थ के हीटिंग के क्षण से समय लगता है। प्रेरण अवधि कम-शक्ति सूजन स्रोतों (स्पार्क्स) के ईंधन पर कार्रवाई में व्यावहारिक महत्व की है। वायु के साथ वाष्प या गैसों के एक दहनशील मिश्रण में घूमते समय, मिश्रण की कुछ मात्रा गर्म हो जाती है और साथ ही स्पार्क ठंडा हो जाता है। इस मामले में मिश्रण की इग्निशन मिश्रण की प्रेरण अवधि और स्पार्क के शीतलन समय के अनुपात पर निर्भर करता है। यदि प्रेरण अवधि स्पार्क के शीतलन समय से अधिक तापमान तक होती है, जो स्वयं-इग्निशन तापमान से कम है, तो मिश्रण की इग्निशन नहीं होती है। यदि प्रेरण की अवधि शीतलन समय स्पार्क से कम है, तो मिश्रण ज्वलनशील है। इस प्रकार, कम शक्ति की चमक मिश्रण की एक छोटी अवधि के साथ मिश्रण को अनदेखा कर सकती है और मिश्रण की बड़ी अवधि के साथ मिश्रण को प्रज्वलित नहीं कर सकती है।
प्रवेशन अवधि ठोस यह गैस और धूल मिश्रण की अवधि से अलग है। यदि प्रेरण अवधि के लिए गैस मिश्रित यह दसियों और सैकड़ों सेकंड है, ठोस दहनशील पदार्थों के लिए प्रेरण की अवधि घड़ियों, दिन और महीने हो सकती है। स्व-इग्निशन पदार्थ के तापमान पर, जलती हुई अभी तक नहीं होती है। यह दहन तापमान (लौ) में होता है और विकसित होता है, जो स्व-इग्निशन के तापमान से काफी अधिक है। उदाहरण के लिए, गैसोलीन 260 0 सी का स्व-इग्निशन तापमान, और इसकी लौ तापमान 1200 - 1300 0 सी है। तापमान में वृद्धि 260 से 1200 0 सी तक बढ़ोतरी गैसोलीन के मिश्रण के स्व-हीटिंग का परिणाम है हवा के साथ वाष्प।
दहनशील पदार्थ की आत्म-इग्निशन का तापमान निरंतर मूल्य नहीं है। आत्म-इग्निशन के थर्मल सिद्धांत के अनुसार, यह तापमान गर्मी उत्पादन दर और गर्मी सिंक वेग पर निर्भर करता है, जो बदले में, दहनशील पदार्थ, इसकी एकाग्रता, दबाव और अन्य कारकों की मात्रा पर निर्भर करता है।
आत्म-इग्निशन के तापमान को निर्धारित करने के लिए प्रयोगों में, यह स्थापित किया गया था कि यह न केवल दहनशील पदार्थ की मात्रा में बदलाव के साथ बदलता है, बल्कि पोत (कंटेनर) के रूप में भी बदलता है, जिसमें पदार्थ स्थित होता है। यह बताता है कि पोत के आकार या आकार में बदलाव के साथ, विशिष्ट गर्मी सिंक सतह भिन्न होती है एस/ वी। उसी जहाज में, यह पोत की मात्रा से छोटा है। इसलिए, पोत की मात्रा में वृद्धि के साथ, गर्मी की सिंक की गति कम हो जाती है और इसके अनुसार, आत्म-इग्निशन का तापमान कम किया जाना चाहिए। विभिन्न खंडों के जहाजों में तरल पदार्थ के वाष्पों की आत्म-इग्निशन के निम्नलिखित तापमान इस धारणा की पुष्टि करते हैं:
|
पोत की मात्रा, एल .................. .. |
||||||||
|
स्व-स्पलैश तापमान |
||||||||
|
एसीटोन ........................... |
||||||||
|
बेंजीन ........................... |
||||||||
|
गैसोलीन ............................. |
||||||||
|
डायइथाइल इथर ............ .. |
||||||||
|
मिटटी तेल ........................ |
||||||||
|
मिथाइल अल्कोहल ............ .. |
||||||||
|
seroublerod .................. .. |
||||||||
|
टोलले ........................... |
||||||||
वॉल्यूम में वृद्धि के साथ स्व-इग्निशन तापमान तब तक घटता है जब तक कि वॉल्यूम एक निश्चित मूल्य तक नहीं पहुंच जाता है (पोत का आकार नहीं बदलता है); वॉल्यूम में और वृद्धि के साथ, आत्म-इग्निशन का तापमान स्थिर रहता है।
इस प्रकार, प्रयोग से पता चलता है कि 12 लीटर से अधिक की मात्रा में, दहनशील मिश्रण की आत्म-इग्निशन का तापमान थोड़ा भिन्न होता है। यह इस तथ्य से समझाया गया है कि बड़ी मात्रा में, दहनशील मिश्रण एक ही समय में वॉल्यूम पर स्वयं प्रस्ताव नहीं है, लेकिन इसके कुछ हिस्सों में, जिसमें सबसे अधिक है इष्टतम स्थितियां। इसलिए, एक छोटे दहन पदार्थ में, बाहरी सतहों के माध्यम से गर्मी सिंक में परिवर्तन आत्म-इग्निशन के तापमान में परिवर्तन को प्रभावित करता है, और बड़ी मात्रा में - नहीं।
मात्रा में कमी के साथ एक दहनशील पदार्थ की आत्म-इग्निशन के तापमान को बढ़ाना भी अनंत नहीं है। बहुत छोटी मात्रा के साथ, गर्मी सिंक का विशिष्ट सतह क्षेत्र इतना बड़ा हो जाता है कि दहनशील मिश्रण के ऑक्सीकरण के कारण गर्मी रिलीज दर, यहां तक \u200b\u200bकि बहुत अधिक तापमान पर, गर्मी सिंक की गति से अधिक नहीं हो सकती है, और आत्म-इग्निशन नहीं होता है। इस सिद्धांत में, गैस मिश्रण (फायरप्रोसेवर) के दहन के प्रचार को रोकने के लिए कई उपकरणों को डिजाइन और संचालित किया जाता है।
सबसे सरल फायरप्रोसेसर एक सुरक्षात्मक ग्रिड एक दहनशील गैस मिश्रण में रखा गया है जो एक ग्रिड द्वारा मामूली मात्रा में टूटा हुआ है। इस मामले में, आत्म-इग्निशन नहीं हो सकता है। सुरक्षात्मक जाल का उपयोग खनन दीपक, साथ ही छोटे व्यास पाइपलाइनों में भी किया जाता है, जिसके अनुसार पेट्रोलियम उत्पादों के जोड़े के साथ हवा का मिश्रण परिवहन किया जाता है। सुरक्षात्मक जाल का उपयोग हाइड्रोजन, एसिटिलीन, स्टीमिंग भाप, शराब, ईथर और अन्य पदार्थों के साथ हवा के मिश्रण के लिए नहीं किया जा सकता है जिनके पास या तो स्व-इग्निशन का निम्न तापमान, या दहन की उच्च गर्मी है। ऐसी स्थितियों में, जलती हुई ग्रिड के माध्यम से पारित होने के दौरान जलती हुई मिश्रण आत्म-इग्निशन के तापमान से नीचे ठंडा नहीं होता है और ग्रिड के पीछे जलना जारी रहता है।
गर्मी सिंक के अधिक विशिष्ट सतह क्षेत्र को न केवल पोत की मात्रा में कमी के परिणामस्वरूप, बल्कि इसे संबंधित रूप देकर भी प्राप्त किया जा सकता है। अंजीर में। 2.4 चित्रित जहाजों विभिन्न आकारों काजो दहनशील मिश्रण की समान मात्रा को समायोजित करता है।
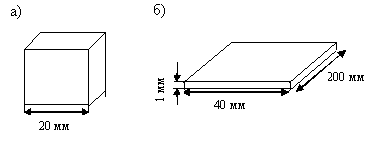
अंजीर। 2.4। गर्मी सिंक की विभिन्न गति पर एक ही कंटेनर के वेसल
पहले पोत (घन) में (अंजीर 2.4, लेकिन अ) गर्म होने पर, मिश्रण की एक आत्म-इग्निशन होता है, दूसरे में पतली स्लॉट (चित्र 2.4) का प्रतिनिधित्व करता है बी), मिश्रण आत्म-प्रस्ताव नहीं है। यह इस तथ्य से समझाया गया है कि दूसरे जहाज में पहली बार गर्मी सिंक की बड़ी सतह है।
\u003e स्वयं जलने के सिद्धांत के तत्व। स्व-हीटिंग तापमान। आत्म-इग्निशन और इग्निशन से स्व-जलने के बीच का अंतर
उचित संगठन अग्निशमन घटनाक्रम और जलने के दौरान होने वाली रासायनिक और भौतिक प्रक्रियाओं के सार को समझने के बिना कोई बुझाने वाली आग नहीं होती है। इन प्रक्रियाओं को जानना सफलतापूर्वक आग से निपटने के लिए संभव बनाता है।
दहन- यह एक रासायनिक ऑक्सीकरण प्रतिक्रिया है, जिसमें बड़ी मात्रा में गर्मी और आमतौर पर एक चमक के साथ रिलीज के साथ। दहन की प्रक्रिया में ऑक्सीडाइज़र ऑक्सीजन हो सकता है, साथ ही क्लोरीन, ब्रोमाइन और अन्य पदार्थ भी हो सकते हैं।
ज्यादातर मामलों में, आग के मामले में, दहनशील पदार्थों का ऑक्सीकरण हवा से ऑक्सीजन होता है। दहन संभव है यदि जलने में सक्षम पदार्थ है, ऑक्सीजन (वायु) और इग्निशन स्रोत। यह आवश्यक है कि एक क्रोध पदार्थ और ऑक्सीजन कुछ मात्रात्मक संबंधों में हैं, और इग्निशन के स्रोत में थर्मल ऊर्जा की आवश्यक आपूर्ति थी।
यह ज्ञात है कि हवा में लगभग 21% ऑक्सीजन होता है। अधिकांश पदार्थों की जलन असंभव हो जाती है जब हवा में ऑक्सीजन सामग्री 14-18% हो जाती है, और केवल कुछ दहनशील पदार्थ (हाइड्रोजन, ईथिलीन, एसिटिलीन इत्यादि) को जलाया जा सकता है जब ऑक्सीजन सामग्री 10% तक हवा में होती है और कम से। ऑक्सीजन सामग्री में और कमी के साथ, अधिकांश पदार्थों को जलाना बंद कर दिया जाता है।
ईंधन और ऑक्सीजन पदार्थ प्रतिक्रिया दे रहे हैं और ईंधन प्रणाली बनाते हैं, और इग्निशन स्रोत दहन प्रतिक्रिया का कारण बनता है। इग्निशन का स्रोत लुढ़का हुआ शरीर के जलते हुए पीपी हो सकता है, साथ ही एक विद्युत निर्वहन होता है जिसमें जलन और अन्य स्व-जलती इग्निशन आग बुझाने के लिए पर्याप्त ऊर्जा आरक्षित होती है
दहनशील प्रणालियों को सजातीय और अमानवीय में बांटा गया है। वर्दी वे सिस्टम हैं जिनमें ईंधन और हवा समान रूप से एक दूसरे के साथ मिश्रित होते हैं (दहनशील गैसों के मिश्रण, हवा के साथ भाप)। ऐसे प्रणालियों का दहन कहा जाता है जलती गतिशील। गति गति से निर्धारित होती है रासायनिक प्रतिक्रियामहत्वपूर्ण उच्च तापमान। कुछ स्थितियों के तहत, इस तरह का दहन विस्फोट या विस्फोट की प्रकृति हो सकती है। असामान्य प्रणाली जिसमें एक ईंधन और हवा एक-दूसरे के साथ मिश्रित नहीं होती है और इसमें अनुभाग की सतह होती है (ठोस दहनशील सामग्री और अस्पष्ट तरल पदार्थ)। अमानवीय दहनशील प्रणालियों के दहन की प्रक्रिया में, वायु ऑक्सीजन को दहन उत्पादों के माध्यम से ईंधन में घुसपैठ (फैलाव) में प्रवेश करता है और इसके साथ प्रतिक्रिया में प्रवेश करता है। इस तरह की जलन कहा जाता है प्रसार जल रहा है,चूंकि इसकी गति मुख्य रूप से अपेक्षाकृत धीरे-धीरे बहती प्रक्रिया-प्रसार निर्धारित करती है।
आग लगाने के लिए, इग्निशन के स्रोत की गर्मी दहनशील पदार्थों को जोड़े और गैसों में परिवर्तित करने और उन्हें आत्म-इग्निशन के तापमान पर गर्म करने के लिए पर्याप्त होनी चाहिए। ईंधन और ऑक्सीडेंट के अनुपात से, गरीब और समृद्ध दहनशील मिश्रणों के दहन की प्रक्रियाओं को प्रतिष्ठित किया जाता है। गरीब मिश्रणों में अधिक ऑक्सीकरण एजेंट होता है और ईंधन घटक की कमी होती है। रिच मिक्स, इसके विपरीत, अतिरिक्त और ऑक्सीकरण एजेंट के नुकसान में एक ज्वलनशील घटक होता है।
दहन की घटना प्रणाली में प्रतिक्रिया के अनिवार्य आत्मविश्वास से जुड़ी है। जलने के लिए अपने संक्रमण के साथ आत्मनिर्भर प्रतिक्रिया की प्रक्रिया को आत्म-इग्निशन कहा जाता है। दहन पर एक रासायनिक प्रतिक्रिया का स्वयं-सिफ्टिंग तीन मुख्य प्रकारों में विभाजित है: गर्मी, श्रृंखला और संयुक्त - श्रृंखला-थर्मल। गर्मी सिद्धांत द्वारा, रासायनिक प्रतिक्रिया की गति में वृद्धि के साथ ऑक्सीकरण प्रक्रिया के सक्रियण द्वारा स्वयं-इग्निशन की प्रक्रिया को समझाया जाता है। श्रृंखला सिद्धांत द्वारा, आत्म-इग्निशन की प्रक्रिया रासायनिक प्रतिक्रिया की श्रृंखला की शाखाओं के कारण होती है। व्यावहारिक रूप से दहन प्रक्रिया मुख्य रूप से संयुक्त श्रृंखला-थर्मल तंत्र द्वारा की जाती है।
दहन पूर्ण और अधूरा अंतर करता है। पूर्ण दहन के साथ, उत्पादों का गठन किया जाता है जो अधिक जलाने में असमर्थ हैं: कार्बन डाइऑक्साइड, सल्फर गैस, पानी जोड़े। अपूर्ण दहन तब होता है जब ऑक्सीजन की पहुंच जलती हुई ज़ोन के लिए मुश्किल होती है, नतीजतन, अपूर्ण दहन उत्पाद बनते हैं: कार्बन मोनोऑक्साइड, अल्कोहल, एल्डेहाइड इत्यादि बनते हैं।
लगभग हवा की मात्रा (एम 3), जो कि 1 किलो पदार्थ के दहन (या गैस के 1 एम 3) के दहन के लिए आवश्यक है,
कुछ पदार्थों की गर्मी दहन: गैसोलीन -47 000 केजे / किग्रा; एयर-ड्राई -14 600 केजे / किग्रा की वुड्स; एसिटिलीन - 54400 केजे / एम 3; मीथेन - 3 9 400 केजे / एम 3; कार्बन ऑक्साइड - 12600 केजे / एम 3।
दहनशील पदार्थ के दहन की गर्मी पर, यह निर्धारित करना संभव है कि अपने दहन, दहन तापमान, बंद वॉल्यूम और अन्य डेटा में विस्फोट के दौरान दबाव के दौरान कितना गर्मी जारी की जाती है।
पदार्थ के दहन तापमान को सैद्धांतिक और मान्य दोनों को परिभाषित किया गया है। सैद्धांतिक दहन तापमान है, जिस पर दहन उत्पादों को गरम किया जाता है, एक धारणा के रूप में कि जलन के दौरान प्रतिष्ठित सभी गर्मी गर्म हो जाती है।
वास्तविक दहन तापमान 30-50% कम सैद्धांतिक है, क्योंकि जलने के दौरान जारी गर्मी का एक महत्वपूर्ण हिस्सा पर्यावरण में विलुप्त हो जाता है।
उच्च दहन तापमान आग के फैलाव में योगदान देता है, इसके साथ एक बड़ी संख्या की गर्मी पर्यावरण के लिए उत्सर्जित होती है, और जलने के लिए दहनशील पदार्थों की गहन तैयारी होती है। उच्च दहन तापमान पर आग बुझाने में बाधा है।
दहन प्रक्रियाओं पर विचार करते समय, निम्नलिखित प्रकारों को प्रतिष्ठित किया जाना चाहिए: एक फ्लैश, आग, इग्निशन, आत्म-इग्निशन, स्वयं जलने, विस्फोट।
Chamak- यह एक दहनशील मिश्रण का एक तेज़ दहन है, संपीड़ित गैसों के गठन के साथ नहीं।
इग्निशन- इग्निशन स्रोत के प्रभाव में दहन की घटना।
इग्निशन- इग्निशन, लौ की उपस्थिति के साथ।
अज्ञान- इग्निशन स्रोत के प्रभाव में प्रज्वलित करने की क्षमता (प्रज्वलित)।
स्वयमेव जल उठना- यह एक्सोथर्मिक प्रतिक्रियाओं की गति में तेज वृद्धि की घटना है, जिससे इग्निशन स्रोत की अनुपस्थिति में पदार्थों (सामग्री, मिश्रण) की उत्पीड़न की घटना होती है।
आत्मनिर्भरता- यह ज्वाला की उपस्थिति के साथ एक आत्म-जलन है।
विस्फोटइसे ऊर्जा की रिहाई और यांत्रिक कार्य के उत्पादन के लिए सक्षम संपीड़ित गैसों के गठन के साथ एक पदार्थ के बेहद तेज़ रासायनिक (विस्फोटक) रूपांतरण कहा जाता है।
इग्निशन (इग्निशन) और स्व-जलने (आत्म-इग्निशन) की प्रक्रियाओं के बीच अंतर को समझना आवश्यक है। खुद को सूजन करने के लिए, एक दहनशील तंत्र में थर्मल पल्स बनाना आवश्यक है जिसमें पदार्थ के आत्म-इग्निशन तापमान से अधिक तापमान होता है। आत्म-इग्निशन के तापमान से नीचे तापमान पर जलने की घटना स्व-जलने (आत्म-इग्निशन) की प्रक्रिया को संदर्भित करती है।
दहन एक इग्निशन स्रोत के बिना होता है - थर्मल या माइक्रोबायोलॉजिकल स्व-जलने के कारण।
गर्मी स्व-जलती हुईएक छिपे हुए या बाहरी हीटिंग स्रोत के प्रभाव में स्व-हीटिंग के परिणामस्वरूप पदार्थ होते हैं। आत्म-इग्निशन केवल तभी संभव है जब आत्म-परीक्षा के दौरान उत्पन्न गर्मी की मात्रा पर्यावरण में गर्मी की वापसी से अधिक हो जाएगी।
माइक्रोबायोलॉजिकल स्व जलन यह पदार्थ (सामग्री, मिश्रण) के द्रव्यमान में सूक्ष्मजीवों की आजीविका के प्रभाव के तहत स्व-हीटिंग के परिणामस्वरूप होता है। आत्म-इग्निशन का तापमान दहनशील पदार्थ की एक महत्वपूर्ण विशेषता है।
स्व-इग्निन तापमान - यह सर्वाधिक है कम तापमान ऐसे पदार्थ जिनमें एक्सोथर्मिक प्रतिक्रियाओं की गति में तेज वृद्धि होती है, जो आग जलने के उद्भव के साथ समाप्त होती है।
मशीन-निर्माण उद्योग में उपयोग किए जाने वाले कुछ तरल पदार्थ, गैसों और ठोस पदार्थों के स्व-इग्निशन तापमान तालिका में दिखाए जाते हैं। एक।
तालिका एक कुछ तरल पदार्थों के स्व-इग्निशन तापमान
आत्म-इग्निशन के तापमान के अलावा, दहनशील पदार्थों को आत्म-इग्निशन के प्रेरण या मंदता समय की अवधि की विशेषता है। प्रेरण की अवधि को समय की अवधि कहा जाता है जिसके दौरान इग्निशन के लिए स्व-हीटिंग। असमान के एक ही दहनशील पदार्थ के लिए प्रेरण की अवधि और मिश्रण, प्रारंभिक तापमान और दबाव की संरचना के आधार पर है।
प्रेरण अवधि कम-शक्ति सूजन स्रोतों (स्पार्क्स) के ईंधन पर कार्रवाई में व्यावहारिक महत्व की है। स्पार्क, वायु के साथ वाष्प या गैसों के ईंधन मिश्रण में शामिल होना, मिश्रण की कुछ मात्रा को गर्म करता है, और साथ ही स्पार्क ठंडा हो रहा है। मिश्रण की इग्निशन मिश्रण की प्रेरण अवधि और स्पार्क के शीतलन समय के अनुपात पर निर्भर करता है। साथ ही, यदि प्रेरण अवधि स्पार्क के शीतलन समय से अधिक है, तो मिश्रण की इग्निशन नहीं होगी।
प्रेरण अवधि इग्निशन के संबंध में खतरे की डिग्री के अनुसार गैस मिश्रणों के वर्गीकरण पर आधारित है। धूल मिश्रणों की प्रेरण की अवधि धूल के आकार, अस्थिर पदार्थों की संख्या, आर्द्रता और अन्य कारकों पर निर्भर करती है।
कुछ पदार्थ सामान्य तापमान पर होने के नाते आत्म-बारी हो सकते हैं। यह मुख्य रूप से ठोस छिद्रपूर्ण पदार्थ ज्यादातर कार्बनिक मूल (भूसा, पीट, जीवाश्म कोयला, आदि) है। एक बड़ी सतह पर एक पतली परत द्वारा वितरित स्व-जलने और तेलों के लिए प्रवण। यह धोए गए वीटो के स्वयं जलने की संभावना का कारण बनता है। धोया रेशेदार सामग्रियों के स्व-जलने का कारण उन सतहों पर एक पतली परत और हवा से ऑक्सीजन के अवशोषण के साथ फैटी पदार्थों का वितरण है। तेल ऑक्सीजन का ऑक्सीकरण गर्मी रिलीज के साथ होता है। ऐसे मामले में जहां गर्मी की मात्रा पर्यावरण में गर्मी की कमी से अधिक हो जाती है, आग का उदय हो सकता है।
स्व-जलने के लिए प्रवण पदार्थों का अग्नि खतरा बहुत अधिक है, क्योंकि वे पदार्थों के आत्म-इग्निशन तापमान के नीचे परिवेश के तापमान पर किसी भी गर्मी की आपूर्ति के बिना प्रकाश डाल सकते हैं, और स्वयं-बोले गए पदार्थों की प्रेरण की अवधि कई घंटे हो सकती है, दिन और यहां तक \u200b\u200bकि महीने। ऑक्सीकरण (पदार्थ की सुनवाई) को तेज करने की प्रक्रिया केवल तब बंद की जा सकती है जब तापमान में खतरनाक वृद्धि का पता चला है, जो इंगित करता है बहुत महत्व आग और निवारक उपाय।
मशीन निर्माण उद्यमों पर स्वयं जलने में सक्षम कई पदार्थों का उपयोग किया जाता है। वायु के साथ बातचीत करते समय आत्म-मोड़ लोहा, सूट, एल्यूमीनियम और जस्ता पाउडर, आदि के सल्फाइड, पानी के साथ बातचीत करते समय आत्म-मोड़ क्षारीय धातु, धातुओं की कार्बाइड, आदि कैल्शियम कार्बाइड (सीएसी 2), पानी के साथ प्रतिक्रिया, एसिटिलीन (सी 2 एन 2) फॉर्म।
जलती को एक एक्सोथर्मिक प्रतिक्रिया कहा जाता है जो इसके प्रगतिशील आत्म-कॉन्फ़िगरेशन में होता है। दहन न केवल हवा ऑक्सीजन के संयोजन के साथ पदार्थों के क्षय की रासायनिक प्रतिक्रिया के परिणामस्वरूप दोनों हो सकता है, बल्कि उन पदार्थों के साथ भी, जिसमें इसे स्वयं में शामिल किया गया है (उदाहरण के लिए, नींबू)। कई पदार्थों का दहन क्लोरीन माध्यम, ब्रोमाइन वाष्प, सल्फर में हो सकता है।
जलने को कई प्रकारों में बांटा गया है: प्रकोप, इग्निशन, सूजन, आत्म-जलन, आत्म-जलन।
फ्लैश का तापमान केंद्रित पदार्थ का सबसे छोटा तापमान है, जिसमें इसकी सतह के ऊपर विशेष परीक्षण की शर्तों के तहत, भाप का गठन किया जाता है, जो इग्निशन स्रोत से हवा में चमकने में सक्षम होता है; सतत जलन नहीं होती है।
सूजन एक दहनशील पदार्थ का तेज़ दहन है जो संपीड़ित गैस के गठन के साथ नहीं है।
ज्वलनशीलता तापमान तरल के नीचे प्रतिनिधित्व नहीं करता है आग का खतरा लौ, स्पार्क या कटा हुआ शरीर की अल्पकालिक कार्रवाई के मामले में। यदि तरल पदार्थ को इग्निशन तापमान और ऊपर के लिए गरम किया जाता है, तो आग की लपटों या स्पार्क की अपनी जोड़ी पर भी अल्पकालिक कार्रवाई अनिवार्य रूप से इसकी इग्निशन का कारण बनती है, और कुछ स्थितियों के तहत आग लग सकती है। इसे ध्यान में रखते हुए, प्रकोप का तापमान डिग्री से तरल पदार्थ के वर्गीकरण के आधार के रूप में लिया जाता है अग्नि सुरक्षा। जलने में सक्षम तरल पदार्थ ज्वलनशील (एलवीजेड) और दहनशील (जीजे) * में विभाजित हैं।
ज्वलनशील पदार्थ जो अक्सर विमानन में पाए जाते हैं, इस तरह के प्रकोप तापमान (डिग्री सेल्सियस में) होते हैं:
* ज्वलनशील तरल पदार्थ में एक खुले क्रूसिबल में निर्धारित करते समय एक बंद क्रूसिबल, या 66 डिग्री सेल्सियस - 61 डिग्री सेल्सियस से अधिक होने वाले प्रकोप के तापमान के साथ ज्वलनशील तरल पदार्थ शामिल हैं। फ्लैश पॉइंट वाला तरल पदार्थ ज्वलनशील के अनुसार निर्दिष्ट सापेक्ष से अधिक है।
भड़कने के तापमान के आधार पर, आपको चुनने की आवश्यकता है सुरक्षित तरीके विभिन्न उद्देश्यों के लिए परिवहन, भंडारण और तरल का उपयोग। प्रकोप के तापमान पर, स्थिर जलने नहीं होते हैं, और केवल तरल के ऊपर बर्न्स तरल के ऊपर वाष्पों के मिश्रण के साथ होते हैं। यदि द्रव तापमान फ्लैश तापमान से कुछ हद तक अधिक है, तो इसके साथ वाष्पीकरण की गति खुली सतह बढ़ी, और मिश्रण के प्रकोप के समय, तरल स्थिर जलने के लिए पर्याप्त मात्रा में लगातार जोड़ी को अलग करने में सक्षम है। इस तरह के तापमान को इग्निशन तापमान कहा जाता है। यह उस पदार्थ का सबसे छोटा तापमान है जिस पर विशेष परीक्षणों की शर्तों के तहत, पदार्थ ईंधन जोड़े और गैसों को इस तरह की गति से हाइलाइट करता है जो ऊर्जा स्रोत के संपर्क में आने पर, वे इग्निशन हैं।
ज्वाला की उपस्थिति के साथ सूजन एक आग है।
ज्वलनशील तरल पदार्थ में, फ्लैशबिलिटी तापमान फ्लैशबिलिटी तापमान 1-5 डिग्री सेल्सियस है, इसके अलावा, द्रव प्रकोप का तापमान कम होता है, यह अंतर कम होता है। तो, बेंजीन, एसीटोन में, शून्य से नीचे एक फ्लैश तापमान होने के कारण, यह अंतर 1 डिग्री सेल्सियस है, दहनशील तरल पदार्थ में - यह अंतर 30 डिग्री सेल्सियस और उच्चतम हो जाता है।
स्वयमेव जल उठना - यह एक्सोथर्मिक वॉल्यूमेट्रिक प्रतिक्रियाओं की गति में तेज वृद्धि है, जिससे तापमान में तेज वृद्धि होती है और इग्निशन स्रोत की अनुपस्थिति में पदार्थों के दहन की घटना होती है।
स्वयं-इग्निशन का थर्मल सिद्धांत पहले एसएन द्वारा विकसित किया गया था। सेमेनोव और आगे डी ए फ्रैंक-कमनेटस्की और ए एन टॉड द्वारा विकसित किया गया।
इस सिद्धांत के मुख्य प्रावधानों को दहनशील वाष्प या हवा के साथ गैस के मिश्रण की आत्म-इग्निशन के उदाहरण पर विचार किया जा सकता है। कम तापमान टी 0 (उदाहरण के लिए, प्लस 20 डिग्री सेल्सियस) पर, मिश्रण में केरोसिन और एयर ऑक्सीजन के बीच प्रतिक्रिया व्यावहारिक रूप से नहीं होती है, क्योंकि कोई सक्रिय ऑक्सीजन अणु नहीं होता है। उनके लिए प्रकट होने के लिए और ऑक्सीकरण प्रतिक्रिया शुरू हुई, मिश्रण को उच्च तापमान टी 1 तक गरम किया जाना चाहिए। इस उद्देश्य के लिए, माध्यम के मिश्रण वाले व्यंजनों को रखा जाता है, तापमान टी 1 (चित्र 15.1, ए) होता है। कुछ समय बाद, इसमें व्यंजन और मिश्रण तापमान टी 1 तक गर्म होते हैं और ऑक्सीकरण की प्रक्रिया गर्मी रिलीज के साथ मिश्रण में होती है। चयनित गर्मी क्यू 1 दहनशील मिश्रण में प्रेषित किया जाता है, तापमान टी 1 तक गर्म होता है। हालांकि, जैसे ही मिश्रण का तापमान व्यंजन और बाहरी वातावरण की दीवारों के तापमान से अधिक हो जाता है, थर्मल-विजुअल मिश्रण व्यंजनों की दीवारों और आगे के लिए शुरू हो जाएगा बाहरी वातावरण। मिश्र धातु गर्मी की मात्रा Q2 द्वारा दर्शाया गया है।

अंजीर। 15.1। दहनशील मिश्रण को स्वयं जलाने की प्रक्रिया की व्याख्या करने वाली योजना:
ए- इसे आपूर्ति की गई थर्मल ऊर्जा के कारण मिश्रण को गर्म करना; बी - थर्मल संतुलन; बी - मिश्रण के स्व-हीटिंग और इसे पर्यावरण में गर्मी की वापसी
मिश्रण का आगे हीटिंग गर्मी उत्पादन और गर्मी सिंक वेग के अनुपात पर निर्भर करेगा। यदि Q1\u003e Q2 तब मिश्रण, ऑक्सीकरण, गर्म हो जाएगा, और यदि q1 \u003d q2, तो मिश्रण किसी के साथ ऑक्सीकरण किया जाएगा स्थिर तापमानजिस पर यह अनुपात उठ गया। मान लीजिए कि मिश्रण के ऑक्सीकरण के कारण गर्मी रिलीज दर गर्मी डूबती दर से अधिक है। हालांकि, यह अभी भी पर्याप्त नहीं है ताकि मिश्रण को गर्म करने के लिए जारी रखा जा सके, क्योंकि दहनशील मिश्रण के तापमान में वृद्धि के साथ, गर्मी और गर्मी सिंक समान रूप से बढ़ी नहीं है। और यदि मिश्रण के बढ़ते तापमान के साथ, गर्मी सिंक की गति गर्मी अपव्यय की तुलना में तेज़ी से बढ़ेगी, फिर मिश्रण के कुछ तापमान पर, वे (91 \u003d 9 2) के बराबर हो जाएंगे और भविष्य में हीटिंग को निलंबित कर दिया जाएगा। यह आमतौर पर एक दहनशील पदार्थ की कम ऑक्सीकरण दर या एक बड़ी गर्मी सिंक के साथ होता है।
उदाहरण के लिए, स्टील चिप्स और भूरे रंग को ऑक्सीकरण भी किया जाता है, इसलिए गर्मी जारी की जाती है, लेकिन कम ऑक्सीकरण दर के कारण, यह हमेशा जलने का कारण नहीं बनता है। फिल्म में आयल पेंट। चित्रित सतह पर, ऑक्सीकरण प्रक्रिया होती है, लेकिन हीटिंग गर्मी सिंक की बहुत बड़ी सतह के कारण, यह मनाया नहीं जाता है।
इसलिए, प्रतिक्रिया, ऑक्सीकरण के कारण तापमान टी 2 तक गरम किया गया मिश्रण धीरे-धीरे तापमान टी 1 तक ठंडा हो जाएगा (जैसे ही मिश्रण में प्रतिक्रियाशील पदार्थों की एकाग्रता कम हो जाती है)। यह इस प्रकार है कि तापमान टी तक गरम किए गए एक दहनशील मिश्रण की ऑक्सीकरण की प्रक्रिया कम प्रतिक्रिया दर में जलने में नहीं जा सकती है।
हम मिश्रण के ऑक्सीकरण की गति को बढ़ाते हैं, इसे तापमान टी 3 में हीटिंग करते हैं। गर्मी सिंक की गति अपरिवर्तित बनी हुई है, क्योंकि पोत की सतह नहीं बदली है। इससे इस तथ्य का कारण बन सकता है कि एक दहनशील मिश्रण के तापमान पर, गर्मी की गति लगातार गर्मी सिंक की गति से अधिक हो रही है और मिश्रण उच्च तापमान के लिए स्वयं निकास करने में सक्षम होगा। जब मिश्रण का तापमान दहन तापमान तक पहुंच जाता है, तो लौ दिखाई देगी और जलती है। नतीजतन, स्व-जलने के प्रवाह के लिए पूर्व शर्त गर्मी सिंक गति के ऊपर मिश्रण में गर्मी रिलीज दर से अधिक है।
इसलिए, थर्मल स्व-जलने को जलने की प्रक्रिया कहा जाता है, जो राज्य को गर्म पदार्थों के स्वयं हीटिंग के परिणामस्वरूप होता है, जिसकी प्रक्रिया में ऑक्सीकरण प्रतिक्रिया के कारण गर्मी रिलीज दर गर्मी सिंक की गति से अधिक होती है। स्व-इग्निशन तापमान आमतौर पर जहाज की दीवारों के तापमान पर शुल्क लिया जाता है, जिसमें इन स्थितियों में आत्म-जलन होती है।
थर्मल स्व-इग्निशन की प्रक्रिया को समय के आधार पर माना जा सकता है (चित्र 15.2)।
ऑक्सीकरण तापमान के नीचे गर्म हवा में ईंधन की स्थिति। इस मामले में पदार्थ का तापमान धीरे-धीरे बढ़ेगा (वक्र 1) और थोड़ी देर के बाद हवा के तापमान टी 0 के बराबर होगा। क्योंकि ऑक्सीकरण तापमान के नीचे t0, ईंधन गैर-दहनशील के रूप में व्यवहार करेगा। यदि हवा को टी 1 के तापमान तक गरम किया जाता है, जो इस पदार्थ के ऑक्सीकरण तापमान से अधिक होगा, तो दहनशील पदार्थ (वक्र 2) तापमान पर गर्म हो जाएगा, टी 1 में अधिक, लेकिन फिर तापमान गिरावट शुरू हो जाएगा।

अंजीर। 15.2। गर्म होने पर दहनशील पदार्थों के तापमान में अनुसूची परिवर्तन
हम तापमान टीएस\u003e टी 1 तक गर्म हैं। स्वाभाविक रूप से, इस मामले में ऑक्सीकरण प्रतिक्रिया की गति पिछले एक की तुलना में काफी अधिक होगी, और पदार्थ का तापमान टीएस वायु तापमान से ऊपर बढ़ेगा, टीबी मूल्यों तक पहुंच जाएगा, जिसके बाद के तापमान में तेजी से वृद्धि होगी दहन तापमान के लिए पदार्थ घटित होगा। गैस मिश्रण के उदाहरण पर स्वयं जलने की प्रक्रिया न केवल दहनशील वाष्प और गैसों के लिए विशेषता है। यह ठोस पर लागू होता है।
आत्म-इग्निशन का तापमान एक ही दहनशील पदार्थ के लिए निरंतर मूल्य नहीं है। यह गर्मी उत्पादन और गर्मी सिंक वेगों पर निर्भर करता है, जो बदले में दहनशील पदार्थ की मात्रा और आकार, मात्रा, दबाव और अन्य कारकों की एक इकाई में इसकी संरचना पर निर्भर करता है। कुछ ज्वलनशील और दहनशील पदार्थों के स्व-इग्निशन तापमान (डिग्री सेल्सियस में) की सीमाएं निम्नानुसार हैं:

थर्मल (बाहरी हीटिंग के साथ) के अलावा, स्व-जलन अभी भी सूक्ष्मजीवविज्ञान और रासायनिक है।
सूक्ष्मजीवों की क्रिया के तहत पदार्थों के द्रव्यमान में आत्म-हीटिंग के कारण माइक्रोबायोलॉजिकल स्व-जलन उत्पन्न होती है। अनाज, घास, पीट, कोयले, आदि को संग्रहीत करते समय यह घटना देखी जाती है।
एक बड़ी ऑक्सीकरण सतह की उपस्थिति और पर्यावरण में कम गर्मी हस्तांतरण की उपस्थिति में हवा और पानी (वनस्पति तेल और पशु वसा, तेल) के संपर्क में होने पर पदार्थों की रासायनिक बातचीत के परिणामस्वरूप रासायनिक आत्म-जलती हुई होती है।
कुछ दहनशील पदार्थों में आत्म-इग्निशन का तापमान 500 डिग्री सेल्सियस से अधिक हो सकता है, और दूसरों में - 16 डिग्री सेल्सियस से नीचे होने के लिए। एक स्व-इग्निशन तापमान वाले सभी दहनशील पदार्थों को दो समूहों में विभाजित किया जा सकता है: पदार्थ जिनमें आत्म-इग्निशन तापमान होता है सामान्य से ऊपर (16-25 डिग्री सेल्सियस) और नीचे। पहले समूह के पदार्थ केवल तभी सक्षम होते हैं जब उन्हें एक या दूसरे तापमान पर गर्म किया जाता है, दूसरे समूह के पदार्थ अतिरिक्त हीटिंग के बिना स्वयं समन्वित होते हैं, क्योंकि पर्यावरण ने उन्हें पहले ही इग्निशन तापमान में गर्म कर दिया है। दहनशील पदार्थों में वृद्धि हुई आग की खतरा है, क्योंकि उन्हें कुछ शर्तों के तहत प्रज्वलित करने की संभावना नहीं है। उदाहरण के लिए, ऑक्सीकरण के परिणामस्वरूप पाउडर के रूप में एल्यूमीनियम दहन की घटना के लिए स्व-हीटिंग करने में सक्षम है। स्व-हीटिंग सामान्य परिवेश तापमान और यहां तक \u200b\u200bकि कम, और जलने के साथ समाप्त हो सकता है। यदि एक पतला कपड़ा, तेल के साथ संश्लेषित, एक तंग बनाते हैं, फिर ऑक्सीकरण के दौरान गठित गर्मी, हवा और रोशनी कपड़े में विलुप्त होने का समय नहीं होगा। हालांकि, अगर एक ही ऊतक विघटित होता है, और मोड़ नहीं होता है, तो स्व-जलन नहीं होगी, क्योंकि तेजी से ऑक्सीकरण प्रक्रिया में आवंटित गर्मी अपने गठन की गति से अधिक दर पर वातावरण में विलुप्त हो जाएगी।
इसलिए, दूसरे समूह से संबंधित पदार्थों को जानना बहुत महत्वपूर्ण है, क्योंकि यह आपको अपने भंडारण और परिवहन के लिए शर्तों को स्थापित करने की अनुमति देता है विशेष जरूरतेंइससे आग लगाना असंभव हो जाता है।
उदाहरण के लिए, जैसा कि आप जानते हैं, खनिज, संयंत्र और पशु तेल हैं। खनिज तेल केवल उच्च तापमान पर हवा में ऑक्सीकरण, और इसलिए आत्म-बारी नहीं है। एक चीर के आत्म जलने के मामले हैं, खनिज विमान के तेलों के साथ गीले हुए, जो वनस्पति तेलों की अशुद्धियों के परिणामस्वरूप उभरा। स्व-जलने में सक्षम कार्बनिक यौगिक युक्त वसा और तेल।
स्व-जलने की क्षमता का आकलन आयोडीन संख्या - आयोडीन ग्राम की संख्या, जो 100 ग्राम तेल के संबंध में आता है। तेल में अधिक कनेक्शन, अधिक आयोडीन आयोडीन में शामिल हो जाता है और इसलिए, स्व-जलने की अधिक क्षमता होती है।
अनुक्रमों के साथ सूखने में तेजी लाने के लिए ओलीफ, रेशेदार सामग्रियों पर लागू, स्वयं जलने में सक्षम है। अर्ध-प्राकृतिक I कृत्रिम ओलिफ लुमिंग या आत्म-मोड़ हो सकता है। तेल, वसा या ओलिफा, जो किसी भी बंद कंटेनर में हैं, आत्म-मोड़ नहीं हो सकते हैं, क्योंकि हवा के साथ उनसे संपर्क करने की सतह बहुत छोटी है। ऑक्सीकरण की सतह में काफी वृद्धि होने पर तेल और वसा की क्षमता में काफी वृद्धि होती है अधिक सतह गर्मी का हस्तांतरण। ऐसी स्थितियां तब बनाई जाती हैं जब धोए गए सामग्रियों को ढेर, ढेर, पैकेज और एक दूसरे के समीप संकलित किया जाता है। स्व-जलने वाले तेल और वसा धोने वाली सामग्री के पैकिंग की घनत्व पर निर्भर करता है। एक निश्चित सीमा को सील करने के मामले में आत्म-जलने की क्षमता, जिसके बाद यह घटने लगती है।
आत्म-इग्निशन की प्रक्रिया में एक महत्वपूर्ण भूमिका परिवेश का तापमान चलाती है। हवा का तापमान जितना अधिक होता है, धोया गई सामग्री की मात्रा को स्व-जलने में सक्षम होता है, और तेलों को कम की आवश्यकता होती है। इस मामले में आग की संभावना कई बार बढ़ जाती है।
सबसे छोटा तापमान, जिसके साथ: जो स्वयं जलने वाले तेल और वसा देखी जाती है, 10-15 डिग्री सेल्सियस के बराबर होती है। सूती अपशिष्ट गर्भवती है वनस्पति तेल (ग्राहक ऊतक समाप्त होता है), में स्थितियों के आधार पर आत्म-मोड़ हो सकता है अलग - अलग समय (कई घंटों से कई दिनों तक)।
प्रेरण की अवधि (स्व-इग्निशन में देरी की अवधि) जो पदार्थ जो आत्म-बारी, गैसों और तरल पदार्थ में सक्षम हैं, गैसीय माध्यम में ऑक्सीकरण किया जाता है, बहुत कम। एरोसोल की स्थिति में ठोस में लगभग एक ही अवधि।
गांठ के रूप में ठोस पदार्थों की प्रेरण की अवधि विभिन्न आकार यह लंबा हो सकता है क्योंकि इस मामले में ऑक्सीकरण की सतह थी। ऑक्सीकरण की सतह पर वायु प्रसार की एक छोटी और गति।
स्व-जलने को ज्वाला की उपस्थिति के साथ स्व-जलन कहा जाता है। जलती हुई आग और विस्फोट के साथ हो सकती है।
पदार्थों और सामग्रियों की दहनशीलता को तीन समूहों में विभाजित किया गया है: - ऐसी सामग्री और संरचनाएं हैं जो आग में लगी नहीं हैं, जो क्रिया या उच्च तापमान में शामिल नहीं हैं और उन्हें चार्ज नहीं किया जाता है (उदाहरण के लिए, ऑक्सीकरण एजेंट या पदार्थों को उत्सर्जित करने वाले पदार्थों को विसर्जित करने वाले पदार्थों को उत्सर्जित करते हैं जब एक दोस्त के साथ पानी, हवा ऑक्सीजन या दोस्त के साथ बातचीत करना);
सामग्री और संरचनाएं खाने, जो आग या उच्च तापमान की क्रिया के तहत, सगाई, स्मोल्डिंग या चिल्लाती हैं और इग्निशन के स्रोत के साथ जला और जलाशय और अनुकूलित होती हैं, और इसे हटा दिए जाने के बाद, इन प्रक्रियाओं को समाप्त कर दिया जाता है।
इसमे शामिल है कृत्रिम सामग्री, गैर-दहनशील को छोड़कर खनिज पदार्थ, कार्बनिक समेकन के वजन से 80% से अधिक है; हार्ड-फटे योग्य सामग्रियों से बने डिज़ाइन, साथ ही जलने योग्य, अग्नि से संरक्षित और गैर-उत्तेजित सामग्रियों (एएसबेस्टोस और छत ग्रंथियों से ढके लकड़ी)
सामग्री और संरचनाएं, जो आग या उच्च तापमान की क्रिया के तहत, इग्निटर के स्रोत को हटाने के बाद जलती हैं, फंसे हुए या बंदरगाह और जलती हैं। इनमें सभी कार्बनिक पदार्थ शामिल हैं, आग या उच्च तापमान से संरक्षित नहीं हैं।
गरम किए जाने पर गरम किए जाने वाले शुरुआती कुल राज्य (ठोस, तरल, गैसीय) के बावजूद अधिकांश दहनशील पदार्थ हवा के साथ दहनशील मिश्रणों को सक्रिय करते हैं। आग की तैयारी वाष्प, धूल या गैसीय उत्पादों की संरचना (एकाग्रता) द्वारा निर्धारित की जाती है। हवा में दहनशील पदार्थों की न्यूनतम और अधिकतम सांद्रता होती है, नीचे और ऊपर जो आग लगाना असंभव है।
इन सांद्रता को तदनुसार निचला और शीर्ष कहा जाता है एकाग्रता सीमा ज्वलनशीलता।
फ्रैमेबल गैसों और ठोस कटा हुआ पदार्थ (धूल) किसी भी तापमान पर दहनशील मिश्रण बना सकते हैं। ठोस, साथ ही तरल पदार्थ केवल कुछ तापमान पर दहनशील मिश्रण बनाते हैं। यदि मिश्रण उपर्युक्त स्थितियों के अनुपालन में तैयार किया जाता है, तो यह माना जा सकता है कि यह आग के लिए तैयार है, जो इग्निशन स्रोत की स्थिति में उत्पन्न हो सकता है।
लौ (इग्निशन) के प्रसार की तापमान सीमा उस पदार्थ के ऐसे तापमान हैं जिनके तहत यह है संतृप्त भाप निचले (निचले तापमान सीमा) और ऊपरी (ऊपरी तापमान सीमा) के बराबर एक ऑक्सीडेटिव माध्यम में एक एकाग्रता बनाता है जो लौ प्रसार की एकाग्रता सीमाओं के बराबर है।
लौ वितरण की तापमान सीमाओं का मूल्य उपयोग किया जाता है: जब वस्तु की आग और विस्फोट सुरक्षा सुनिश्चित करने के उपायों को विकसित करना; आग और विस्फोटक की गणना करने के लिए तापमान मोड तकनीकी उपकरणों का संचालन; अनुमान आपातकालीन क्षणदहनशील तरल पदार्थ फैलाने के साथ जुड़े; लौ वितरण की एकाग्रता सीमाओं की गणना। तापमान सीमाओं का तापमान मानकों या में शामिल किया जाना चाहिए तकनीकी स्थितियां दहनशील पदार्थों पर। दहन की संभावना मुख्य रूप से फ्लैश तापमान, इग्निशन, आत्म-इग्निशन और स्वयं जलने से विशेषता है।
स्वयमेव जल उठनाExothermich आत्मसम्मान के कारण दहनशील ठोस सामग्री के स्व-हीटिंग के परिणामस्वरूप घटना। प्रतिक्रियाएं। आत्म-जलन इस तथ्य के कारण होता है कि प्रतिक्रियाओं के दौरान गर्मी अपव्यय पर्यावरण में अधिक गर्मी सिंक है।
स्व-जलने की शुरुआत स्व-हीटिंग तापमान द्वारा विशेषता है ( टी सीएच), जो अनुभव की शर्तों के तहत न्यूनतम है, तापमान जिस पर गर्मी अपव्यय का पता चला है।
जब स्व-हीटिंग की प्रक्रिया में प्राप्त होता है विशिष्ट तापमान, जिसे स्व-जलती तापमान कहा जाता है ( टी ध्वनि), नाली या लौ जलने से प्रकट सामग्री का दहन होता है। बाद के मामले में टी पर्याप्त तापमान ध्वनि ( टी एसवी), जिसके तहत अग्नि अधिनियम में उभरता है और कुछ महत्वपूर्ण तापमान के लिए गर्म होने पर। (अग्नि मामले में देखें) .
सिद्धांत रूप में, भौतिक इकाई में स्वयं जलने और आत्म-इग्निशन समान होते हैं और केवल दहन के प्रकार में भिन्न होते हैं, आत्म-इग्निशन केवल ज्वलंत जलने के रूप में होता है।
स्व-हीटिंग (पक्षपातपूर्ण हीटिंग) के मामले में, यह कुछ और डिग्री के भीतर विकसित होता है और इसलिए आग खतरे और तरल पदार्थ का मूल्यांकन करते समय ध्यान में नहीं रखा जाता है। जब आत्म-जलन, स्वयं-हीटिंग क्षेत्र कई सौ डिग्री तक पहुंच सकता है (उदाहरण के लिए, पीट 70 से 225 डिग्री सेल्सियस तक)। नतीजतन, स्व-हीटिंग की घटना को हमेशा स्व-जलने के लिए ठोस पदार्थों की प्रवृत्ति को निर्धारित करने के लिए ध्यान में रखा जाता है
किसी दिए गए तापमान पर अध्ययन के तहत सामग्री को थर्मोस्टेट करने और तापमान के बीच निर्भरता स्थापित करने का अध्ययन किया जाता है, जिस पर जलन, नमूना आकार और थर्मोस्टेट में हीटिंग समय होता है।
दहनशील सामग्री के नमूने के स्व-जलने के दौरान होने वाली प्रक्रियाएं आकृति में दिखाए जाते हैं। तापमान पर टी Ch (जैसे, टी 1) सामग्री को अपरिवर्तित (कोई गर्मी रिलीज नहीं) गर्म किया जाता है। पहुँचने पर टी सामग्री में ch exothermic प्रतिक्रियाएं होती हैं। उत्तरार्द्ध, गर्मी संचय (भौतिक द्रव्यमान, अपने परमाणुओं और अणुओं की पैकेजिंग की घनत्व, प्रक्रिया की अवधि, आदि) की शर्तों के आधार पर सक्षम होने के थकावट पर एक छोटे आत्म-हीटिंग की अवधि के बाद हो सकता है थर्मोस्टेट (वक्र 1) के प्रारंभिक तापमान तक नमूना से ठंडा होने के लिए सामग्री घटकों का आत्म-कारण या समायोजित करना जारी रखें टी ध्वनि (वक्र 2)। ओब्लास्त टी च I टी सोज़ोस संभावित रूप से खतरनाक हैं, नीचे टी एस.एन. -
सुरक्षित।
तापमान परिवर्तन टीसमय में ईंधन सामग्री के थर्मोस्टेड नमूने में टी।
संभावित रूप से आग-खतरनाक क्षेत्र में स्वयं जलती हुई सामग्री की संभावना समीकरणों का उपयोग करके सेट की जाती है:
कहा पे टी OKR-Embetter पर्यावरण, ° C; एल- सामग्री की आकार (आमतौर पर मोटाई) निर्धारित करना; टी-टाइम जिसके दौरान आत्म-जलन हो सकती है; ए। 1 , एन 1 I लेकिन अ 2 , एन प्रयोगात्मक डेटा (तालिका देखें) के अनुसार प्रत्येक सामग्री के लिए 2 -Coefer परिभाषित।
एक दिए गए के लिए समीकरण (1) द्वारा एल खोज टी ओसीसी जिस पर आत्म-जलन हो सकती है पदार्थ, समीकरण द्वारा (2) -prident ज्ञात टी ओसीसी मान टी। नीचे एक तापमान पर गणना की गई टी ओसीडी, या टी, समीकरण (2) द्वारा गणना की गई समय से कम, स्व-जलने नहीं होगा।
प्रारंभिक प्रक्रिया की प्रकृति के आधार पर, जिससे सामग्री की आत्म-हीटिंग, और मूल्यों का कारण बनता है टी सीएच कोमिकल, माइक्रोबायोलॉजिकल और थर्मल स्व-जलती हुई

रासायनिक स्व-जलने में पदार्थों की एक्सोथर्मिक इंटरैक्शन शामिल है (उदाहरण के लिए, जब कागज पर केंद्रित एचएनओ 3 द्वारा मारा जाता है, लकड़ी भूरा और आदि।)। ऐसी प्रक्रिया का सबसे सामान्य और सामान्य उदाहरण पानी वाले वाहन या एक विकसित सतह के साथ अन्य रेशेदार सामग्रियों का स्व-जलन है। असंतृप्त रासायनिक बंधनों के साथ यौगिकों वाले खतरनाक तेल और उच्च आयोडीन संख्या (सूती, सूरजमुखी, जूट, आदि) द्वारा विशेषता।
रासायनिक स्व-जलने की घटना में कई पदार्थों की रोशनी भी शामिल है (उदाहरण के लिए, छोटे-सेरेब्रेड अल और एफई, एसआई हाइड्राइड, इन और कुछ धातुओं, ऑर्गोमेटलिक यौगिकों - एल्यूमिनियमोर्गनिक, आदि) जब वे संपर्क में होते हैं हीटिंग की अनुपस्थिति में हवा। ऐसी स्थितियों में आत्म-जलने के पदार्थों की क्षमता को पायरोफॉर्म कहा जाता है। पाइरोफोरिक पदार्थों की सुविधा यह है कि वे हैं टी ध्वनि (या। टी एसवी) कमरे के तापमान के नीचे: - एसआईएच 4 के लिए 200 डिग्री सेल्सियस, ए 1 के लिए 80 डिग्री सेल्सियस (सी 2 एच 5) 3। रासायनिक स्व-जलने को रोकने के लिए, दहनशील पदार्थों और सामग्रियों को सह-भंडारण करने की प्रक्रिया सख्ती से विनियमित होती है।
सूक्ष्मजीवविज्ञान स्व-जलने की प्रवृत्ति में दहनशील सामग्री होती है, विशेष रूप से नमकीन, जो सूक्ष्मजीवों के लिए पोषक माध्यम के रूप में कार्य करती है, जिसकी आजीविका गर्मी (पीट, लकड़ी के भूरे, आदि) की रिहाई से जुड़ी होती है। इस कारण से, बड़ी संख्या में आग और विस्फोट होते हैं जब कृषि उत्पादों (उदाहरण के लिए, सिलो, गीली घास) को लिफ्ट में संग्रहीत किया जाता है। माइक्रोबायोलॉजिकल और रासायनिक स्व-जलने के लिए, यह विशेषता है कि टी Ch सामान्य मूल्यों से अधिक नहीं है टी ओसीसी और नकारात्मक हो सकता है। होने वाली सामग्री टी कमरे के तापमान से ऊपर, थर्मल स्व-जलने में सक्षम
सामान्य रूप से, एक विकसित सतह (उदाहरण के लिए, रेशेदार) के साथ कई ठोस सामग्री, साथ ही साथ कुछ तरल और पिघलने वाले पदार्थ, जिसमें असंतृप्त यौगिक होते हैं, विकसित (गैर-दहनशील) सतह पर लागू होते हैं, सभी प्रकार के स्वयं की प्रवृत्ति होती है -जलता हुआ। रासायनिक, माइक्रोबायोलॉजिकल और थर्मल स्व-जलने के लिए महत्वपूर्ण परिस्थितियों की गणना समीकरणों (1) और (2) द्वारा की जाती है। प्रायोगिक परिभाषा के तरीके टी
अग्निशमन घटनाओं और बुझाने वाली आग को बुझाने के दौरान होने वाली रासायनिक और भौतिक प्रक्रियाओं के सार की समझ के बिना असंभव है। इन प्रक्रियाओं को जानना सफलतापूर्वक आग से निपटने के लिए संभव बनाता है।
जलती एक रासायनिक ऑक्सीकरण प्रतिक्रिया है, साथ ही बड़ी मात्रा में गर्मी और आमतौर पर एक चमक के साथ रिलीज के साथ। दहन की प्रक्रिया में ऑक्सीडाइज़र ऑक्सीजन हो सकता है, साथ ही क्लोरीन, ब्रोमाइन और अन्य पदार्थ भी हो सकते हैं।
ज्यादातर मामलों में, आग के मामले में, दहनशील पदार्थों का ऑक्सीकरण हवा से ऑक्सीजन होता है। इस प्रकार का ऑक्सीकरण एजेंट और भविष्य की प्रस्तुति में अपनाया गया। दहन संभव है यदि जलने में सक्षम पदार्थ है, ऑक्सीजन (वायु) और इग्निशन स्रोत। यह आवश्यक है कि एक क्रोध पदार्थ और ऑक्सीजन कुछ मात्रात्मक संबंधों में हैं, और इग्निशन के स्रोत में थर्मल ऊर्जा की आवश्यक आपूर्ति थी।
यह ज्ञात है कि हवा में लगभग 21% ऑक्सीजन होता है। अधिकांश पदार्थों की जलन असंभव हो जाती है जब हवा में ऑक्सीजन सामग्री 14-18% हो जाती है, और केवल कुछ दहनशील पदार्थ (हाइड्रोजन, ईथिलीन, एसिटिलीन इत्यादि) को जलाया जा सकता है जब ऑक्सीजन सामग्री 10% तक हवा में होती है और कम से। ऑक्सीजन सामग्री में और कमी के साथ, अधिकांश पदार्थों को जलाना बंद कर दिया जाता है।
ईंधन और ऑक्सीजन पदार्थ प्रतिक्रिया दे रहे हैं और ईंधन प्रणाली बनाते हैं, और इग्निशन स्रोत दहन प्रतिक्रिया का कारण बनता है। इग्निशन का स्रोत लुढ़का हुआ शरीर के जलती पीपी हो सकता है, साथ ही एक विद्युत निर्वहन होता है जिसमें दहन में होने के लिए पर्याप्त ऊर्जा आरक्षित होता है।
दहनशील प्रणालियों को सजातीय और अमानवीय में बांटा गया है। वर्दी वे सिस्टम हैं जिनमें ईंधन और हवा समान रूप से एक दूसरे के साथ मिश्रित होते हैं (दहनशील गैसों के मिश्रण, हवा के साथ भाप)। इस तरह के सिस्टम के दहन को गतिशील जलती हुई कहा जाता है। गति रासायनिक प्रतिक्रिया की दर से निर्धारित की जाती है, जो उच्च तापमान पर महत्वपूर्ण है। कुछ स्थितियों के तहत, इस तरह का दहन विस्फोट या विस्फोट की प्रकृति हो सकती है। असामान्य प्रणाली जिसमें एक ईंधन और हवा एक-दूसरे के साथ मिश्रित नहीं होती है और इसमें अनुभाग की सतह होती है (ठोस दहनशील सामग्री और अस्पष्ट तरल पदार्थ)। अमानवीय दहनशील प्रणालियों के दहन की प्रक्रिया में, वायु ऑक्सीजन को दहन उत्पादों के माध्यम से ईंधन में घुसपैठ (फैलाव) में प्रवेश करता है और इसके साथ प्रतिक्रिया में प्रवेश करता है। इस तरह के जलने को प्रसार दहन कहा जाता है, क्योंकि इसकी गति मुख्य रूप से अपेक्षाकृत धीमी प्रक्रिया-प्रसार द्वारा निर्धारित की जाती है।
आग लगाने के लिए, इग्निशन के स्रोत की गर्मी दहनशील पदार्थों को जोड़े और गैसों में परिवर्तित करने और उन्हें आत्म-इग्निशन के तापमान पर गर्म करने के लिए पर्याप्त होनी चाहिए। ईंधन और ऑक्सीडेंट के अनुपात से, गरीब और समृद्ध दहनशील मिश्रणों के दहन की प्रक्रियाओं को प्रतिष्ठित किया जाता है। गरीब मिश्रणों में अधिक ऑक्सीकरण एजेंट होता है और ईंधन घटक की कमी होती है। रिच मिक्स, इसके विपरीत, अतिरिक्त और ऑक्सीकरण एजेंट के नुकसान में एक ज्वलनशील घटक होता है।
दहन की घटना प्रणाली में प्रतिक्रिया के अनिवार्य आत्मविश्वास से जुड़ी है। जलने के लिए अपने संक्रमण के साथ आत्मनिर्भर प्रतिक्रिया की प्रक्रिया को आत्म-इग्निशन कहा जाता है। दहन पर एक रासायनिक प्रतिक्रिया का स्वयं-सिफ्टिंग तीन मुख्य प्रकारों में विभाजित है: गर्मी, श्रृंखला और संयुक्त - श्रृंखला-थर्मल। गर्मी सिद्धांत द्वारा, रासायनिक प्रतिक्रिया की गति में वृद्धि के साथ ऑक्सीकरण प्रक्रिया के सक्रियण द्वारा स्वयं-इग्निशन की प्रक्रिया को समझाया जाता है। श्रृंखला सिद्धांत द्वारा, आत्म-इग्निशन की प्रक्रिया रासायनिक प्रतिक्रिया की श्रृंखला की शाखाओं के कारण होती है। व्यावहारिक रूप से दहन प्रक्रिया मुख्य रूप से संयुक्त श्रृंखला-थर्मल तंत्र द्वारा की जाती है।
दहन पूर्ण और अधूरा अंतर करता है। पूर्ण दहन के साथ, उत्पादों का गठन किया जाता है जो अधिक जलाने में असमर्थ हैं: कार्बन डाइऑक्साइड, सल्फर गैस, पानी जोड़े। अपूर्ण दहन तब होता है जब ऑक्सीजन की पहुंच जलती हुई ज़ोन के लिए मुश्किल होती है, नतीजतन, अपूर्ण दहन उत्पाद बनते हैं: कार्बन मोनोऑक्साइड, अल्कोहल, एल्डेहाइड इत्यादि बनते हैं।
लगभग हवा की मात्रा (एम 3), जो 1 किलो पदार्थ के दहन (या गैस के 1 मीटर 3) के दहन के लिए आवश्यक है,
जहां क्यू दहन, केजे / किग्रा, या केजे / एम 3 की गर्मी है।
कुछ पदार्थों की गर्मी दहन: गैसोलीन -47 000 केजे / किग्रा; एयर-ड्राई -14 600 केजे / किग्रा की वुड्स; एसिटिलीन - 54400 केजे / एम 3; मीथेन - 3 9 400 केजे / एम 3; कार्बन ऑक्साइड - 12,600 केजे / एम 3।
दहनशील पदार्थ के दहन की गर्मी पर, यह निर्धारित करना संभव है कि अपने दहन, दहन तापमान, बंद वॉल्यूम और अन्य डेटा में विस्फोट के दौरान दबाव के दौरान कितना गर्मी जारी की जाती है।
पदार्थ के दहन तापमान को सैद्धांतिक और मान्य दोनों को परिभाषित किया गया है। सैद्धांतिक दहन तापमान है, जिस पर दहन उत्पादों को गरम किया जाता है, एक धारणा के रूप में कि जलन के दौरान प्रतिष्ठित सभी गर्मी गर्म हो जाती है।
सैद्धांतिक दहन तापमान
जहां मीटर 1 किलो पदार्थ के दहन के दौरान गठित दहन उत्पादों की मात्रा है; सी दहन उत्पादों, केजे / (किलो * के) की गर्मी क्षमता है; θ - हवा का तापमान, के; क्यू - दहन की गर्मी, केजे / किग्रा।
वास्तविक दहन तापमान 30-50% कम सैद्धांतिक है, क्योंकि जलने के दौरान जारी गर्मी का एक महत्वपूर्ण हिस्सा पर्यावरण में विलुप्त हो जाता है।
उच्च दहन तापमान आग के फैलाव में योगदान देता है, इसके साथ गर्मी की एक बड़ी मात्रा पर्यावरण के लिए उत्सर्जित होती है, और जलने के लिए दहनशील पदार्थों की गहन तैयारी होती है। उच्च दहन तापमान पर आग बुझाने में बाधा है।
दहन प्रक्रियाओं पर विचार करते समय, निम्नलिखित प्रकारों को प्रतिष्ठित किया जाना चाहिए: एक फ्लैश, आग, इग्निशन, आत्म-इग्निशन, स्वयं जलने, विस्फोट।
फ्लैश एक दहनशील मिश्रण का तेज़ दहन है, संपीड़ित गैसों के गठन के साथ नहीं।
आग इग्निशन स्रोत के प्रभाव में दहन की घटना है।
ज्वाला की उपस्थिति के साथ सूजन एक आग है।
विफलता - इग्निशन स्रोत के प्रभाव में प्रज्वलित करने की क्षमता (आग लगाना)।
स्व-जलन exothermic प्रतिक्रियाओं की गति में तेज वृद्धि की घटना है, जिससे एक इग्निशन स्रोत की अनुपस्थिति में पदार्थों (सामग्री, मिश्रण) की उत्पीड़न की घटना होती है।
आत्म-इग्निशन ज्वाला की उपस्थिति के साथ स्व-जलन है।
एक विस्फोट को ऊर्जा की रिहाई और यांत्रिक कार्य के उत्पादन में सक्षम संपीड़ित गैसों के गठन के साथ एक पदार्थ के बेहद तेज़ रासायनिक (विस्फोटक) रूपांतरण कहा जाता है।
इग्निशन (इग्निशन) और स्व-जलने (आत्म-इग्निशन) की प्रक्रियाओं के बीच अंतर को समझना आवश्यक है। खुद को सूजन करने के लिए, एक दहनशील तंत्र में थर्मल पल्स बनाना आवश्यक है जिसमें पदार्थ के आत्म-इग्निशन तापमान से अधिक तापमान होता है। आत्म-इग्निशन के तापमान से नीचे तापमान पर जलने की घटना स्व-जलने (आत्म-इग्निशन) की प्रक्रिया को संदर्भित करती है।
दहन एक इग्निशन स्रोत के बिना होता है - थर्मल या माइक्रोबायोलॉजिकल स्व-जलने के कारण।
गर्मी स्व-जलती हुईएक छिपे हुए या बाहरी हीटिंग स्रोत के प्रभाव में स्व-हीटिंग के परिणामस्वरूप पदार्थ होते हैं। आत्म-इग्निशन केवल तभी संभव है जब आत्म-परीक्षा के दौरान उत्पन्न गर्मी की मात्रा पर्यावरण में गर्मी की वापसी से अधिक हो जाएगी।
माइक्रोबायोलॉजिकल स्व जलन यह पदार्थ (सामग्री, मिश्रण) के द्रव्यमान में सूक्ष्मजीवों की आजीविका के प्रभाव के तहत स्व-हीटिंग के परिणामस्वरूप होता है। आत्म-इग्निशन का तापमान दहनशील पदार्थ की एक महत्वपूर्ण विशेषता है।
आत्म-इग्निशन तापमान पदार्थ का सबसे कम तापमान होता है जिस पर exothermic प्रतिक्रियाओं की गति में तेज वृद्धि होती है, जो लौ जलने के उद्भव के साथ समाप्त होता है।
मशीन-निर्माण उद्योग में उपयोग किए जाने वाले कुछ तरल पदार्थ, गैसों और ठोस पदार्थों के स्व-इग्निशन तापमान तालिका में दिखाए जाते हैं। 28।
तालिका 28। कुछ तरल पदार्थों के स्व-इग्निशन तापमान
| पदार्थ | स्व-इग्निशन तापमान, ° с |
फास्फोरस व्हाइट |
20 |
Seroublerod। |
112 |
सिलोलाइड |
140-180 |
हाइड्रोजन सल्फाइड |
246 |
तेल तेल |
250-400 |
| 250 | |
गैसोलीन ए -76 |
255 |
| 380-420 | |
कोयला |
400 |
एसिटिलीन |
406 |
इथेनॉल |
421 |
लकड़ी का कोयला |
450 |
nitrobenzene |
482 |
| 530 | |
| 612 | |
| 625 | |
कार्बन मोनोऑक्साइड |
644 |
| 700 |
आत्म-इग्निशन के तापमान के अलावा, दहनशील पदार्थों को आत्म-इग्निशन के प्रेरण या मंदता समय की अवधि की विशेषता है। प्रेरण अवधि को समय की अवधि कहा जाता है,
जबकि इग्निशन के लिए स्व-हीटिंग। असमान के एक ही दहनशील पदार्थ के लिए प्रेरण की अवधि और मिश्रण, प्रारंभिक तापमान और दबाव की संरचना के आधार पर है।
प्रेरण अवधि कम-शक्ति सूजन स्रोतों (स्पार्क्स) के ईंधन पर कार्रवाई में व्यावहारिक महत्व की है। स्पार्क, वायु के साथ वाष्प या गैसों के ईंधन मिश्रण में शामिल होना, मिश्रण की कुछ मात्रा को गर्म करता है, और साथ ही स्पार्क ठंडा हो रहा है। मिश्रण की इग्निशन मिश्रण की प्रेरण अवधि और स्पार्क के शीतलन समय के अनुपात पर निर्भर करता है। साथ ही, यदि प्रेरण अवधि स्पार्क के शीतलन समय से अधिक है, तो मिश्रण की इग्निशन नहीं होगी।
प्रेरण अवधि इग्निशन के संबंध में खतरे की डिग्री के अनुसार गैस मिश्रणों के वर्गीकरण पर आधारित है। धूल मिश्रणों की प्रेरण की अवधि धूल के आकार, अस्थिर पदार्थों की संख्या, आर्द्रता और अन्य कारकों पर निर्भर करती है।
कुछ पदार्थ सामान्य तापमान पर होने के नाते आत्म-बारी हो सकते हैं। यह मुख्य रूप से ठोस छिद्रपूर्ण पदार्थ ज्यादातर कार्बनिक मूल (भूसा, पीट, जीवाश्म कोयला, आदि) है। एक बड़ी सतह पर एक पतली परत द्वारा वितरित स्व-जलने और तेलों के लिए प्रवण। यह धोए गए वीटो के स्वयं जलने की संभावना का कारण बनता है। धोया रेशेदार सामग्रियों के स्व-जलने का कारण उन सतहों पर एक पतली परत और हवा से ऑक्सीजन के अवशोषण के साथ फैटी पदार्थों का वितरण है। तेल ऑक्सीजन का ऑक्सीकरण गर्मी रिलीज के साथ होता है। ऐसे मामले में जहां गर्मी की मात्रा पर्यावरण में गर्मी की कमी से अधिक हो जाती है, आग का उदय हो सकता है।
स्व-जलने के लिए प्रवण पदार्थों का अग्नि खतरा बहुत अधिक है, क्योंकि वे पदार्थों के आत्म-इग्निशन तापमान के नीचे परिवेश के तापमान पर किसी भी गर्मी की आपूर्ति के बिना प्रकाश डाल सकते हैं, और स्वयं-बोले गए पदार्थों की प्रेरण की अवधि कई घंटे हो सकती है, दिन और यहां तक \u200b\u200bकि महीने। ऑक्सीकरण (पदार्थ की सुनवाई) के त्वरण की परिणामी प्रक्रिया को केवल तभी रोक दिया जा सकता है जब तापमान में खतरनाक वृद्धि का पता चला हो जाता है, जो आग-निवारक उपायों के महान महत्व को इंगित करता है।
मशीन निर्माण उद्यमों पर स्वयं जलने में सक्षम कई पदार्थों का उपयोग किया जाता है। आयरन, सूट, एल्यूमीनियम और जस्ता पाउडर के सल्फिड हवा के साथ बातचीत करते समय आत्म-मोड़ हो सकते हैं, और डॉ। आत्म-मोड़ पानी के साथ बातचीत करते समय क्षारीय धातु, धातुओं की कार्बाइड, आदि कैल्शियम कार्बाइड (सीएसी 2), पानी के साथ प्रतिक्रिया कर सकते हैं , फॉर्म एसिटिलीन (सी 2 एन 2)।





