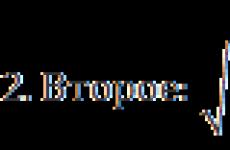Alkanes हाइड्रोजन के साथ बातचीत करते हैं। Alkanov का अंतर्राष्ट्रीय नामकरण। अल्कांस: संरचना, गुण। सुगंधित हाइड्रोकार्बन के रासायनिक गुण
सीमा हाइड्रोकार्बन ऐसे यौगिक हैं जो कार्बन परमाणुओं से युक्त अणु होते हैं जो हाइब्रिडाइजेशन एसपी 3 की स्थिति में होते हैं। वे एक दूसरे के साथ विशेष रूप से सहसंयोजक सिग्मा बांड से जुड़े हुए हैं। नाम "सीमा" या "संतृप्त" हाइड्रोकार्बन इस तथ्य से आगे बढ़ता है कि ये यौगिक किसी भी परमाणु संलग्न करने में सक्षम नहीं हैं। वे बेहद संतृप्त हैं। अपवाद साइक्लॉकनस है।
एल्केन्स क्या है?
Alkanians सीमा के हाइड्रोकार्बन हैं, और उनकी कार्बन श्रृंखला unbripped है और इसमें एकल संबंधों का उपयोग करके कार्बन परमाणुओं से जुड़े होते हैं। इसमें अन्य नहीं होते हैं (यानी, डबल, जैसे अल्केन, या ट्रिपल, जैसे अल्किलोव) कनेक्शन। अल्कांस को पैराफिन भी कहा जाता है। उन्होंने इस नाम को प्राप्त किया, क्योंकि प्रसिद्ध पैराफिन मुख्य रूप से इन सीमा हाइड्रोकार्बन के मिश्रण हैं, जिसमें विशेष रूप से 18-सी 35 के साथ विशेष रूप से जड़ता है।
एल्कन और उनके रेडिकल के बारे में सामान्य जानकारी
उनका सूत्र: सी एन पी 2 एन +2, यहां एन एन से अधिक या बराबर है। दाढ़ी द्रव्यमान की गणना सूत्र द्वारा की जाती है: एम \u003d 14 एन + 2. एक विशेषता विशेषता: उनके नामों में अंत "-एएन" है। अन्य परमाणुओं को हाइड्रोजन परमाणुओं को बदलने के परिणामस्वरूप गठित उनके अणुओं के अवशेषों को अल्फाटिक रेडिकल, या एल्किल कहा जाता है। वे आर आर द्वारा दर्शाए गए हैं। Monovalent Aliphatic रेडिकल के लिए सामान्य सूत्र: एनपी 2 एन +1 के साथ, यहां एन 1 से अधिक या बराबर है। एलीफेटिक रेडिकल के दाढ़ी द्रव्यमान की गणना सूत्र द्वारा की जाती है: m \u003d 14n + 1 । अल्फाटिक रेडिकल की विशेषता विशेषता: नामों में समाप्त होना "- आईएल। अल्कानोव अणुओं की संरचना की अपनी विशेषताएं हैं:
- सी-सी का कनेक्शन 0.154 एनएम की लंबाई की विशेषता है;
- सी-एच कनेक्शन 0.10 9 एनएम की लंबाई की विशेषता है;
- वैलेंस कोण (कार्बन कार्बन के बॉन्ड के बीच का कोण) 109 डिग्री और 28 मिनट के बराबर है।

एल्केन्स की होमोलॉगस श्रृंखला शुरू होती है: मीथेन, इथेन, प्रोपेन, ब्यूटेन, और इतने पर।
Alkanov के भौतिक गुण
अल्कांस ऐसे पदार्थ होते हैं जिनमें रंग नहीं होते हैं और पानी में अघुलनशील होते हैं। जिस तापमान में अल्कान पिघलने लगते हैं, और जिस तापमान पर वे उबालते हैं, वे आणविक भार में वृद्धि और हाइड्रोकार्बन श्रृंखला की लंबाई के अनुसार बढ़ रहे हैं। कम शाखाओं वाले से अधिक शाखाओं वाले एलकनों तक, उबलते और पिघलने वाले तापमान को कम कर दिया जाता है। गैसीय एल्केन एक पीले नीले या रंगहीन लौ को जलाने में सक्षम हैं, जबकि काफी गर्मी खड़ी है। सीएच 4 -सी 4 एच 10 गैसें हैं जो अनुपस्थित और गंध भी हैं। सी 5 एच 12 -सी 15 एच 32 तरल पदार्थ हैं जिनके पास एक विशिष्ट गंध है। 15 एन 32 और इसी तरह से, ये ठोस हैं जो गंध भी नहीं करते हैं।
Alkanov के रासायनिक गुण
ये यौगिक एक रासायनिक योजना में कम सक्रिय हैं, जिन्हें हार्ड-परिष्कृत सिग्मा-लिंक - सी-सी और सी-एन की ताकत से समझाया जा सकता है। यह भी ध्यान में रखना चाहिए कि सी-सी के साथ संबंध गैर-ध्रुवीय हैं, और एसएन कम ध्रुवीय है। ये उपस्थिति के सिग्मा से संबंधित लिंक के कम-ध्रुवीय प्रकार हैं और तदनुसार, सबसे बड़ी संभावना को तोड़ने के लिए वे एक गोमोलिटिकल तंत्र बन जाएंगे, जिसके परिणामस्वरूप कट्टरपंथी गठित किए जाएंगे। इस प्रकार, अल्कानान के रासायनिक गुण मुख्य रूप से कट्टरपंथी प्रतिस्थापन की प्रतिक्रियाओं तक ही सीमित हैं।

न्यूटिंग प्रतिक्रियाएं
अल्कान केवल 10% की एकाग्रता के साथ नाइट्रिक एसिड के साथ या एक गैस माध्यम में एक टेट्राफिक नाइट्रोजन ऑक्साइड के साथ 140 डिग्री सेल्सियस के तापमान पर इंटरैक्ट करते हैं। अल्केन नाइट्रेशन की प्रतिक्रिया कोलोवलोव की प्रतिक्रिया कहा जाता है। नतीजतन, नाइट्रो यौगिकों और पानी बनते हैं: सीएच 4 + नाइट्रिक एसिड (पतला) \u003d सी 3 - संख्या 2 (नाइट्रोमेथेन) + पानी।
रिएक्शन जल रहा है
सीमा हाइड्रोकार्बन को अक्सर ईंधन के रूप में उपयोग किया जाता है, जो उनके शरीर की क्षमता से न्यायसंगत है: एन पी 2 एन + 2 + ((3 एन + 1) / 2) ओ 2 \u003d (एन + 1) एच 2 ओ + एन सीओ 2 के साथ।
ऑक्सीकरण प्रतिक्रियाएं
अलकनानों के रासायनिक गुणों में ऑक्सीकरण की उनकी क्षमता भी शामिल है। इस पर निर्भर करता है कि किन स्थितियों के साथ प्रतिक्रिया के साथ और उन्हें कैसे बदला जाता है, विभिन्न अंत उत्पादों को प्राप्त करने के लिए एक ही पदार्थ से प्राप्त किया जा सकता है। एक उत्प्रेरक की उपस्थिति में मीथेन ऑक्सीजन का मुलायम ऑक्सीकरण जो प्रतिक्रिया को तेज करता है, और लगभग 200 डिग्री सेल्सियस के तापमान में निम्नलिखित पदार्थों में परिणाम हो सकता है:
1) 2CH 4 (ऑक्सीजन ऑक्सीकरण) \u003d 2sh 3 यह (शराब - मेथनॉल)।
2) सीएच 4 (ऑक्सीजन ऑक्सीकरण) \u003d सीएच 2 ओ (एल्डेहाइड - मेथनल या फॉर्मल्डेहाइड) + एन 2 ओ।
3) 2CH 4 (ऑक्सीजन ऑक्सीकरण) \u003d 2NSON (कार्बोक्साइलिक एसिड - मीथेन या फॉर्मिक) + 2 एन 2 ओ।

इसके अलावा, अल्कानों का ऑक्सीकरण एक गैसीय या तरल हवा में उत्पादित किया जा सकता है। ऐसी प्रतिक्रियाएं उच्च फैटी अल्कोहल और संबंधित एसिड के गठन की ओर ले जाती हैं।
हीटिंग के लिए रवैया
तापमान पर + 150-250 डिग्री सेल्सियस से अधिक नहीं है, जरूरी उत्प्रेरक की उपस्थिति में, कार्बनिक पदार्थों का संरचनात्मक पुनर्गठन होता है, जिसमें परमाणुओं के परिसर के क्रम को बदलने में शामिल होता है। इस प्रक्रिया को आइसोमेराइजेशन कहा जाता है, और प्रतिक्रिया के परिणामस्वरूप प्राप्त पदार्थ - आइसोमर। इस प्रकार, सामान्य ब्यूटेन से यह अपने आइसोमर - आइसोबूटेन को बदल देता है। 300-600 डिग्री सेल्सियस के तापमान और उत्प्रेरक की उपस्थिति में, हाइड्रोजन अणुओं (डीहाइड्रोजनीकरण प्रतिक्रिया), एक चक्र में कार्बन श्रृंखला बंद करने के साथ हाइड्रोजन अणुओं के साथ सी-एच बॉन्ड का टूटना होता है (चक्रवात प्रतिक्रिया या अल्कानोव अरोमाइजेशन प्रतिक्रियाएं):
1) 2ch 4 \u003d सी 2 एच 4 (ईथेन) + 2 एन 2।
2) 2ch 4 \u003d सी 2 एच 2 (एथिन) + 3 एच 2।
3) सी 7 एच 16 (सामान्य हेपेन) \u003d सी 6 एच 5 - सी 3 (टोल्यून) + 4 एन 2।

हलोजन प्रतिक्रिया
ऐसी प्रतिक्रियाएं कार्बनिक पदार्थ अणु में हलोजन (उनके परमाणुओं) की शुरूआत में हैं, जिसके परिणामस्वरूप सी-हलोजन कनेक्शन बनता है। हलोजन के साथ एल्केन की बातचीत में, हलोजन डेरिवेटिव बनते हैं। इस प्रतिक्रिया में विशिष्ट विशेषताएं हैं। यह कट्टरपंथी के तंत्र से आगे बढ़ता है, और उचित रूप से उचित होने के लिए, पराबैंगनी विकिरण को प्रभावित करने के लिए हलोजन और अल्कानानों को प्रभावित करना आवश्यक है या बस इसे गर्म करना आवश्यक है। अल्कानान के गुण हलोजन परमाणुओं के लिए पूर्ण प्रतिस्थापन प्राप्त होने तक हलोजन प्रतिक्रिया को प्रवाह करने की अनुमति देते हैं। यही है, मीथेन का क्लोरिनेशन एक चरण और मिथाइल क्लोराइड के उत्पादन के साथ समाप्त नहीं होगा। प्रतिक्रिया आगे बढ़ेगी, सभी संभावित प्रतिस्थापन उत्पादों का गठन किया जाएगा, क्लोरोमेथेन से शुरू और टेट्रेक्लोरोमेथेन के साथ समाप्त हो जाएगा। अन्य अल्कानों पर इन स्थितियों के तहत क्लोरीन के प्रभाव के परिणामस्वरूप विभिन्न कार्बन परमाणुओं में हाइड्रोजन प्रतिस्थापन के परिणामस्वरूप प्राप्त विभिन्न उत्पादों का गठन होगा। उस तापमान से जिस पर प्रतिक्रिया चल रही है, सीमित उत्पादों का अनुपात और उनके गठन की गति पर निर्भर करेगा। एलकेन की हाइड्रोकार्बन श्रृंखला जितनी लंबी होगी, इस प्रतिक्रिया के लिए यह आसान होगा। जब हलोजन, कार्बन परमाणु को पहले कम से कम हाइड्रोजनीकृत (तृतीयक) के साथ प्रतिस्थापित किया जाएगा। प्राथमिक अन्य सभी के बाद प्रतिक्रिया दर्ज करेगा। चरणों में हलोजन प्रतिक्रिया होती है। पहले चरण में, केवल एक हाइड्रोजन परमाणु प्रतिस्थापित किया जाता है। हलोजन समाधान (क्लोरीन और ब्रोमाइन पानी) के साथ, एल्केन्स इंटरैक्ट नहीं करते हैं।

सल्फूलिंग प्रतिक्रियाएं
अलकनानों के रासायनिक गुणों को सल्फूलिंग प्रतिक्रिया से भी पूरक किया जाता है (इसे प्रतिक्रिया की प्रतिक्रिया कहा जाता है)। पराबैंगनी विकिरण के संपर्क में आने पर, एल्केन क्लोरीन और सल्फर डाइऑक्साइड के मिश्रण के साथ प्रतिक्रिया करने में सक्षम हैं। नतीजतन, क्लोराइड का गठन होता है, साथ ही एक अल्किल कट्टरपंथी, जो सल्फर डाइऑक्साइड में शामिल होता है। नतीजतन, एक जटिल यौगिक प्राप्त किया जाता है, जो क्लोरीन परमाणु के कब्जे और इसके एक अणु के विनाश के कारण स्थिर हो जाता है: आर-एच + तो 2 + सीएल 2 + पराबैंगनी विकिरण \u003d आर-एसओ 2 सीएल + एचसीएल। प्रतिक्रिया के परिणामस्वरूप गठित सल्फोनिल क्लोराइड का उपयोग सर्फैक्टेंट के उत्पादन में व्यापक रूप से उपयोग किया जाता है।
सबसे सरल कार्बनिक यौगिक हैं हाइड्रोकार्बनकार्बन और हाइड्रोजन से मिलकर। हाइड्रोकार्बन में रासायनिक बंधनों की प्रकृति और कार्बन और हाइड्रोजन के बीच संबंधों के आधार पर, वे सीमित और अप्रत्याशित (अल्केन्स, एल्किन्स इत्यादि) में विभाजित हैं।
सीमाहाइड्रोकार्बन (एलकैनस, मीथेन पंक्ति के हाइड्रोकार्बन) हाइड्रोजन के साथ कार्बन के यौगिक हैं, जिनके अणुओं में प्रत्येक कार्बन एटम एक यौगिक पर किसी भी अन्य पड़ोसी परमाणु के साथ एक से अधिक वैधता के साथ खर्च करता है, और सभी वैलेंस को कनेक्ट होने की अनुमति नहीं दी जाती है हाइड्रोजन कार्बन के लिए। एल्केन में सभी कार्बन परमाणु एसपी 3 - स्थिति में हैं। सीमा हाइड्रोकार्बन सामान्य सूत्र द्वारा विशेषता एक समरूप श्रृंखला बनाते हैं से एन एन 2n + 2। । इस श्रृंखला की जुड़वां प्राथमिकता मीथेन है।
आइसोमेरिया। नामकरण।
एन \u003d 1,2,3 के साथ एल्कन केवल एक आइसोमर के रूप में मौजूद हो सकते हैं
एन \u003d 4 के साथ शुरू, संरचनात्मक आइसोमेरिज्म की घटना प्रकट होती है।

कार्बन परमाणुओं की संख्या में वृद्धि के साथ क्षारों के संरचनात्मक आइसोमर की संख्या तेजी से बढ़ रही है, उदाहरण के लिए, पेंटन में 3 आइसोमर, हेप्टन - 9, आदि हैं।
अल्केन आइसोमर्स की संख्या बढ़ जाती है और संभावित स्टीरियोइंसर के कारण। सी 7 एन 16 से शुरू, चिराल अणुओं का अस्तित्व जो दो enantiomers बनाते हैं संभव है।
एल्केन्स का नामकरण।
प्रमुख नामकरण IUPAC नामकरण है। उसी समय, यह मामूली नामों के तत्व प्रस्तुत करता है। इस प्रकार, एल्केन्स की होमोलॉगस श्रृंखला के पहले चार सदस्यों में तुच्छ नाम हैं।
सीएच 4 - मीथेन
2n 6 - एथेन से
सी 3 एच 8 - प्रोपेन
4 एच 10 - भूटान के साथ।
शेष homologues के नाम ग्रीक लैटिन संख्यात्मक से गठित किया जाता है। तो, कई सामान्य (अनियंत्रित) निर्माण के निम्नलिखित सदस्यों के लिए, नामों का उपयोग किया जाता है:
5 एच 12 से - पेंटन, 6 एच 14 से - हेक्सेन, 7 एच 18 - हेप्टेन से,
14 एच 30 से टेट्राडेकैन, 15 एच 32 - पेंटाडेकन इत्यादि से
शाखाओं वाले अल्कानोव के लिए IUPAC के बुनियादी नियम
ए) सबसे लंबी अनियंत्रित श्रृंखला चुनें, जिसका नाम आधार (रूट) है। यह आधार प्रत्यय "ए"
बी) कम से कम लॉकर्स के सिद्धांत पर इस श्रृंखला को संख्या,
सी) प्रतिस्थापन स्थान के स्थान को इंगित करने वाले वर्णमाला क्रम में उपसर्ग के रूप में इंगित करता है। यदि वसंत संरचना में कई समान प्रतिस्थापन हैं, तो उनकी संख्या ग्रीक संख्यात्मक को इंगित करती है।
अन्य कार्बन परमाणुओं की संख्या के आधार पर जिनके साथ कार्बन एटम सीधे जुड़ा हुआ है, प्रतिष्ठित: प्राथमिक, माध्यमिक, तृतीयक और क्वाटरनेरी कार्बन परमाणु।


एल्किल समूह या अल्किल रेडिकल को ब्रांडेड एल्कन में सबस्टिट्यूट के रूप में वर्णित किया गया है, जिन्हें एक हाइड्रोजन परमाणु के अल्केन अणु से कटौती के परिणामस्वरूप माना जाता है।
एल्किल समूहों का नाम इसी एलकनों के नाम से अंतिम प्रत्यय "ए" को द सॉफिक्स "आईएल" में बदलकर फॉर्म का नाम है।
सी 3 - मिथाइल
सी 3 च 2 - एथिल
Ch 3 ch 2 ch 2 - प्रोपिल

ब्रांडेड एल्किल समूहों के नाम के लिए, श्रृंखला की संख्या का भी उपयोग किया जाता है:

एथेन से शुरू, एल्केन्स कॉनफॉर्मर बनाने में सक्षम हैं, जो अवरोधित संरचना से मेल खाते हैं। अस्पष्ट के माध्यम से दूसरे को एक अवरुद्ध संरचना के संक्रमण की संभावना रोटेशन के अवरोध द्वारा निर्धारित की जाती है। संरचना का निर्धारण, conformers और रोटेशन बाधाओं की संरचना विनोचन विश्लेषण के कार्य हैं। क्षीण प्राप्त करने के तरीके।
1. प्राकृतिक गैस या गैसोलीन तेल अंश का आंशिक आसवन।इस तरह, व्यक्तिगत एल्केन को 11 कार्बन परमाणुओं को अलग किया जा सकता है।
2. कोयले का हाइड्रोजनीकरण।प्रक्रिया 450-470 डिग्री सेल्सियस पर उत्प्रेरक (मोलिब्डेनम, टंगस्टन, निकल के ऑक्साइड और सल्फाइड्स) की उपस्थिति में की जाती है और 30 एमपीए तक दबाव डालती है। कोयला और उत्प्रेरक पाउडर और हाइड्रोजनीकृत हाइड्रोजनीकृत में ट्रिटुरेटेड होते हैं, निलंबन के माध्यम से हाइड्रोजन को रोकते हैं। एक मोटर ईंधन के रूप में एल्केन और साइक्लॉकन के परिणामस्वरूप मिश्रण का उपयोग किया जाता है।
3. हाइड्रोजनीकरण सह और साथ 2 .
सीओ + एच 2 एल्केन्स
सीओ 2 + एच 2 एल्केन्स
सह, फे, और अन्य इन प्रतिक्रियाओं के उत्प्रेरक के रूप में उपयोग किया जाता है। डी - तत्व।
4. एलकेन्स और एल्किन्स का हाइड्रोजनीकरण।

5. धातु विज्ञान संश्लेषण।
लेकिन अ)। Watza का संश्लेषण।
2rhal + 2na r r + 2nahal
यह संश्लेषण अनुपयुक्त है यदि दो अलग-अलग हेलोलेनास कार्बनिक अभिकर्मकों के रूप में उपयोग किए जाते हैं।
b)। Grignar अभिकर्मकों का प्रोटोलिसिस।
R hal + mg rmghal
Rmghal + hoh आरएच + एमजी (ओह) हैल
में)। एल्किल हॉलिड्स के साथ लिथियम डायलकिपैट्स (एलआईआर 2 सीयू) की बातचीत
Lir 2 cu + r x r r + rcu + lix
लिथियम डायलकिपैट्स खुद को दो-चरण विधि द्वारा प्राप्त किए जाते हैं।
2r li + cui lir 2 cu + lii
6. कार्बोक्सालिक लवण (सिंटेज़ कोल्बे) का इलेक्ट्रोलिसिस।
2RCOONA + 2H 2 O r r + 2CO 2 + 2NAOH + H 2

7. क्षार के साथ कार्बोक्साइलिक एसिड नमक का रोल।
प्रतिक्रिया का उपयोग निचले एल्केन को संश्लेषित करने के लिए किया जाता है।
8. कार्बोनेल यौगिकों और हेलोलियनोव का हाइड्रोजेनोलिसिस।
लेकिन अ)। कार्बोनील यौगिकों। क्लेमेंट का संश्लेषण।

b)। हलोजन। उत्प्रेरक हाइड्रजनोलिसिस।
![]()
एनआई, पीटी, पीडी उत्प्रेरक के रूप में उपयोग किया जाता है।
ग) हलोजन। अभिकर्मक वसूली।
Rhal + 2Hi आरएच + HHAL + I 2
एल्केन के रासायनिक गुण।
एल्केन में सभी कनेक्शन कम-ध्रुवीय हैं, इस पर वे कट्टरपंथी प्रतिक्रियाओं द्वारा विशेषता है। पीआई बांड की अनुपस्थिति अनुलग्नक की प्रतिक्रिया के लिए असंभव बनाती है। अल्कानान के लिए, प्रतिस्थापन, दरार, दहन की प्रतिक्रिया विशेषता है।
|
प्रतिक्रिया का प्रकार और नाम | |
|
1. प्रतिस्थापन की प्रतिक्रियाएं | |
|
ए) हलोजन के साथ (से) क्लोरोमसीएल। 2 -और प्रकाश, Br। 2 - गर्म होने पर) प्रतिक्रिया obeys markovnik नियम (नियम Markovnikov) - मुख्य रूप से हलोजन कम से कम हाइड्रोजनीकृत कार्बन परमाणु में हाइड्रोजन की जगह लेता है। प्रतिक्रिया चरणों में गुजरती है - एक चरण के लिए एक से अधिक हाइड्रोजन परमाणु को प्रतिस्थापित नहीं किया जाता है। आयोडीन का जवाब देने का सबसे कठिन तरीका, और इसके अलावा, प्रतिक्रिया अंत में नहीं जाती है, उदाहरण के लिए, आयोडीन के साथ मीथेन की बातचीत के साथ, आयोडाइड हाइड्रोजन का गठन होता है, मेथेन और आयोडीन के गठन के साथ आयोडाइड मिथाइल के साथ प्रतिक्रिया करता है (रिवर्सिबल रिएक्शन): |
सीएच 4 + सीएल 2 → सी 3 सीएल + एचसीएल (क्लोरोमेथेन) सीएच 3 सीएल + सीएल 2 → सीएच 2 सीएल 2 + एचसीएल (डिक्लोरोमेथेन) सीएच 2 सीएल 2 + सीएल 2 → सीएचसीएल 3 + एचसीएल (ट्राइक्लोरोमेथेन) सीएलसीएल 3 + सीएल 2 → सीसीएल 4 + एचसीएल (टेट्रैक्लोरोमेथेन)। |
|
बी) नटिंग (Konovalov प्रतिक्रिया) एल्कान गैस चरण में 10% नाइट्रिक एसिड समाधान या नाइट्रोजन ऑक्साइड एन 2 ओ 4 के साथ 140 डिग्री के तापमान पर और नाइट्रो-उत्पादन के गठन के साथ मामूली दबाव के साथ प्रतिक्रिया कर रहे हैं। प्रतिक्रिया भी मार्कोवनिकोव के शासन का पालन करती है। हाइड्रोजन परमाणुओं में से एक को अवशेष संख्या 2 (नाइट्रो समूह) द्वारा प्रतिस्थापित किया गया है और पानी प्रतिष्ठित है |
|
|
2. क्लेवाज की प्रतिक्रियाएं | |
|
ए) निर्जलीकरण - हाइड्रोजन। प्रतिक्रिया की स्थिति उत्प्रेरक -प्लैटिन और तापमान। |
Ch 3 - ch 3 → ch 2 \u003d ch 2 + h 2 |
|
B) क्रैकिंग एक छोटी श्रृंखला के साथ कनेक्शन बनाने के लिए बड़े अणुओं की कार्बन श्रृंखला के विभाजन की प्रतिक्रिया के आधार पर, हाइड्रोकार्बन की थर्मल अपघटन की प्रक्रिया। 450-700 ओ के तापमान पर, एलकैन्स सी-सी बॉन्ड के टूटने के कारण विघटित हो जाते हैं (इस तरह के तापमान के अधिक टिकाऊ सी-एनपीआरआई बॉन्ड संरक्षित होते हैं) और एल्केन और अल्केन्स कार्बन परमाणुओं की एक छोटी संख्या के साथ गठित होते हैं। |
सी। 6 एच 14 सी। 2 एच 6 + सी। 4 एच 8 |
|
सी) पूर्ण थर्मल अपघटन |
सीएच 4 सी + 2 एच 2 |
|
3. ऑक्सीकरण प्रतिक्रियाएं | |
|
A) जलती हुई प्रतिक्रिया (टी \u003d 600 ओ सी) को आग लगने पर, एल्केन ऑक्सीजन के साथ प्रतिक्रिया करते हैं, जबकि उनके ऑक्सीकरण कार्बन डाइऑक्साइड और पानी के लिए हो रहा है। |
सी एन 2 एन + 2 + ओ 2 -\u003e सीओ 2 + एच 2 ओ + क्यू सीएच 4 + 2 ओ 2 -\u003e सीओ 2 + 2 एच 2 ओ + क्यू |
|
बी) उत्प्रेरक ऑक्सीकरण- अपेक्षाकृत कम तापमान के साथ और उत्प्रेरक का उपयोग करके अणु और सी-एन के बीच में सी-थाईफोल्ड के बंधनों के केवल हिस्से के टूटने के साथ और मूल्यवान उत्पाद प्राप्त करने के लिए उपयोग किया जाता है: कार्बोक्साइलिक एसिड, केटोन, एल्डिहाइड, अल्कोहल। |
उदाहरण के लिए, ब्यूटेन के अपूर्ण ऑक्सीकरण के साथ (संचार सी 2 -सी 3 -सी 3) का बंधन एसिटिक एसिड द्वारा प्राप्त किया जाता है |
|
4. आइसोमेराइजेशन की प्रतिक्रियाएं arakterna सभी Alkanov के लिए नहीं। उत्प्रेरक की उपस्थिति, दूसरों के लिए एक आइसोमर को परिवर्तित करने की संभावना के लिए ध्यान खींचा जाता है। |
सी 4 एच 10 सी 4 एच 10 |
|
5.. 6 या अधिक कार्बन परमाणुओं में मुख्य श्रृंखला के साथ एल्कन भी प्रतिक्रिया dehydrocyclization, लेकिन हमेशा एक 6 सदस्यीय चक्र (साइक्लोहेक्सन और इसके डेरिवेटिव) का निर्माण होगा। प्रतिक्रिया परिस्थितियों में, यह चक्र आगे डीहाइड्रोजनीकरण के अधीन है और सुगंधित हाइड्रोकार्बन (क्षेत्र) के ऊर्जावान रूप से अधिक स्थिर बेंजोल चक्र में बदल जाता है। |
|
हलोजन प्रतिक्रिया तंत्र:
हेलॉयडिंग
एल्केन्स का हलोजन एक कट्टरपंथी तंत्र के माध्यम से आगे बढ़ता है। प्रतिक्रिया शुरू करने के लिए, यूवी प्रकाश या गर्मी को विकिरण करने के लिए अल्केन और हलोजन का मिश्रण आवश्यक है। मीथेन क्लोराइनेशन मेथिल क्लोराइड प्राप्त करने के चरण में नहीं रुकता है (यदि क्लोरीन और मीथेन की समानता की मात्रा ली जाती है), और मिथाइल क्लोराइड से टेट्रैक्लौपर तक सभी संभावित प्रतिस्थापन उत्पादों के गठन की ओर अग्रसर होती है। अन्य एल्केन्स का क्लोरिनेशन विभिन्न कार्बन परमाणुओं में हाइड्रोजन प्रतिस्थापन उत्पादों के मिश्रण की ओर जाता है। क्लोरिनेशन उत्पादों का अनुपात तापमान पर निर्भर करता है। प्राथमिक, माध्यमिक और तृतीयक परमाणुओं के क्लोरीनीकरण की दर तापमान पर निर्भर करती है, कम तापमान पर, गति पंक्ति में घट जाती है: तृतीयक, माध्यमिक, प्राथमिक। बढ़ते तापमान के साथ, गति के बीच का अंतर तब तक घटता है जब तक यह समान नहीं होता है। गतिशील कारक के अलावा, क्लोरीननीकरण उत्पादों के वितरण का सांख्यिकीय कारक का असर पड़ता है: क्लोरीन हमले की संभावना प्राथमिक और दोगुनी से 3 गुना कम है। इस प्रकार, एल्केन्स का क्लोरिनेशन एक गैर-स्टेरो-चुनिंदा प्रतिक्रिया है, जो मामलों को खत्म कर देता है जब केवल एक मोनोक्लोरीनेशन उत्पाद संभव होता है।
हलोजनकरण प्रतिस्थापन की प्रतिक्रियाओं में से एक है। अल्कानोव का हलोजनमेशन मार्कोवनिक (मार्कोव्निकोव नियम) के नियम का पालन करता है - मुख्य रूप से कम से कम हाइड्रोजनीकृत कार्बन परमाणु को हल करता है। Alkanan Halogenation धीरे-धीरे गुजरता है - एक चरण में, एक से अधिक हाइड्रोजन परमाणु हलोजन नहीं किया जाता है।
सीएच 4 + सीएल 2 → सी 3 सीएल + एचसीएल (क्लोरोमेथेन)
सीएच 3 सीएल + सीएल 2 → सीएच 2 सीएल 2 + एचसीएल (डिक्लोरोमेथेन)
सीएच 2 सीएल 2 + सीएल 2 → सीएचसीएल 3 + एचसीएल (ट्राइक्लोरोमेथेन)
सीएलसीएल 3 + सीएल 2 → सीसीएल 4 + एचसीएल (टेट्रेक्लोरोमेथेन)।
प्रकाश की क्रिया के तहत, क्लोरीन अणु परमाणुओं के लिए क्षय होता है, फिर वे मीथेन अणुओं पर हमला करते हैं, नतीजतन, हाइड्रोजन परमाणु पर फाड़ते हैं, मेथिल रेडिकल गठित होते हैं, जिन्हें क्लोरीन अणुओं का सामना करना पड़ता है, उन्हें नष्ट कर दिया जाता है, उन्हें नष्ट कर दिया जाता है और नए रेडिकल बनाने का सामना करना पड़ता है।
Nitching (Konovalov प्रतिक्रिया)
एल्कान गैस चरण में 10% नाइट्रिक एसिड समाधान या नाइट्रोजन ऑक्साइड एन 2 ओ 4 के साथ 140 डिग्री के तापमान पर और नाइट्रो-उत्पादन के गठन के साथ मामूली दबाव के साथ प्रतिक्रिया कर रहे हैं। प्रतिक्रिया भी मार्कोवनिकोव के शासन का पालन करती है।
आरएच + एचएनओ 3 \u003d आरएनओ 2 + एच 2 ओ
यानी हाइड्रोजन परमाणुओं में से एक को अवशेष संख्या 2 (एनआई-ट्रोग्रुप) द्वारा प्रतिस्थापित किया गया है और पानी प्रतिष्ठित है।
आइसोमर्स की संरचना की विशेषताएं इस प्रतिक्रिया के दौरान दृढ़ता से प्रतिबिंबित होती हैं, क्योंकि एसआई अवशेष (केवल कुछ आइसोमर में मौजूदा) में नाइट्रो समूह में हाइड्रोजन परमाणु को प्रतिस्थापित करना सबसे आसान है, सीएच 2 समूह में हाइड्रोजन है कम आसानी से, और और भी मुश्किल - अवशेष सी 3 में।
नाइट्रोजन डाइऑक्साइड या नाइट्रिक एसिड जोड़े के 150-475 डिग्री सेल्सियस पर गैस चरण में पैराफिन पहनना काफी आसान है; इस मामले में, यह भाग में होता है और। ऑक्सीकरण। मीथेन की थ्रेडिंग लगभग विशेष रूप से नाइट्रोमेथेन है:
सभी उपलब्ध डेटा एक मुक्त कट्टरपंथी तंत्र इंगित करते हैं। प्रतिक्रिया के परिणामस्वरूप, उत्पादों के मिश्रण का गठन किया जाता है। सामान्य तापमान पर नाइट्रिक एसिड लगभग पैराफिन हाइड्रोकार्बन पर कार्य नहीं करता है। गर्म होने पर, यह मुख्य रूप से एक ऑक्सीकरण एजेंट के रूप में कार्य करता है। हालांकि, जैसा कि मैंने एम। I. Konovovalov (1889) पाया, गर्मियों में नाइट्रिक एसिड अधिनियम और "तनाव" तरीके से काम करता है; कमजोर नाइट्रिक एसिड के साथ नाइट्रेशन की प्रतिक्रिया हीटिंग और ऊंचे दबाव के तहत विशेष रूप से अच्छी तरह से अच्छी तरह से अच्छी तरह से है। नाइट्रेशन की प्रतिक्रिया समीकरण द्वारा व्यक्त की जाती है।
मीथेन के बाद, होमोलॉग गुजरने वाले विभाजन के कारण विभिन्न नाइट्रोपराफिन का मिश्रण देते हैं। जब ईथेन के नाइट्रोजेनेशन को नाइट्रेटन सी 3-सी 2-एन 2 और नाइट्रोमेथेन सी 3 -नहीं 2 प्राप्त किया जाता है। प्रोपेन से नाइट्रोपराफिन का मिश्रण बनता है:
गैस चरण में पैराफिन नटिंग अब एक औद्योगिक पैमाने पर किया जाता है।
सल्फूलिंग:
एक महत्वपूर्ण प्रतिक्रिया अल्कानानों की सल्फोक्लिलेशन है। जब अल्केन क्लोरीन और सल्फर आराइड्राइड के साथ बातचीत करता है, तो हाइड्रोजन को क्लोरोसुलफोनिल समूह के साथ बदल दिया जाता है:

इस प्रतिक्रिया के चरण:
सीएल + आर: एच → आर + एचसीएल
आर + तो 2 → आरएसओ 2
आरएसओ 2 + सीएल: सीएल → आरएसओ 2 सीएल + सीएल
AlcanofoClorrides आसानी से alkanesulfoxylost (आरएसओ 2 ओएच), सोडियम नमक (आरएसओ 3¯ Na + - सोडियम alkanfonate) के लिए sodium नमक के लिए hydrolyzed हैं, जो साबुन के समान गुण प्रदर्शित करते हैं और निर्धारकों के रूप में उपयोग किया जाता है।
भौतिक गुण। सामान्य परिस्थितियों में, अल्कानानों की होमोलॉगस श्रृंखला के पहले चार सदस्य (1 से 4) गैसें हैं। पेंटन से हेप्टाडेकन तक सामान्य एल्केन्स (सी 5 - सी 17 ) - 18 और ऊपर से शुरू होने वाले तरल पदार्थ - ठोस। चूंकि श्रृंखला में कार्बन परमाणुओं की संख्या बढ़ जाती है, यानी। बढ़ते सापेक्ष आणविक भार के साथ, alkanes के उबलते और पिघलने का तापमान बढ़ता है। एक शाखा की संरचना के साथ एल्कवेड अल्केन अणु में कार्बन परमाणुओं की संख्या के साथ, सामान्य एल्केन की तुलना में कम उबलते बिंदु हैं।
अल्काना पानी में व्यावहारिक रूप से अघुलनशील, चूंकि उनके अणु कम-ध्रुवीय होते हैं और पानी के अणुओं के साथ बातचीत नहीं करते हैं, वे गैर-ध्रुवीय कार्बनिक सॉल्वैंट्स, जैसे बेंजीन, टेट्रेक्लोरोमेथेन इत्यादि में अच्छी तरह से घुलनशील होते हैं। तरल एल्केन आसानी से एक दूसरे के साथ मिश्रित होते हैं।
अल्कानन के मुख्य प्राकृतिक स्रोत - तेल और प्राकृतिक गैस। विभिन्न तेल अंशों में एल्केन्स होते हैंसी 5 एच 12 30 H 62 तक। प्राकृतिक गैस में मीथेन और प्रोपेन के एक मिश्रण के साथ मीथेन (9 5%) शामिल हैं।
का प्राप्त करने के सिंथेटिक तरीकेअल्कानोव आप निम्न का चयन कर सकते हैं: /\u003e
एक । असंतृप्त हाइड्रोकार्बन से प्राप्त करना। हाइड्रोजन ("हाइड्रोजनीकरण") के साथ अलकेन्स या एल्किन्स की बातचीत धातु उत्प्रेरक (/\u003e नी, पीडी की उपस्थिति में होती है ) जैसा
गरम करना:
च डब्ल्यू - C ≡SN + 2 एन 2 → सी 3-सीएच 2-सीएच 3।
2। बाहर निकलते हुए हलोजन प्रोडक्ट्स। धातु सोडियम के साथ मोनोगलोजेन-प्रतिस्थापित अलकनन को गर्म करते समय, एल्केन्स एक जुड़वां संख्या कार्बन परमाणुओं (वुर्ट्ज प्रतिक्रिया) के साथ प्राप्त होते हैं: /\u003e
सी 2 एच 5 बीआर + 2 एनए + बीआर - सी 2 एच 5 → सी 2 एच 5 - सी 2 एच 5 + 2 Nabr।.
यह प्रतिक्रिया दो अलग के साथ नहीं की जाती है हलोजन एवजी Alkanians, क्योंकि यह तीन अलग-अलग अल्कानानों का मिश्रण निकलता है
3। कार्बोक्साइलिक एसिड लवण प्राप्त करना। जब क्षारियों के साथ निर्जलीय कार्बोक्सिलिक एसिड लवण फ्यूज करते हैं, तो एल्केन्स को मूल कार्बोक्साइलिक एसिड की कार्बन श्रृंखला से कम कार्बन परमाणु शामिल किया जाता है: /\u003e
4. मीथेन। हाइड्रोजन के वातावरण में जलने वाले विद्युत चाप में, मीथेन की एक महत्वपूर्ण मात्रा बनती है: /\u003e
सी + 2 एन 2 → सी 4 .
एक ही प्रतिक्रिया एक हाइड्रोजन वातावरण में कार्बन हीटिंग के साथ उत्प्रेरक की उपस्थिति में 400-500 डिग्री सेल्सियस तक होती है।
प्रयोगशाला की स्थिति में, मीथेन अक्सर एल्यूमीनियम कार्बाइड से प्राप्त किया जाता है:
एक एल 4। सी 3 + 12 एन 2 ओ \u003d जेडएसएन 4 + 4 एl (ओह) 3।
रासायनिक गुण। सामान्य परिस्थितियों में, क्षीण रासायनिक रूप से निष्क्रिय हैं। वे कई अभिकर्मकों के प्रतिरोधी हैं: केंद्रित और पिघला हुआ क्षारियों के साथ केंद्रित सल्फर और नाइट्रिक एसिड के साथ बातचीत न करें, मजबूत ऑक्सीडाइज़र द्वारा ऑक्सीकरण नहीं किया जाता है - पोटेशियम परमैंगनेटकेएमएन।लगभग 4, आदि
एल्केन की रासायनिक स्थिरता उच्च शक्ति के कारण होती हैएस -सी-एस और सी-एन कनेक्शन, साथ ही साथ उनकी गैर-ध्रुवीयता। गैर-ध्रुवीय बांड सी-सी और सी-एच इनकनों में आयन टूटने के लिए प्रवण नहीं होते हैं, लेकिन सक्रिय मुक्त कणों के प्रभाव में होमोलॉजी को विभाजित करने में सक्षम होते हैं। इसलिए, कट्टरपंथी प्रतिक्रियाएं अलकनानों की विशेषता होती हैं, जिसके परिणामस्वरूप यौगिक प्राप्त होते हैं, जहां हाइड्रोजन परमाणु अन्य परमाणुओं या परमाणुओं के समूहों के साथ प्रतिस्थापित होते हैं। नतीजतन, एल्केन्स प्रतीक द्वारा दर्शाए गए कट्टरपंथी प्रतिस्थापन के तंत्र के माध्यम से बहती प्रतिक्रिया दर्ज करते हैंएस आर ( अंग्रेजी सेप्रतिस्थापन। रेडिकिकिक). इस तंत्र के तहत, तृतीयक में हाइड्रोजन परमाणु, फिर माध्यमिक और प्राथमिक कार्बन परमाणुओं पर प्रतिस्थापित किया जाता है।
1. हलोजन। जब यूवी विकिरण या उच्च तापमान की क्रिया के तहत हलोजन (क्लोरीन और ब्रोमॉम) के साथ अल्कानन की बातचीत, मोनो से उत्पादों का मिश्रण- पॉलीहलोजेन-प्रतिस्थापित अल्कानान इस प्रतिक्रिया का समग्र आरेख मीथेन के उदाहरण पर दिखाया गया है: /\u003e
बी) श्रृंखला वृद्धि। क्लोरीन का कट्टरपंथी अल्केन अणु पर एक हाइड्रोजन परमाणु लेता है:
सीएल।· + Ch 4 → na /\u003e \u200b\u200bl + ch 3 ·
उसी समय, एक अल्किल रेडिकल का गठन किया जाता है, जो क्लोरीन अणु पर क्लोरीन परमाणु लेता है:
सी 3 · + सी एल 2 → सी 3 एल + सी के साथ एल·
इन प्रतिक्रियाओं को तब तक दोहराया जाता है जब तक सर्किट प्रतिक्रियाओं में से एक के अनुसार टूट जाता है:
सीएल।· + सीएल।→ एल /\u003e 2 के साथ, सी 3 · + सी 3 · → सी 2 एच 6, सी 3 · + सीएल।→ → सी 3 एल के साथ ·
कुल प्रतिक्रिया समीकरण:
| एचवी | ||
| सीएच 4 + एसएल 2 | → | सीएच 3 सीएल + एचसीएल। |
बनाने वाले क्लोरोमेथेन को आगे क्लोरिनेशन के अधीन किया जा सकता है, जिससे उत्पादों का मिश्रण दिया जा सकता हैसी 2 सीएल। 2, सीएचसीएल 3, एसएस एल 4 योजना के अनुसार (*).
श्रृंखला सिद्धांत का विकास मुक्त मूलक प्रतिक्रियाएं एक उत्कृष्ट रूसी वैज्ञानिक, नोबेल पुरस्कार विजेता एनआई के नाम से निकटता से संबंधित हैं। सेमेनोवा (18 9 6-1986)।
2. नटिंग (Konovalov प्रतिक्रिया)। 140 डिग्री सेल्सियस पर एल्केन के लिए पतला नाइट्रिक एसिड की क्रिया के तहत और कम दबाव एक कट्टरपंथी प्रतिक्रिया बहती है: /\u003e
कट्टरपंथी प्रतिक्रियाओं (हलोजन, नाइट्रेशन) के साथ, तृतीयक में हाइड्रोजन परमाणु, फिर माध्यमिक और प्राथमिक कार्बन परमाणुओं में मिश्रित होते हैं। यह इस तथ्य से समझाया गया है कि हाइड्रोजन (बंधन ऊर्जा 376 (3 9 0 केजे / एमओएल) के साथ तृतीयक कार्बन परमाणु का हल्का, और केवल प्राथमिक (415 केजे / एमओएल), फिर सबसे आसान है।
3. आइसोमेराइजेशन। कुछ स्थितियों के तहत सामान्य एल्केन्स एक शाखा श्रृंखला के साथ अल्केन में बदल सकते हैं: /\u003e
4. क्लैकिंग सी-सी कनेक्शन का एक हेमोलिटिक टूटना है, जो गरम होने और उत्प्रेरक की कार्रवाई के तहत बहती है।
उच्चतम एल्कन्स की क्रैकिंग पर, एलकेन्स और लोअर एल्केन बनते हैं, मीथेन और ईथेन की क्रैकिंग के दौरान एसिटिलीन का गठन किया जाता है: /\u003e
सी /\u003e 8 एच 18 → सी 4 एच 10 + सी 4 एन 8, /\u003e
2 एसएच 4 → सी 2 एच 2 + जेएन 2,
सी 2 एच 6 → सी 2 एच 2 + 2 एन 2।
इन प्रतिक्रियाओं में एक बड़ा औद्योगिक मूल्य है। इस तरह, उच्च उबलते तेल भिन्नता (ईंधन तेल) गैसोलीन, केरोसिन और अन्य मूल्यवान उत्पादों में परिवर्तित हो जाते हैं।
5. ऑक्सीकरण। विभिन्न उत्प्रेरक, मिथाइल अल्कोहल, फॉर्मल्डेहाइड, फॉर्मिक एसिड की उपस्थिति में मीथेन ऑक्सीजन के हल्के ऑक्सीजन के साथ प्राप्त किया जा सकता है:
 |
ब्यूटेन एयर ऑक्सीजन का सॉफ्ट कैटलिटिक ऑक्सीकरण - एसिटिक एसिड के उत्पादन के लिए औद्योगिक तरीकों में से एक:
टी°
2 सी 4 /\u003e एच /\u003e 10 + 5 ओ /\u003e 2 → 4 सीएच /\u003e 3 सीओईओएच /\u003e + 2 एन 2 ओ .
बिल्ली।
एयर अल्काना पर सीओ 2 और एच 2 ओ: /\u003e के लिए जला
N 2 n +2 + के साथ एन+1) / 2 ओ 2 \u003d एन 2 + (एन +1) एच 2 ओ के साथ।
अल्कांस (सीमित हाइड्रोकार्बन, पैराफिन)
- Alkana - Aliphatic (Acyclic) चरम हाइड्रोकार्बन जिसमें कार्बन परमाणुओं को अनियंत्रित या ब्रांडेड श्रृंखलाओं में सरल (एकल) कनेक्शन द्वारा जोड़ा जाता है।
अल्काना - अंतर्राष्ट्रीय नामकरण पर सीमा हाइड्रोकार्बन का नाम।
पैराफिन- ऐतिहासिक रूप से स्थापित नाम, इन यौगिकों के गुणों को दर्शाता है (लैट से। पररम affinis - कम संबंध, कम)।
सीमा, या तर-बतरइन हाइड्रोकार्बन को हाइड्रोजन के कार्बन श्रृंखला परमाणुओं की पूर्ण संतृप्ति के कारण कहा जाता है।
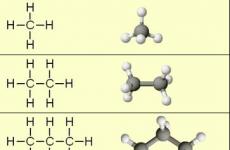
Alkanov के सबसे सरल प्रतिनिधियों:
अणु मॉडल:


इन यौगिकों की तुलना करते समय यह स्पष्ट है कि वे समूह के लिए एक-दूसरे से अलग हैं। -च 2 - (मिथिलीन)। प्रोपेन में एक और समूह जोड़ना -च 2 -, मुझे भूटान मिलता है 4 एच 10 से, फिर अल्काना 5 एन 12 से, 6 एन 14 से आदि।
अब आप अल्कानान के सामान्य सूत्र को वापस ले सकते हैं। अल्कानोव की एक पंक्ति में कार्बन परमाणुओं की संख्या हम ले लेंगे एन
, फिर हाइड्रोजन परमाणुओं की संख्या परिमाण होगी 2n + 2।
। नतीजतन, अल्कानोव की संरचना सामान्य सूत्र से मेल खाती है C n h 2n + 2.
इसलिए, इस तरह की परिभाषा का उपयोग किया जाता है:
अल्काना - हाइड्रोकार्बन जिनकी रचना सामान्य सूत्र द्वारा व्यक्त की जाती है C n h 2n + 2कहां है एन - कार्बन परमाणुओं की संख्या।
अल्कानन की संरचना
रासायनिक संरचना (अणुओं में परमाणुओं के यौगिकों का क्रम) सरलतम एल्केन्स - मीथेन, ईथेन और प्रोपेन - धारा 2 में दिखाए गए अपने संरचनात्मक सूत्रों को दिखाएं। इन सूत्रों से यह स्पष्ट है कि एल्केन में दो प्रकार के रासायनिक संबंध हैं:
सी-एस। तथा सी-एन।.
संचार सी-सी एक सहसंयोजक गैर-ध्रुवीय है। संचार सी - एच एक सहसंयोजक कमजोर है, क्योंकि कार्बन और हाइड्रोजन इलेक्ट्रोनबिलिटी (2.5 - कार्बन और 2.1 के लिए - हाइड्रोजन के लिए) के करीब हैं। कार्बन और हाइड्रोजन परमाणुओं के सामान्य इलेक्ट्रॉनिक जोड़े के कारण एलकनों में सहसंयोजक बंधन का गठन इलेक्ट्रॉनिक सूत्रों का उपयोग करके दिखाया जा सकता है:

इलेक्ट्रॉनिक और संरचनात्मक सूत्र प्रतिबिंबित करते हैं रासायनिक संरचनालेकिन विचारों के बारे में मत देना अणुओं की स्थानिक संरचनाजो पदार्थ के गुणों को काफी प्रभावित करता है।
स्थानिक संरचना। अंतरिक्ष में अणु परमाणुओं की सापेक्ष व्यवस्था इन परमाणुओं के परमाणु ऑर्बिटल्स (एओ) की दिशा पर निर्भर करती है। हाइड्रोकार्बन में, मुख्य भूमिका कार्बन ऑर्बिटल्स के स्थानिक अभिविन्यास द्वारा खेला जाता है, क्योंकि हाइड्रोजन परमाणु के गोलाकार 1 एस-एओ एक निश्चित अभिविन्यास से वंचित है।
बदले में कार्बन एओ की स्थानिक व्यवस्था हाइब्रिडाइजेशन (भाग I, धारा 4.3) के प्रकार पर निर्भर करती है। एल्केन में एक समृद्ध कार्बन परमाणु चार अन्य परमाणुओं से जुड़ा हुआ है। नतीजतन, इसका राज्य एसपी 3-हाइब्रिडाइजेशन (भाग I, खंड 4.3.1) से मेल खाता है। इस मामले में, चार एसपी 3-हाइब्रिड कार्बन एओ में से प्रत्येक अक्षीय (σ-) एस-एओ हाइड्रोजन से ओवरलैपिंग में शामिल है या एस-एच या सी-सी के साथ σ-बॉन्ड बनाने के लिए, एक और कार्बन परमाणु के एसपी 3 -एओ के साथ।

कार्बन के चार σ-बांड को 109 डिग्री सेल्सियस 28 के कोण पर अंतरिक्ष में निर्देशित किया जाता है, जो इलेक्ट्रॉनों के सबसे छोटे प्रतिकृति से मेल खाता है। इसलिए, एल्केन्स के सबसे सरल प्रतिनिधि का अणु - मीथेन सीएच 4 - एक टेट्राहेड्रॉन का रूप है , जिसके केंद्र में कार्बन परमाणु होते हैं, और शिखर पर - हाइड्रोजन परमाणु:

एन-सी-एन का वैलेंस कॉर्नर 109 है "। मीथेन की स्थानिक संरचना थोक (स्केल) और स्केललाइन मॉडल का उपयोग करके दिखाया जा सकता है।
रिकॉर्डिंग के लिए यह एक स्थानिक (स्टीरियोकेमिकल) सूत्र का उपयोग करना सुविधाजनक है।

अगले होमोलॉजिस्ट के अणु में - 2 एच 6 - दो टेट्राहेड्रल के साथ इथेन एसपी। 3 कार्बन मैट एक अधिक जटिल स्थानिक संरचना बनाते हैं:

2 से अधिक कार्बन परमाणुओं वाले अल्कानोव अणुओं के लिए, घुमावदार रूप विशेषताएं हैं। यह उदाहरण पर दिखाया जा सकता है एन-बूटन (वीआरएमएल मॉडल) या एन-पेंटा:

Isomeriya alkanov
- आइसोमेरियस - यौगिकों की उपस्थिति जिसमें एक ही संरचना (एक ही आण्विक सूत्र) है, लेकिन एक अलग संरचना है। ऐसे यौगिकों को बुलाया जाता है आइसोमार्स.
अणुओं में परमाणुओं के परिसर के क्रम में अंतर (यानी रासायनिक संरचना में) का नेतृत्व करता है संरचनात्मक आइसोमेरिया। संरचनात्मक आइसोमर की संरचना संरचनात्मक सूत्रों द्वारा प्रतिबिंबित होती है। कई अल्कानियों में, संरचनात्मक आइसोमेरिज्म सर्किट में 4 और अधिक कार्बन परमाणुओं की सामग्री होने पर प्रकट होता है, यानी भूटान से 4 एच 10 के साथ शुरू करना।
यदि एक ही संरचना और एक ही रासायनिक संरचना के अणुओं में, अंतरिक्ष में परमाणुओं की विभिन्न पारस्परिक व्यवस्था संभव है, तो मनाया जाता है स्थानिक आइसोमेरिज्म (स्टीरियोइस्मेरिया)। इस मामले में, संरचनात्मक सूत्रों का उपयोग पर्याप्त नहीं है और अणुओं या विशेष सूत्रों के मॉडल का उपयोग किया जाना चाहिए - स्टीरियोकेमिकल (स्थानिक) या प्रक्षेपण।
एथेन एच 3 सी-सी 3 से शुरू होने वाले एल्केन्स, विभिन्न स्थानिक रूपों में मौजूद हैं ( रचना) σ-लिंक सी-सी के इंट्रामोल्यूलर रोटेशन के कारण, और तथाकथित प्रकट होता है रोटरी (अनुरूपता) आइसोमेरिज्म.
इसके अलावा, यदि 4 अलग-अलग विकल्पों से जुड़े अणु में कार्बन परमाणु है, तो एक और प्रकार का स्थानिक आइसोमेरिज्म संभव है, जब दो स्टीरियोइंसर एक दूसरे से संबंधित वस्तु और इसकी दर्पण छवि के रूप में संबंधित होते हैं (जैसे कि बाएं हाथ सही को संदर्भित करता है )। अणुओं की संरचना में ऐसे मतभेदों को बुलाया जाता है ऑप्टिकल आइसोमेरिया.
संरचनात्मक आइसोमेरिया अल्कानोव
- संरचनात्मक आइसोमर - एक ही संरचना के यौगिक, बाध्यकारी परमाणुओं के लिए प्रक्रिया द्वारा विशेषता, यानी। अणुओं की रासायनिक संरचना।
अल्कानों की एक पंक्ति में संरचनात्मक आइसोमेरिज्म के प्रकटीकरण का कारण विभिन्न संरचनाओं के सर्किट बनाने के लिए कार्बन परमाणुओं का उपकरण है। इस प्रकार के संरचनात्मक आइसोमेरिज्म कहा जाता है आइसोमेरिया कार्बन कंकाल.
उदाहरण के लिए, अल्कान संरचना सी 4 एच 10 के रूप में मौजूद हो सकता है दो संरचनात्मक आइसोमर:

और alkan c 5 h 12 - फॉर्म में तीन संरचनात्मक आइसोमर, कार्बन श्रृंखला की संरचना द्वारा विशेषता:

अणुओं की संरचना में कार्बन परमाणुओं की संख्या में वृद्धि के साथ, श्रृंखला को ब्रांच करने की संभावनाएं, यानी आइसोमर की मात्रा कार्बन परमाणुओं की संख्या की सीमा बढ़ रही है।

संरचनात्मक आइसोमर भौतिक गुणों से प्रतिष्ठित हैं। अणुओं की कम घने पैकेजिंग के कारण एक शाखाबद्ध संरचना के साथ एल्केन और तदनुसार, छोटे इंटरमोल्यूलर इंटरैक्शन, तापमान को अपने अनियंत्रित आइसोमर की तुलना में उबालते हैं।
आइसोमर्स के संरचनात्मक सूत्रों के उत्पादन में, निम्नलिखित तकनीकें उपयोग करती हैं।
हाइड्रोकार्बन सबसे सरल कार्बनिक यौगिक हैं। वे कार्बन और हाइड्रोजन हैं। इन दो तत्वों के यौगिकों को सीमा हाइड्रोकार्बन या एल्केन कहा जाता है। उनकी रचना सामान्य रूप से सीएनएच 2 एन + 2 सूत्र के साथ एल्केन के लिए व्यक्त की जाती है, जहां एन कार्बन परमाणुओं की संख्या है।
के साथ संपर्क में
Odnoklassniki।
अल्काना - डेटा यौगिकों का अंतर्राष्ट्रीय नाम। इसके अलावा, इन यौगिकों को पैराफिन और संतृप्त हाइड्रोकार्बन कहा जाता है। अलकनन अणुओं में संचार सरल (या एकल) है। शेष वैलेंस हाइड्रोजन परमाणुओं से संतृप्त है। सभी एल्केन्स सीमा तक हाइड्रोजन के साथ संतृप्त हैं, इसके परमाणु एसपी 3 संकरण की स्थिति में हैं।
हाइड्रोकार्बन को सीमित करने की होमोलॉजिकल रेंज
 संतृप्त हाइड्रोकार्बन की समरूप पंक्ति में पहला मीथेन है। उसका फॉर्मूला CH4। अंत में हाइड्रोकार्बन सीमित करने के नाम पर है, यह एक विशिष्ट विशेषता है। इसके बाद, उपर्युक्त सूत्र के अनुसार, ईथेन - सी 2 एच 6 एक होमोलॉगस श्रृंखला, सी 3 एच 8 प्रोपेन, ब्यूटेन - सी 4 एच 10 में स्थित हैं।
संतृप्त हाइड्रोकार्बन की समरूप पंक्ति में पहला मीथेन है। उसका फॉर्मूला CH4। अंत में हाइड्रोकार्बन सीमित करने के नाम पर है, यह एक विशिष्ट विशेषता है। इसके बाद, उपर्युक्त सूत्र के अनुसार, ईथेन - सी 2 एच 6 एक होमोलॉगस श्रृंखला, सी 3 एच 8 प्रोपेन, ब्यूटेन - सी 4 एच 10 में स्थित हैं।
पांचवें अल्काना से यौगिकों के शीर्षक की होमोलॉगस श्रृंखला निम्नानुसार बनाई गई है: यूनानी संख्या अणु + अंत में हाइड्रोकार्बन परमाणुओं की संख्या का संकेत देती है। इसलिए, गार्सरी में, क्रमशः संख्या 5 - पंडे, पेंटन - सी 5 एच 12 भूटान के लिए जाता है। अगला - हेक्सेन सी 6 एच 14। हेप्टन - सी 7 एच 16, ऑक्टान - सी 8 एच 18, नॉनन - सी 9 एच 20, डीन - सी 10 एच 22, आदि
क्षारयों के भौतिक गुण होमोलॉगस श्रृंखला में स्पष्ट रूप से बदलते हैं: पिघलने बिंदु, उबलते बिंदु बढ़ता है, घनत्व बढ़ता है। सामान्य परिस्थितियों में मीथेन, ईथेन, प्रोपेन, ब्यूटेन, यानी लगभग 22 डिग्री गर्मी सेल्सियस के तापमान पर, हेक्सडेकन समावेशी - तरल पदार्थ, हेप्टेडकेन - ठोस पदार्थों के साथ, गैसों के साथ गैस हैं। भूटान से शुरू, क्षानण में आइसोमर हैं।
प्रतिबिंबित टेबल हैं अल्कानानों की समरूप पंक्ति में परिवर्तनजो स्पष्ट रूप से उनके भौतिक गुणों को दर्शाता है।
संतृप्त हाइड्रोकार्बन का नामकरण, उनके डेरिवेटिव्स
 यदि हाइड्रोजन परमाणु को हाइड्रोकार्बन अणु से अलग किया जाता है, तो मोनोवलेंट कण बनते हैं, जिन्हें रेडिकल (आर) कहा जाता है। कट्टरपंथी का नाम हाइड्रोकार्बन देता है, जिससे इस कट्टरपंथी का उत्पादन होता है, जबकि अंत-अंत में परिवर्तन होता है। उदाहरण के लिए, एक कट्टरपंथी मेथिल रेडिकल को हाइड्रोजन एटम के अलगाव के दौरान मीथेन से बनाया जाता है, ईथेन - एथिल, प्रोपेन से - प्रोपिल इत्यादि से।
यदि हाइड्रोजन परमाणु को हाइड्रोकार्बन अणु से अलग किया जाता है, तो मोनोवलेंट कण बनते हैं, जिन्हें रेडिकल (आर) कहा जाता है। कट्टरपंथी का नाम हाइड्रोकार्बन देता है, जिससे इस कट्टरपंथी का उत्पादन होता है, जबकि अंत-अंत में परिवर्तन होता है। उदाहरण के लिए, एक कट्टरपंथी मेथिल रेडिकल को हाइड्रोजन एटम के अलगाव के दौरान मीथेन से बनाया जाता है, ईथेन - एथिल, प्रोपेन से - प्रोपिल इत्यादि से।
रेडिकल भी अकार्बनिक यौगिकों का गठन किया जाता है। उदाहरण के लिए, एक नाइट्रिक एसिड पर, एक मोनोवलेंट कट्टरपंथी -नहीं 2 कट्टरपंथी प्राप्त करना संभव है, जिसे नाइट्रुप कहा जाता है।
जब अणु से अलग होता है एलकन दो हाइड्रोजन परमाणुओं को द्विपक्षीय कट्टरपंथियों द्वारा गठित किया जाता है, जिनके नाम संबंधित हाइड्रोकार्बन के नाम से भी गठित होते हैं, लेकिन अंत में परिवर्तन:
- ओरिन, इस घटना में कि हाइड्रोजन परमाणु एक कार्बन परमाणु से फाड़ा जाता है,
- इलेन, इस घटना में कि दो हाइड्रोजन परमाणु दो पड़ोसी कार्बन परमाणुओं से फाड़े गए हैं।
अल्काना: रासायनिक गुण
Alkanans की प्रतिक्रियाओं पर विचार करें। सभी एल्केन सामान्य रासायनिक गुणों में निहित हैं। ये पदार्थ कम सक्रिय हैं।
हाइड्रोकार्बन से जुड़े सभी ज्ञात प्रतिक्रियाओं को दो प्रकारों में विभाजित किया गया है:
- संचार एस-एच (एक उदाहरण एक प्रतिस्थापन प्रतिक्रिया है);
- संचार अंतर सी-सी (क्रैकिंग, व्यक्तिगत भागों का गठन)।
कट्टरपंथी गठन के क्षण में बहुत सक्रिय। अपने आप से, वे सेकंड के शेयर मौजूद हैं। रेडिकल आसानी से खुद के बीच प्रतिक्रिया में प्रवेश करते हैं। उनके अनपेक्षित इलेक्ट्रॉन एक नया सहसंयोजक कनेक्शन बनाते हैं। उदाहरण: सीएच 3 + सीएच 3 → सी 2 एच 6
रेडिकल आसानी से प्रतिक्रिया में प्रवेश करते हैं कार्बनिक अणुओं के साथ। वे या तो उनसे जुड़े हुए हैं, या उनसे अलग हो जाते हैं, जिसके परिणामस्वरूप नए रेडिकल दिखाई देते हैं, जो बदले में, अन्य अणुओं के साथ प्रतिक्रियाओं में प्रवेश कर सकते हैं। ऐसी श्रृंखला प्रतिक्रिया के साथ, मैक्रोमोल्यूल प्राप्त किए जाते हैं, जो केवल चेन ब्रेक (उदाहरण: दो रेडिकल का कनेक्शन) केवल बढ़ने के लिए बंद हो जाता है
मुक्त कणों की प्रतिक्रियाएं कई महत्वपूर्ण रासायनिक प्रक्रियाओं की व्याख्या करती हैं, जैसे कि:
- विस्फोट;
- ऑक्सीकरण;
- क्रैकिंग तेल;
- असंतृप्त यौगिकों का बहुलकरण।
 विस्तार रासायनिक गुणों पर विचार करें मीथेन के उदाहरण पर संतृप्त हाइड्रोकार्बन। हमने पहले ही अल्केन अणु की संरचना पर विचार किया है। कार्बन परमाणु एसपी 3 संकरण की स्थिति में मीथेन अणु में स्थित हैं, और एक टिकाऊ कनेक्शन बनता है। मीथेन गंध और रंगों का एक गैस आधार है। यह हवा से आसान है। पानी में थोड़ा विलायक।
विस्तार रासायनिक गुणों पर विचार करें मीथेन के उदाहरण पर संतृप्त हाइड्रोकार्बन। हमने पहले ही अल्केन अणु की संरचना पर विचार किया है। कार्बन परमाणु एसपी 3 संकरण की स्थिति में मीथेन अणु में स्थित हैं, और एक टिकाऊ कनेक्शन बनता है। मीथेन गंध और रंगों का एक गैस आधार है। यह हवा से आसान है। पानी में थोड़ा विलायक।
अल्काना जला सकता है। मीथेन एक नीली लौ के साथ जल रहा है। इस मामले में, प्रतिक्रिया का नतीजा कार्बन मोनोऑक्साइड और पानी होगा। जब हवा के साथ मिश्रित होता है, साथ ही ऑक्सीजन के मिश्रण में, विशेष रूप से यदि वॉल्यूम्स का अनुपात 1: 2 होता है, तो हाइड्रोकार्बन का डेटा विस्फोटक मिश्रण होता है, यही कारण है कि रोजमर्रा की जिंदगी और खानों में उपयोग के लिए यह बेहद खतरनाक है। यदि मीथेन पूरी तरह से जलता है, तो सूट का गठन किया जाता है। उद्योग में, यह इस प्रकार प्राप्त किया जाता है।
फॉर्मल्डेहाइड और मिथाइल अल्कोहल उत्प्रेरक की उपस्थिति में ऑक्सीकरण द्वारा मीथेन से प्राप्त किए जाते हैं। यदि मीथेन भारी गर्मी है, तो यह ch4 → सी + 2h2 सूत्र द्वारा विघटित करता है
मीथेन क्षय आप विशेष रूप से सुसज्जित भट्टियों में मध्यवर्ती उत्पाद को लागू कर सकते हैं। एक मध्यवर्ती उत्पाद एसिटिलीन होगा। प्रतिक्रिया फॉर्मूला 2ch4 → सी 2 एच 2 + 3 एच 2। मीथेन से एसिटिलीन की रिहाई उत्पादन लागत लगभग दो बार कम हो जाती है।
इसके अलावा, हाइड्रोजन मीथेन से भी प्राप्त किया जाता है, पानी वाष्प के साथ मीथेन के रूपांतरण का उत्पादन होता है। मीथेन के लिए विशेषता प्रतिस्थापन की प्रतिक्रियाएं हैं। तो, एक पारंपरिक तापमान पर, मीथेन अणु से हाइड्रोजन हलोजन (सीएल, बीआर) के प्रकाश में विस्थापित हो जाता है। इस प्रकार, पदार्थों का गठन किया जाता है, जिसे हलोजन डेरिवेटिव कहा जाता है। क्लोरीन परमाणुहाइड्रोकार्बन अणु में हाइड्रोजन परमाणुओं की जगह, विभिन्न कनेक्शन का मिश्रण तैयार करें।
इस तरह के मिश्रण में क्लोरोमेथेन (सीएच 3 सीएल या मिथाइल क्लोराइड), डिक्लोरोमेथेन (सीएच 2Cl2ili मेथिलिन क्लोराइड), ट्राइक्लोरोमेथेन (सीएचसीएल 3 या क्लोरोफॉर्म), टेट्रेक्लोरोमेथेन (सीसीएल 4 या कार्बन टेट्राक्लोराइड) हैं।
इनमें से कोई भी यौगिक मिश्रण से अलग किया जा सकता है। उत्पादन में, क्लोरोफॉर्म और टेट्राक्लोमेथेन आयात आयात किए जाते हैं, इस तथ्य के कारण कि वे कार्बनिक यौगिकों (वसा, रेजिन, रबड़) के सॉल्वैंट्स हैं। हलोजन डेरिवेटिव एक श्रृंखला मुक्त कट्टरपंथी तंत्र द्वारा गठित होते हैं।
प्रकाश क्लोरीन अणुओं को प्रभावित करता है, जिसके परिणामस्वरूप वे विघटित होते हैं अकार्बनिक कट्टरपंथी जो मीथेन अणु से एक इलेक्ट्रॉन के साथ हाइड्रोजन परमाणु को फाड़ते हैं। उसी समय, एचसीएल और मिथाइल का गठन किया जाता है। मिथाइल क्लोरीन अणु के साथ प्रतिक्रिया करता है, जिसके परिणामस्वरूप एक हलोजन व्युत्पन्न और क्लोरीन कट्टरपंथी होता है। इसके बाद, क्लोरीन कट्टरपंथी श्रृंखला प्रतिक्रिया जारी रखता है।
सामान्य तापमान पर, मीथेन में क्षार, एसिड, कई ऑक्सीडाइज़र के लिए पर्याप्त प्रतिरोध होता है। अपवाद - नाइट्रिक एसिड। इसके साथ प्रतिक्रिया नाइट्रोमेथेन और पानी बनती है।
मीथेन के लिए कनेक्शन प्रतिक्रियाएं विशेषता नहीं हैं, क्योंकि इसके अणु में सभी वैलेंस संतृप्त होते हैं।
जिन प्रतिक्रियाओं में हाइड्रोकार्बन न केवल सी-एच कनेक्शन के विभाजन के साथ, बल्कि सी-एस के टूटने के साथ भी हो सकते हैं। इस तरह के परिवर्तन उच्च तापमान की उपस्थिति में होते हैं। और उत्प्रेरक। ऐसी प्रतिक्रियाओं में डीहाइड्रोजनीकरण और क्रैकिंग शामिल हैं।
ऑक्सीकरण द्वारा संतृप्त हाइड्रोकार्बन में, एसिड प्राप्त होते हैं - एसिटिक (ब्यूटेन से), फैटी एसिड (पैराफिन से)।
मीथेन प्राप्त करना
 प्रकृति मीथेन में व्यापक व्यापक। यह दहनशील प्राकृतिक और कृत्रिम गैसों के बहुमत का मुख्य घटक है। यह दलदल के नीचे से, खानों में कोयला जलाशयों से अलग है। प्राकृतिक गैसों (जो पेट्रोलियम क्षेत्रों के संबंधित गैसों में बहुत ध्यान देने योग्य है) न केवल मीथेन, बल्कि अन्य एल्केन भी होते हैं। इन पदार्थों का उपयोग अलग-अलग है। उन्हें विभिन्न उद्योगों में, चिकित्सा और प्रौद्योगिकी में ईंधन के रूप में उपयोग किया जाता है।
प्रकृति मीथेन में व्यापक व्यापक। यह दहनशील प्राकृतिक और कृत्रिम गैसों के बहुमत का मुख्य घटक है। यह दलदल के नीचे से, खानों में कोयला जलाशयों से अलग है। प्राकृतिक गैसों (जो पेट्रोलियम क्षेत्रों के संबंधित गैसों में बहुत ध्यान देने योग्य है) न केवल मीथेन, बल्कि अन्य एल्केन भी होते हैं। इन पदार्थों का उपयोग अलग-अलग है। उन्हें विभिन्न उद्योगों में, चिकित्सा और प्रौद्योगिकी में ईंधन के रूप में उपयोग किया जाता है।
प्रयोगशाला की स्थिति के तहत, इस गैस को अलग किया जाता है जब मिश्रण सोडियम एसीटेट + सोडियम हाइड्रॉक्साइड द्वारा गर्म किया जाता है, साथ ही एल्यूमीनियम और पानी के कार्बाइड की प्रतिक्रिया भी होती है। यह भी सरल पदार्थों से मीथेन प्राप्त किया जाता है। इस अनिवार्य स्थितियों के लिए हीटिंग और उत्प्रेरक हैं। औद्योगिक महत्व जल वाष्प के आधार पर मीथेन संश्लेषण प्राप्त कर रहा है।
मीथेन और इसके होमोलॉग को क्षारीय के साथ उपयुक्त कार्बनिक एसिड के नमक की गणना करके प्राप्त किया जा सकता है। अलकनान प्राप्त करने का एक और तरीका वुरज़ की प्रतिक्रिया है, जिस पर धातु सोडियम के साथ मोनोगोलोजेनिक उत्पादन गर्म किया जाता है।