दहनशील गैसों का दहन तापमान। गैस ईंधन जलते समय मिश्रण और दहन। गैस जलने के तरीके
8.1। रिएक्शन जल रहा है
जी ओ आर ई एन ई - ऑक्सीजन के साथ दहनशील घटकों के यौगिकों की उच्च बहती रासायनिक प्रतिक्रिया, गहन गर्मी की रिलीज और दहन उत्पादों के तापमान में तेज वृद्धि के साथ। दहन प्रतिक्रियाओं को तथाकथित द्वारा वर्णित किया गया है। Stoichiometric समीकरण गुणात्मक रूप से और मात्रात्मक रूप से प्रतिक्रिया और उसके पदार्थ से परिणामस्वरूप (दहनशील मिश्रण की stoichiometric संरचना (ग्रीक से। Stoicheion आधार, तत्व और ग्रीक है। मेट्रीओ - मैं मापता हूं) - मिश्रण की संरचना जिसमें ऑक्सीडाइज़र बिल्कुल ईंधन के पूर्ण ऑक्सीकरण के लिए जितना आवश्यक हो)। किसी भी हाइड्रोकार्बन के दहन का सामान्य समीकरण
पूर्वगामी को ध्यान में रखते हुए, हमें मिलता है। उपर्युक्त आवश्यकताओं के प्रकाश में, इमारत में व्यक्तिगत प्रकार के आवास की दिशा में निर्देशित वायु प्रवाह निम्नानुसार है। अपार्टमेंट टाइप ए - जहां बाथरूम और शौचालय एक कमरा, एक बाथरूम और शौचालय अपार्टमेंट - निजी कमरे हैं।
प्राकृतिक गैस प्राकृतिक भूमिगत जमा से आता है। इसे सब्जी या पशु कचरे के दीर्घकालिक परिवर्तन से कच्चे तेल के रूप में बनाया गया था। यह आमतौर पर वहां और कच्चे तेल पाता है। मुख्य घटक प्राकृतिक गैस। यह दहनशील गैस का मीथेन है, इसके अलावा, अन्य दहनशील गैसों, गैसोलीन और कार्बन डाइऑक्साइड, हाइड्रोजन सल्फाइड की एक छोटी राशि है। हम दो प्रकार की प्राकृतिक गैस को अलग करते हैं: गीले और सूखे। सूखे में कुछ गैसोलीन होते हैं, यह बहुत साफ होता है - पतला करना आसान होता है। गैसोलीन को अलग करने, गैसोलीन को अलग करने से पहले गैस को नमी से अवगत कराया जाता है सक्रिय कोयलाजो बड़े अवशोषक गुणों के साथ गैसोलीन बंद हो जाता है।
सी एम एच एन + (एम + एन / 4) ओ 2 \u003d एमसीओ 2 + (एन / 2) एच 2 ओ + क्यू (8.1)
जहां एम, एन अणु में कार्बन और हाइड्रोजन परमाणुओं की संख्या है; क्यू प्रतिक्रिया का थर्मल प्रभाव, या दहन की गर्मी है।
कुछ गैसों की दहन प्रतिक्रिया तालिका में दिखाए जाते हैं। 8.1। ये समीकरण संतुलित हैं, और प्रतिक्रियाओं की गति या रासायनिक परिवर्तनों की तंत्र का न्याय करना असंभव है।
तालिका 8.1। दहन प्रतिक्रियाएं और सूखी गैसों की गर्मी दहन (0 डिग्री सेल्सियस और 101.3 केपीए पर)
गैसोलीन का अलगाव गैस संपीड़न के साथ संघनन द्वारा होता है, इसके बाद शीतलन होता है। प्राकृतिक गैस का कैलोरीफ मूल्य इसकी संरचना के आधार पर महत्वपूर्ण रूप से भिन्न होता है। ठोस या तरल ईंधन का कैलोरीफ मूल्य गर्मी की मात्रा है जो कब खड़ी होती है सामान्य ईंधन रोशनी 1 किलो। हालांकि, यदि आप गैस ईंधन के कैलोरीफ मूल्य को मापना चाहते हैं, तो आपको इस ईंधन के 1 एम 3 को पूरी तरह जला देना होगा। प्राकृतिक गैस मुख्य रूप से ईंधन गैस के रूप में उपयोग की जाती है और शहरों और औद्योगिक केंद्रों में गैस पाइपलाइनों में लंबी दूरी पर भी भेजी जाती है।
| गैस | जलने की प्रतिक्रिया | गर्मी दहन | |||||
|---|---|---|---|---|---|---|---|
| दाढ़ी, केजे / केएमओएल | मास, केजे / किग्रा | वॉल्यूमनी, केजे / एम 3 | |||||
| उच्चतर | खो गया | उच्चतर | खो गया | उच्चतर | खो गया | ||
| हाइड्रोजन | एच 2 + 0.5o 2 \u003d एच 2 0 | 286,06 | 242,90 | 141 900 | 120 080 | 12 750 | 10 790 |
| कार्बन ऑक्साइड | सीओ + 0.5 ओ 2 \u003d सीओ 2 | 283,17 | 283,17 | 10 090 | 10 090 | 12 640 | 12 640 |
| मीथेन | सीएच 4 + 2 ओ 2 \u003d सीओ 2 + 2 एच 2 ओ | 880,90 | 800,90 | 55 546 | 49 933 | 39 820 | 35 880 |
| एटैन | सी 2 एच 6 + 0.5o 2 \u003d 2CO 2 + 3 एच 2 ओ | 1560,90 | 1425,70 | 52 019 | 47 415 | 70 310 | 64 360 |
| प्रोपेन | सी 3 एच 8 + 5 एच 2 ओ \u003d 3CO 2 + 4H 2 ओ | 2221,40 | 2041,40 | 50 385 | 46 302 | 101 210 | 93 180 |
| एन-बोधिन | 2880,40 | 2655,00 | 51 344 | 47 327 | 133 800 | 123 570 | |
| आइसोबुटन | सी 4 एच 10 + 6,5O 2 \u003d 4CO 2 + 5H 2 ओ | 2873,50 | 2648,30 | 51 222 | 47 208 | 132 960 | 122 780 |
| एन-पेंटन | सी 5 एच 12 + 8 ओ 2 \u003d 5CO 2 + 6H 2 ओ | 3539,10 | 3274,40 | 49 052 | 45 383 | 169 270 | 156 630 |
| ईथीलीन | सी 2 एच 4 + 3 ओ 2 \u003d 2CO 2 + 2H 2 ओ | 1412,00 | 1333,50 | 50 341 | 47 540 | 63 039 | 59 532 |
| प्रोपिलीन | सी 3 एच 6 + 4,5O 2 \u003d 3CO 2 + 3H 2 ओ | 2059,50 | 1937,40 | 48 944 | 46 042 | 91 945 | 88 493 |
| बुटीलीन | सी 4 एच 8 + 6 ओ 2 \u003d 4CO 2 + 4H 2 ओ | 2720,00 | 2549,70 | 48 487 | 45 450 | 121 434 | 113 830 |
टी ई एन ओ वी ओ ई एफ एफ ф ई (दहन की गर्मी) क्यू सामान्य शारीरिक परिस्थितियों में 1 किमी, 1 किलो या 1 मीटर 3 गैस के पूर्ण दहन में जारी गर्मी की मात्रा है। दहन की उच्चतम क्यूसी और कम क्यूएन गर्मी: दहन की उच्चतम गर्मी में जलने की प्रक्रिया में जल वाष्प के संघनन की गर्मी शामिल होती है (वास्तविकता में गैस जलते समय, पानी के वाष्प संघनित नहीं होते हैं, लेकिन अन्य दहन उत्पादों के साथ हटा दिए जाते हैं )। आम तौर पर, तकनीकी गणना आमतौर पर जल वाष्प (≈ 2400 केजे / किग्रा) के संघनन की गर्मी को ध्यान में रखे बिना दहन की सबसे कम गर्मी का नेतृत्व करती है।
विशेष जलाने वालों के साथ प्राकृतिक गैस जल गई। हवा के साथ मिश्रण में यह विस्फोट होता है। गैस या कोक प्लांट से गैस की तुलना में यह बहुत कम विषाक्त है, क्योंकि इसमें कार्बन मोनोऑक्साइड नहीं होता है। लाइट गैस एक गैस है जो कोयले के शुष्क आसवन के साथ प्राप्त की जाती है, यानी बिना हवा के हीटिंग। आसुत गैस अपने कमीशन से पहले कई मूल्यवान additives, जैसे बेंजीन और इसके डेरिवेटिव से शुद्ध किया जाता है; और हानिकारक प्रदूषक, जैसे हाइड्रोजन सल्फाइड और अन्य सल्फर यौगिकों; ब्लू नाफ्थालेन, आदि बाकी गैर-दहनशील गैस हैं: कार्बन डाइऑक्साइड और नाइट्रोजन।
प्रकाश गैस संरचना परिवर्तनीय है और निर्माण की विधि पर निर्भर करता है; गैस अक्सर अन्य दहनशील गैसों के साथ मिश्रित होती है। प्रकाश गैस से दूषित हवा में होना बहुत खतरनाक है; यहां तक \u200b\u200bकि छोटी मात्रा में गैस विषाक्तता का कारण बनती है। यदि आप हवा में हवा की गंध महसूस करते हैं, तो तुरंत खिड़कियां खोलें, एक एयरफ्लो बनाएं, और फिर गैस पाइपलाइनों की प्रसंस्करण शुरू करें। इग्निशन एक ऐसे स्थान पर भी मेल खाता है जहां हवा हल्की गैस से अधिक दूषित होती है, खतरनाक है, क्योंकि हवा में इग्निशन और विस्फोट के लिए पर्याप्त गैस हो सकती है।
दहन की सबसे कम गर्मी पर गणना की गई दक्षता, औपचारिक रूप से अधिक है, लेकिन पानी के वाष्पों के संघनन की गर्मी काफी बड़ी है, और इसका उपयोग उचित से अधिक है। इसकी पुष्टि संपर्क गर्मी एक्सचेंजर्स की हीटिंग तकनीक में एक सक्रिय अनुप्रयोग है, जो डिजाइन में बहुत विविध है।
दहनशील गैसों के मिश्रण के लिए, गैसों के उच्चतम (और निम्न) गर्मी दहन अनुपात द्वारा निर्धारित किया जाता है
परिणामस्वरूप सामग्री के साथ हम क्या करेंगे
लाइट गैस को तथाकथित से लैस बर्नर के साथ दीपक में जला दिया जाता है। उज्जवल लैंप। गरमागरम लैंप दुर्लभ धातु मलबे के साथ गर्भवती सूती कपड़े से बने होते हैं। कपड़ों में निहित इन धातु कण जलती हुई गैस चमक रहे हैं। इस प्रकार, लौ लौ मात्रा पर निर्भर करता है ठोसउदाहरण के लिए, ईथिलीन में कोयला, जो लौ और रोशनी में जला नहीं सकता है, जो मीथेन पर लागू नहीं होता है। गरमागरम लैंप बहुत नाजुक हैं, वे केवल एक विशेष हैंडल के साथ उपयोग किया जा सकता है।
Q \u003d r 1 q 1 + r 2 q 2 + ... + r n q n (8.2)
जहां आर 1, आर 2, ..., आर एन मिश्रण में शामिल घटकों के थोक (मोलर, बड़े पैमाने पर) अंश है; प्रश्न 1, क्यू 2, ..., क्यू एन - घटकों के गर्मी दहन।
तालिका का लाभ उठाते हुए। 8.1, दहन की उच्चतम और निम्न गर्मी, केजे / एम 3, जटिल गैस निम्नलिखित सूत्रों द्वारा निर्धारित की जा सकती है:
क्यू \u003d 127.5 एच 2 + 126.4 सी + 3 9 8 सी 4 + 703 सी 2 एच 6 + 1012 सी 8 एच 8 + 1338 सी 4 एच 10 + 1329 सी 4 एच 10 +
+ 1693 सी 5 एच 12 + 630 सी 2 एच 4 + 9 1 9 सी 3 एच 6 +1214 सी 4 एच 8 (8.3)
हवा को चमकदार की एक परत के माध्यम से हवा उड़ाने से प्राप्त किया जाता है ठोस ईंधन, पेड़, पीट, लिग्नाइट या पत्थर या कोक। कार्बन डाइऑक्साइड के उत्पादन के लिए पर्याप्त हवा लागू करते समय ईंधन चालू होता है; यह पूरी तरह से जलता है। यदि हम वायु आपूर्ति को कम करते हैं, तो अपूर्ण दहन होता है, जिससे ज्वलनशील कार्बन मोनोऑक्साइड के गठन का कारण बन जाएगा। चट्टान। इस प्रक्रिया को ठोस ईंधन गैसीफिकेशन कहा जाता है। वायु गैस के लिए ठोस ईंधन का गैसीकरण तथाकथित में किया जाता है।
कोक आमतौर पर ठोस जेनरेटर में उपयोग किया जाता है। कभी-कभी ब्राउन कोयले, पत्थर कोयले या पीट। इसका उपयोग मुख्य रूप से आंतरिक दहन इंजन के लिए औद्योगिक भट्टियों को फायर करने और हल्की गैस के लिए अशुद्धता के रूप में उपयोग किया जाता है। पानी - गैस। कार्बन मोनोऑक्साइड और हाइड्रोजन का मिश्रण। यह एक चमकते कोक पर जल वाष्प की क्रिया द्वारा गठित किया जाता है, इस तरह से जनरेटर पहले हवा डालता है, कोक कोक सफेद आग में जाता है, और फिर प्रशंसकों को चालू करने के बाद जल वाष्प में प्रवेश करता है।
क्यू एच \u003d 107.9 एच \u200b\u200b2 + 126.4 सीओ + 358,8 सीएच 4 + 643 सी 2 एच 6 + 931.8 सी 8 एच 8 + 1235 सी 4 एच 10 + 1227 सी 4 एच 10 +
+ 1566 सी 5 एच 12 + 5 9 5 सी 2 एच 4 + 884 सी 8 एच 6 + 1138 सी 4 एच 8 (8.4)
जहां एच 2, सीओ, सीएच 4, आदि - गैस ईंधन में व्यक्तिगत घटकों की सामग्री, के बारे में। %।
दहन प्रक्रिया फॉर्मूला (8.1) के अनुसार अधिक कठिन हो जाती है, क्योंकि चेन की शाखा के साथ, वे मध्यवर्ती स्थिर यौगिकों के गठन से टूट जाते हैं, जो उच्च तापमान पर आगे रूपांतरण से गुजरते हैं। एक पर्याप्त ऑक्सीजन एकाग्रता के साथ, अंतिम उत्पाद बनते हैं: जल वाष्प एन 2 ओ और कार्बन डाइऑक्साइड सीओ 2। ऑक्सीकरण एजेंट की कमी के साथ-साथ प्रतिक्रिया क्षेत्र द्वारा ठंडा होने पर, इंटरमीडिएट कनेक्शन स्थिर हो सकते हैं और पर्यावरण में प्रवेश कर सकते हैं।
गर्म लॉन्च के दौरान, एक गैस जनरेटर का गठन होता है - एक ठंडा रन के दौरान - जल गैस। जब जोड़े पेश किए जाते हैं, तो कोक जेनरेटर में ठंडा किया जाता है, और इसलिए, ठंड शुरू होने के बाद, जनरेटर एक गर्म पाठ्यक्रम में स्विच करता है, और फिर वैकल्पिक रूप से गुजरता है। एकत्रित गैसों को अलग से एकत्रित किया जाता है या एक साथ मिश्रित किया जाता है। पानी की गैस अलग-अलग एकत्रित, हीटिंग उद्देश्यों के लिए बहुत महंगा है, लेकिन उत्पादन के लिए उपयुक्त है उच्च तापमान। इसकी लौ हल्की गैस की तुलना में गर्म है, इसलिए इसका उपयोग वेल्डिंग बॉयलर, पाइप, सोल्डरिंग, जलन और पिघलने वाली धातुओं के लिए किया जाता है।
गर्म और ठंडे गैसों का मिश्रण ईंधन गैस के रूप में उपयोग किया जाता है। एसिटिलीन एक असंतृप्त हाइड्रोकार्बन है, क्योंकि यह अभी भी हाइड्रोजन जोड़ सकता है। यह कार्बाइड के लिए पानी की कार्रवाई द्वारा हासिल किया जाता है। यह उच्च गुणवत्ता वाला ईंधन है और ऑक्सीजन में जलते समय उच्च तापमान पैदा करता है। इसका उपयोग धातु वेल्डिंग के लिए, प्रकाश व्यवस्था के लिए, शायद ही कभी हीटिंग के लिए किया जाता है। इसका उत्पादन होता है प्वाइंट वेल्डिंग या विशेष उपकरण में रोशनी - इनवर्टर या डायटोमेसियस एसीटोन से भरे स्टील सिलेंडरों में एक संपीड़ित रूप में खरीदा गया।
गर्मी उत्पादन तीव्रता और तापमान वृद्धि सक्रिय कण प्रतिक्रिया प्रणाली में वृद्धि की ओर ले जाती है। लगभग सभी दहन प्रक्रियाओं के लिए श्रृंखला प्रतिक्रिया और तापमान के इस तरह के हस्तक्षेप ने श्रृंखला-थर्मल विस्फोट की अवधारणा की शुरूआत की है - रासायनिक दहन प्रतिक्रियाओं के पास एक श्रृंखला चरित्र है, और गर्मी और तापमान की रिहाई के कारण उनका त्वरण होता है प्रतिक्रिया प्रणाली में वृद्धि।
बंजेन बर्नर का आविष्कार ईंधन के रूप में गैसों के प्रचार के लिए बहुत ध्यान देने योग्य था। इस बर्नर का व्यापक रूप से उपयोग किया जाता है: इसका उपयोग सभी घरेलू उपकरणों, प्रयोगशालाओं में और यहां तक \u200b\u200bकि उद्योग में भी किया जाता है। लकड़ी लकड़ी की लकड़ी के लिए मुख्य ईंधन है। यह घर हीटिंग के लिए आदर्श है। लेकिन क्या आप जानते हैं कि पेड़ वास्तव में जला नहीं है? क्या आप फायरप्लेस में जलने वाले जंगलों की सफाई करते समय प्रक्रियाओं को जानते हैं? क्या आप जानते हैं कि फायरप्लेस में गर्म आग क्यों नृत्य कर रहा है? यदि आपने किसी भी प्रश्न को "पता नहीं" का उत्तर दिया है, तो आपको इस प्रविष्टि को पढ़ने की आवश्यकता है।
एक सजातीय मिश्रण में रासायनिक प्रतिक्रिया की दर प्रतिक्रियाशील पदार्थों की सांद्रता के उत्पाद के आनुपातिक है:
w \u003d kc 1 c 2 (8.5)
जहां सी 1 और सी 2 प्रतिक्रियाशील घटकों, केएमओएल / एम 3 की एकाग्रता है; प्रतिक्रिया प्रतिक्रियाओं और तापमान की प्रकृति के आधार पर एक प्रतिक्रिया दर स्थिर है।
प्रतिक्रियाशीलों की गैस एकाग्रता को जलाने पर अपरिवर्तित माना जा सकता है, क्योंकि जलती हुई ज़ोन में अस्पष्ट संरचना के ताजा घटकों का निरंतर प्रवाह होता है।
कोई भी जिसकी फायरप्लेस है, वह जानता है कि इसका क्या उपयोग करना है, आपको इसे जला देना होगा। अपवादों के अलावा, जो कचरा बाल्टी में और कचरा की तरह जला, फायरप्लेस में अधिकांश धूम्रपान। चाहे लकड़ी के तख्ते के रूप में या ब्रिकेट्स के रूप में, लकड़ी लकड़ी है। फिर लिविंग रूम में हमारे पास एक बॉयलर रूम है, दीवारों पर, काले पट्टिका से भरा हुआ है, और फायरप्लेस में कार्बन और कालिख से भरा है। क्या आप जानते हैं कि लकड़ी जलती है? आग और पेड़ की तुलना में एक ब्रिकेट अधिक निर्दयता से क्यों है?
लकड़ी की तुलना में 100% प्राकृतिक और नवीकरणीय सामग्री है, उदाहरण के लिए, कोयले या गैस के साथ, जिनके प्राकृतिक संसाधन हर दिन कम हो जाते हैं। पेड़ जल रहा है, क्योंकि हमारे पूर्वजों ने आग लगाई, यह स्वच्छ और पर्यावरण अनुकूल है। ऐश, जो जलने की सामान्य प्रक्रिया के बाद बनी हुई है, वह लवण और खनिज है जो विकास अवधि के दौरान मिट्टी से निकाला गया है। फायरप्लेस की राख जिसमें जंगल जला दिया जाता है, आप सफलतापूर्वक कंपोस्टर में डाल सकते हैं या सिर्फ एक घास के मैदान या लॉन में डाल सकते हैं।
प्रतिक्रिया दर स्थिर (Arrhenius समीकरण के अनुसार):
K \u003d k 0 e -e / rt (8.6)
जहां के 0 बायोमेट्रिक सजातीय मिश्रण, ≈1.0 के लिए लिया गया पूर्व-घातीय कारक है; ई - सक्रियण ऊर्जा, केजे / केएमओएल; आर एक सार्वभौमिक गैस स्थिर है, जे / (किलो करने के लिए); टी - पूर्ण तापमान, (डिग्री सेल्सियस) करने के लिए; ई प्राकृतिक लॉगरिदम का आधार है।
0 के लिए पूर्व-घातीय कारक को अणुओं के टक्कर की समापन की पूर्णता के रूप में व्याख्या किया जा सकता है, और ई - अणुओं के बंधन बांड की न्यूनतम ऊर्जा और सक्रिय कणों के गठन की न्यूनतम ऊर्जा के रूप में, जो टकराव की प्रभावशीलता सुनिश्चित करता है। सामान्य दहनशील मिश्रणों के लिए, यह (80 ÷ 150) 10 3 केजे / kmol के भीतर ढेर।
वन जीवन तब शुरू होता है जब एक छोटा बीज गिरता है गीली मिट्टी और जड़ें चला जाता है। बीज तब एक पेड़ को विकसित करना शुरू कर रहे हैं जो कई दसियों या कई सौ साल पहले बढ़ सकता है बड़े आकार। अक्सर, हालांकि, एक दर्जन या इतने दशकों के माध्यम से, इस तरह के भिखारी, आदमी और लकड़ी चुपचाप बढ़ते हैं। फिर वह शाखाओं को काटता है, पेड़ को टुकड़ों में काटता है और इसे शाम को या लकड़ी की संरचना पर ले जाता है। यहां है लकड़ी के लॉगछोटे टुकड़ों में कटा हुआ, कटा हुआ और रखी गई।
शायद ही कभी, कटौती के ढेर, कटा हुआ जंगल निजी घरों के बगीचों में पाया जा सकता है। वे विशेष रूप से प्रशिक्षित जंगलों में स्थित हैं। फिलहाल, वह है, ढेर में एक गीला, कटा हुआ लकड़ी डालने के समय लकड़ी को जलाने की प्रक्रिया शुरू होती है। पहला चरण शुरू होता है, जो लकड़ी सूखता है। हां, आप गीले पेड़ से जला सकते हैं, लेकिन फिर अंदर चिमनी पाइप हमारे पास बहुत सारा पानी है, लकड़ी की ऊर्जा दक्षता खराब है, और चिमनी या भट्टी सूट और आर्द्रता के साथ स्नेहक है, और धूम्रपान दहन के दौरान बनाई गई है।
समीकरण (8.6) उस गति से पता चलता है रसायनिक प्रतिक्रिया बढ़ते तापमान के साथ मूल रूप से बढ़ता है: उदाहरण के लिए, दहन प्रतिक्रिया की गति में 500 से 1000 तक तापमान में वृद्धि 2 10 4 ÷ 5 10 8 गुना (सक्रियण ऊर्जा के आधार पर)।
दहन प्रतिक्रियाओं की दर उनके चेन चरित्र को प्रभावित करती है। प्रारंभ में उत्पन्न परमाणु और कट्टरपंथी स्रोत पदार्थों और साथ में यौगिकों में प्रवेश करते हैं, जो कि प्रतिक्रियाओं की एक ही श्रृंखला को दोहराते हुए सीमित उत्पादों और नए कणों का निर्माण करते हैं। ऐसे कणों की बढ़ती पीढ़ी रासायनिक प्रतिक्रियाओं के "त्वरण" की ओर ले जाती है - वास्तव में पूरे मिश्रण को विस्फोट करती है।
अधिक लकड़ी को निचोड़ने के लिए, हमें इसे अच्छी तरह से सूखना चाहिए। लकड़ी में इष्टतम नमी सामग्री 10% से कम है, लेकिन इसे केवल सुखाने वाले कमरे में ही प्राप्त किया जा सकता है, जो घर पर अटूट है। अक्सर लकड़ी सूख जाती है खुली हवा में, जंगल में या ढेर के साथ कवर किया गया। फिर, लगभग दो साल की सुखाने, हम लकड़ी की खुराक के साथ एक दर्जन प्रतिशत के साथ नीचे आ सकते हैं।
अगला कदम सूखे लकड़ी को फायरप्लेस में लोड करना है। आग उजागर करने के लिए, आपको फायरप्लेस में आग लगाना चाहिए। हम ग्रिल के लिए लकड़ी और कागज या आग के छोटे सूखे टुकड़ों का उपयोग करते हैं। और यहाँ सबसे अच्छा है। इससे इस तथ्य की ओर जाता है कि शेष लकड़ी वाष्पित हो जाती है और पूरी तरह से लकड़ी के टुकड़े सूख जाती है। तापमान में और वृद्धि प्रक्रिया को दहन प्रक्रिया के दूसरे चरण में जाने का कारण बनती है। यह degassing चरण है, जो लगभग 100 डिग्री सेल्सियस - 150 डिग्री सेल्सियस के तापमान पर होता है: लकड़ी की लकड़ी और थर्मल अपघटन की लकड़ी और degassing लकड़ी और गैसों का उत्पादन शुरू होता है, जिसमें लकड़ी का उत्पादन होता है।
हाइड्रोकार्बन का उच्च तापमान दहन जटिल है और परमाणुओं और कट्टरपंथियों के रूप में सक्रिय कणों के निर्माण के साथ-साथ मध्यवर्ती आणविक यौगिकों के रूप में भी जुड़ा हुआ है। उदाहरण के तौर पर, सबसे सरल हाइड्रोकार्बन की दहन प्रतिक्रियाएं - मीथेन दिए जाते हैं:
- N + o 2 -\u003e वह + ओ
सीएच 4 + यह -\u003e सी 3 + एच 2 ओ
सीएच 4 + ओ -\u003e सीएच 2 + एन 2 ओ - Ch 3 + o 2 -\u003e NSNO + वह
सीएच 2 + ओ 2 -\u003e एनएसएनओ + ओ - Nso + he -\u003e nso + n 2
एनएनओ + ओ -\u003e सीओ + एन 2 ओ
NSO + O 2 -\u003e CO + O + - सीओ + ओ -\u003e सीओ 2
सीओ + आईटी -\u003e सीओ 2 + एन
इकाई चक्र का नतीजा:
हां, हां, 80% लकड़ी में अस्थिर भाग और 20% ठोस भाग होता है। बैट ऐश, कार्बन मोनोऑक्साइड, हाइड्रोजन। इसका हिस्सा लकड़ी की राख थी। फिर हम जो गैसों को देखते हैं उसे जलाने की प्रक्रिया एक लौ है, और ऐसा लगता है कि लकड़ी जलती है, और इसलिए यह वास्तव में गैसों को जलाती है जो लकड़ी को उच्च तापमान के प्रभाव में नष्ट कर देती हैं। "जलती हुई" लकड़ी के चरण उस तापमान पर निर्भर करते हैं जिसमें यह स्थित है।
ज्वलनशील सामग्री आग का एक स्रोत है, लेकिन क्या कोई वायु आपूर्ति है?
जलने की प्रक्रिया के बारे में बात करने के लिए, तीन स्थितियों को किया जाना चाहिए। यह ज्वलनशील होना चाहिए, वहां वायु आपूर्ति होनी चाहिए, और आग का स्रोत होना चाहिए। फायरिंग के दौरान, हम आमतौर पर अधिकतम वायु प्रवाह सेट करते हैं। फिर आग जलती है, लेकिन अप्रभावी है जब हमारे पास ऑक्सीजन की अधिकता होती है, जो फायरप्लेस को ठंडा करती है और लकड़ी को जलाती है, जो तापमान को कम करती है और चिप्स गैसों को धीमा कर देती है। तार्किक रूप से सोच, लकड़ी के बर्न के छोटे टुकड़ों के तुरंत बाद, विभाजन को बहुत अधिक हवा की आपूर्ति को सीमित करने के लिए थोड़ा बंद होना चाहिए।
2 एसएच 4 + 4 ओ 2 -\u003e 2 + 2 + 4 एन 2
8.2। जलन की गणना
दहन के लिए ऑक्सीजन हवा से उसके रूप में आता है अंग। गणना के लिए, यह माना जाता है कि शुष्क हवा की वॉल्यूमेट्रिक संरचना निम्नानुसार है:
ऑक्सीजन - 21.0%, नाइट्रोजन - 79.0%।
प्रदान की गई जानकारी के मुताबिक, ऑक्सीजन का 1 मीटर 3 100/21 \u003d 4.76 मीटर 3 हवा में निहित है, या नाइट्रोजन के 79/21 \u003d 3.76 मीटर 3 के लिए ऑक्सीजन खातों के 1 मीटर 3 में निहित है। यह देखते हुए कि सामान्य परिस्थितियों में 1 किलोमीटर गैस में 22.4 लीटर की क्षमता है, हवा में किसी भी हाइड्रोकार्बन के दहन प्रतिक्रिया (समीकरण 8.1 देखें) को सामान्यीकृत रूप में लिखा जा सकता है:
सी एम एच एन + (टी + एन / 4) (ओ 2 + 3.76 एन 2) \u003d टीसीओ 2 + (एन / 2) एच 2 ओ + (टी + एन / 4) 3.76 एन 2
विभिन्न गैसों के जलने के दौरान ऑक्सीजन और हवा की आवश्यकताओं, उपरोक्त दहन प्रतिक्रियाओं के अनुसार गिना जाता है, तालिका में प्रस्तुत किया जाता है। 8.2।
तालिका 8.2। सूखे ऑक्सीजन और वायु, एम 3, और 1 मीटर 3 गैस जलते समय गैस दहन उत्पादों की मात्रा के लिए सैद्धांतिक आवश्यकता
| गैस | सैद्धांतिक आवश्यकता | दहन के उत्पाद | ||||
|---|---|---|---|---|---|---|
| ऑक्सीजन | वायु | कार्बन डाइऑक्साइड | जल समृद्धि | नाइट्रोजन | संपूर्ण | |
| हाइड्रोजन एच 2। | 0,5 | 2,38 | – | 1,0 | 1,88 | 2,88 |
| कार्बन ऑक्साइड कं | 0,5 | 2,38 | 1,0 | – | 1,88 | 2,88 |
| मीथेन सी 4। | 2,0 | 9,52 | 1,0 | 2,0 | 7,52 | 10,52 |
| एथन सी 2 एच 6 | 3,5 | 16,66 | 2,0 | 3,0 | 13,16 | 18,16 |
| प्रोपेन सी 3 एच 8 | 5,0 | 23,80 | 3,0 | 4,0 | 18,80 | 25,80 |
| ब्यूटेन सी 4 एच 10 | 6,5 | 30,94 | 4,0 | 5,0 | 24,44 | 33,44 |
| पेंटन सी 5 एच 12 | 8,0 | 38,08 | 5,0 | 6,0 | 30,08 | 41,08 |
| ईथिलीन सी 2 एच 4 | 3,0 | 14,28 | 2,0 | 2,0 | 11,28 | 15,28 |
| प्रोपेलीन सी 3 एच 6 | 4,5 | 21,42 | 3,0 | 3,0 | 16,92 | 22,92 |
| Boutylene सी 4 एच 8 | 6,0 | 28,56 | 4,0 | 4,0 | 22,56 | 30,56 |
| पेंटिलीन सी 5 एच 10 | 7,5 | 35,70 | 5,0 | 5,0 | 28,20 | 38,20 |
| एसिटिलीन सी 2 एच 2 | 2,5 | 11,90 | 2,0 | 1,0 | 9,40 | 12,40 |
जटिल गैस के लिए, शुष्क वायु उपभोग वी सी, एम 3 / एम 3 को सूत्र द्वारा गणना की जाती है जो मिश्रण के व्यक्तिगत घटकों के ऑक्सीजन की आवश्यकता को ध्यान में रखती है:
वी सी \u003d 4.76 / 100 (0.5 एन 2 + 0.5CH + 2SH 4 + 3.5C 2 H 6 + 5C 3 H 8 + 6.5C 4 H 10 + 3C 2N 4 + 4,5C 3N 6 + 6C 4 H 8-O 2 ) (8.7)
गीले एयर वी वीएल, एम 3 / एम 3 की सैद्धांतिक खपत, पानी वाष्प की मात्रा पर फॉर्मूला (8.7) द्वारा निर्धारित अधिक:
V vl \u003d v c + 0.001244d v c (8.8) में
जहां डी हवा की आर्द्रता है, जी / एम 3।
गैसों की एक अज्ञात रासायनिक संरचना के साथ, लेकिन क्यू एच, केजे / एम 3 के दहन की अच्छी तरह से कम गर्मी, वायु वी टी, एम 3 / एम 3 की सैद्धांतिक खपत,
वी टी ≈ क्यू एन /3770 (8.9)
वास्तविक वायु उपभोग वी डीवी, एम 3 / एम 3, हमेशा कुछ हद तक बड़ा लिया जाता है:
वी डीवी \u003d वी टी α (8.10)
जहां α गोस्ट की आवश्यकताओं के अनुरूप एक अतिरिक्त वायु गुणांक है। ईंधन के पूर्ण दहन के लिए, α का मूल्य 1 से अधिक होना चाहिए 1. सूखी हवा में कुछ गैसों की दहन प्रतिक्रियाओं द्वारा गणना की गई दहन उत्पादों की संरचना और मात्रा, तालिका में दी गई है। 8.2।
8.3। दहन तापमान
गर्मी इंजीनियरिंग में, निम्नलिखित गैस दहन तापमान भिन्न होता है: गर्मी उत्पादन, कैलोरीमेट्रिक, सैद्धांतिक और मान्य (गणना)। गर्मी उत्पादकता टी एफ - अतिरिक्त वायु गुणांक α \u003d 1.0 के साथ और गैस और हवा के तापमान पर 0 डिग्री सेल्सियस के बराबर एडियाबेटिक स्थितियों में गैस के कुल दहन का अधिकतम तापमान:
टी डब्ल्यू \u003d क्यू एन / (σVC पी) (8.11)
जहां क्यू एन सबसे कम गर्मी दहन गर्मी, केजे / एम 3 है; ΣVC पी - कार्बन डाइऑक्साइड वॉल्यूम के उत्पादों की मात्रा, पानी वाष्प और नाइट्रोजन गैस के 1 मीटर 3 के दहन के दौरान गठित (एम 3 / एम 3), और 0 डिग्री सेल्सियस से तापमान के भीतर निरंतर दबाव में उनकी औसत वॉल्यूमेट्रिक गर्मी क्षमता टी जी (केजे / (एम 3 ओ डिग्री सेल्सियस)।
गैसों की गर्मी क्षमता की असाधारणता के आधार पर, गर्मी का उत्पादन लगातार अनुमानों की विधि से निर्धारित होता है। यह प्रारंभिक पैरामीटर के रूप में प्राकृतिक गैस (≈ 2000 डिग्री सेल्सियस) के लिए अपना मूल्य लेता है, α \u003d 1.0 के साथ, दहन उत्पादों के घटकों की मात्रा तालिका में निर्धारित की जाती है। 8.3 उनकी औसत गर्मी क्षमता है और फिर सूत्र (8.11) के अनुसार, गर्मी उत्पादन क्षमता पर विचार किया जाता है। यदि गिनने के परिणामस्वरूप यह कम या उच्च होगा, तो एक और तापमान निर्दिष्ट किया गया है और गणना दोहराई जाती है।
तालिका 8.3। गैसों की औसत वॉल्यूमेट्रिक गर्मी क्षमता, केजे / (एम 3 डिग्री सेल्सियस)
तापमान, ° С |
सीओ 2। | N 2। | ओ 2। | कं | Ch 4। | एच 2। | एच 2 ओ (पानी के जोड़ों) | वायु | |
|---|---|---|---|---|---|---|---|---|---|
| सूखी | 1 मीटर 3 पर गीला सुह गैस। |
||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 |
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 |
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 |
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 |
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 |
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 |
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 |
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 |
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 |
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 |
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 |
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 |
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 |
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | – | 1,3566 | 1,8085 | 1,4482 | 1,4771 |
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | – | 1,3650 | 1,8341 | 1,4582 | 1,4876 |
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | – | 1,3818 | 1,8585 | 1,4675 | 1,4973 |
| 1600 | 2,3751 | 1,4587 | 1,5427 | – | – | – | 1,8824 | 1,4763 | 1,5065 |
| 1700 | 2,3944 | 1,4671 | 1,5511 | – | – | – | 1,9055 | 1,4843 | 1,5149 |
| 1800 | 2,4125 | 1,4746 | 1,5590 | – | – | – | 1,9278 | 1,4918 | 1,5225 |
| 1900 | 2,4289 | 1,4822 | 1,5666 | – | – | – | 1,9698 | 1,4994 | 1,5305 |
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | – | – | 1,9694 | 1,5376 | 1,5376 |
| 2100 | 2,4591 | 1,4952 | 1,5809 | – | – | – | 1,9891 | – | – |
| 2200 | 2,4725 | 1,5011 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2300 | 2,4860 | 1,5070 | 1,5943 | – | – | – | 2,0252 | – | – |
| 2400 | 2,4977 | 1,5166 | 1,6002 | – | – | – | 2,0389 | – | – |
| 2500 | 2,5091 | 1,5175 | 1,6045 | – | – | – | 2,0593 | – | – |
सूखी हवा में उनके दहन के दौरान सामान्य सरल और जटिल गैसों की गर्मी-उत्पाद तालिका में दी जाती है। 8.4। वायुमंडलीय हवा में गैस जलते समय, लगभग 1 वजन होता है। % नमी, गर्मी उत्पादन क्षमता 25-30 डिग्री सेल्सियस कम हो जाती है।
तालिका 8.4। सूखी हवा में गैस गर्मी उत्पादन क्षमता
| साधारण गैस | हीट उत्पादकता, ° с | परिष्कृत गैस औसत रचना |
अनुमानित गर्मी दक्षता, ° с |
|---|---|---|---|
| हाइड्रोजन | 2235 | प्राकृतिक गैस जमा |
2040 |
| कार्बन ऑक्साइड | 2370 | प्राकृतिक तेल क्षेत्र |
2080 |
| मीथेन | 2043 | कोक |
2120 |
| एटैन | 2097 | उच्च तापमान आसवन शेल |
1980 |
| प्रोपेन | 2110 | दबाव में पैरॉक्सोजेनस दबाव |
2050 |
| बुटान | 2118 | ठोस कोयला जनरेटर |
1750 |
| पेंटेन | 2119 | फ्यूल जनरेटर |
1670 |
| ईथीलीन | 2284 | तरलीकृत (50% सी 3 एच 4 + 50% सी 4 एच 10) |
2115 |
| एसिटिलीन | 2620 | 2210 |
कैलोरीमेट्रिक दहन तापमान टी के पानी वाष्प और कार्बन डाइऑक्साइड के विघटन को ध्यान में रखे बिना तापमान निर्धारित किया जाता है, लेकिन वास्तविक प्रारंभिक गैस और वायु तापमान को ध्यान में रखते हुए। यह इस तथ्य में हीट उत्पादक टी डब्ल्यू से अलग है कि गैस और वायु का तापमान, साथ ही वायु गुणांक α को उनके मान्य मूल्यों के अनुसार स्वीकार किया जाता है। सूत्र द्वारा टी के निर्धारित करें:
टी के \u003d (क्यू एच + क्यू फिज़) / (σVC पी) (8.12)
जहां क्यू पिज़ - गैस और वायु की गर्मी युक्त (शारीरिक गर्मी), 0 डिग्री सेल्सियस, केजे / एम 3 से गिना जाता है।
प्राकृतिक और द्रवीकृत हाइड्रोकार्बन गैसों को आमतौर पर जलने से पहले गरम नहीं किया जाता है, और जलने के लिए आने वाली हवा की मात्रा की तुलना में उनकी मात्रा छोटी होती है। इसलिए, कैलोरीमेट्रिक तापमान निर्धारित करते समय, गैसों की गर्मी पीढ़ी पर विचार नहीं किया जा सकता है। दहन (जनरेटर, डोमेन इत्यादि) की कम गर्मी के साथ गैसों को जलाते समय, उनकी गर्मी उत्पादन (विशेष रूप से दहन से पहले गरम) कैलोरीमेट्रिक तापमान पर एक बहुत ही महत्वपूर्ण प्रभाव पड़ता है।
0 डिग्री सेल्सियस के तापमान के साथ हवा में औसत संरचना की प्राकृतिक गैस के कैलोरीमेट्रिक तापमान की निर्भरता और वायु अतिरिक्त गुणांक α की आर्द्रता तालिका में दी गई है। 8.5, द्रवीकृत हाइड्रोकार्बन गैस के लिए जब यह सूखी हवा में जलता है - तालिका में। 8.7। विवरण सारणी। 8.5-8.7 को अन्य प्राकृतिक गैसों के दहन का कैलोरीमेट्रिक तापमान स्थापित करते समय पर्याप्त सटीकता के साथ निर्देशित किया जा सकता है, अपेक्षाकृत निकटता, और लगभग किसी भी रचना के हाइड्रोकार्बन गैसों को स्थापित किया जाता है। यदि आवश्यक हो, तो कम हवा अतिरिक्त गुणांक के साथ गैसों को जलते समय उच्च तापमान प्राप्त करने के साथ-साथ भट्टियों की दक्षता में वृद्धि करने के लिए, हवा को प्रैक्टिस में गर्म किया जाता है, जिससे कैलोरीमेट्रिक तापमान में वृद्धि होती है (तालिका 8.6 देखें)।
तालिका 8.5। टी \u003d 0 डिग्री सेल्सियस के साथ हवा में जलती हुई प्राकृतिक गैस के कैलोरीमेट्रिक और सैद्धांतिक तापमान और अतिरिक्त वायु गुणांक α के आधार पर 1% की आर्द्रता
| सैद्धांतिक दहन तापमान टी टी, डिग्री सेल्सियस | वायु अतिरिक्त गुणांक α | कैलोरीमेट्रिक दहन तापमान टी से, डिग्री सेल्सियस | ||
|---|---|---|---|---|
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | – | 1,82 | 1260 |
| 1,25 | 1700 | – | 1,87 | 1230 |
| 1,28 | 1670 | – | 1,94 | 1200 |
| 1,30 | 1650 | – | 2,00 | 1170 |
तालिका 8.6। शुष्क हवा और उसके तापमान (गोलाकार मूल्यों) के गुणांक के आधार पर प्राकृतिक गैस टी, डिग्री सेल्सियस के जलने का कैलोरीमेट्रिक तापमान
| वायु अतिरिक्त गुणांक α | सूखी हवा का तापमान, ° C | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
तालिका 8.7। अतिरिक्त वायु गुणांक α के आधार पर टी \u003d 0 डिग्री सेल्सियस के साथ सूखी हवा में तकनीकी प्रोपेन के लिए कैलोरीमेट्रिक दहन तापमान टी
| वायु अतिरिक्त गुणांक α | कैलोरीमेट्रिक दहन तापमान टी से, डिग्री सेल्सियस | वायु अतिरिक्त गुणांक α | कैलोरीमेट्रिक दहन तापमान टी से, डिग्री सेल्सियस |
|---|---|---|---|
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
सैद्धांतिक दहन तापमान टी टी - अधिकतम तापमान कैलोरीमेट्रिक टी के के समान निर्धारित होता है, लेकिन कार्बन डाइऑक्साइड डाइऑक्साइड और पानी के भाप के विघटन के एंडोथर्मिक (आवश्यकता की आवश्यकता) में संशोधन के साथ, वॉल्यूम में वृद्धि के साथ जा रहा है:
सीओ 2 \u003c-\u003e सीओ + 0.5 ओ 2 - 283 एमजे / एमओएल (8.13)
एच 2 ओ \u003c-\u003e एच 2 + 0.5 ओ 2 - 242 एमजे / एमओएल (8.14)
उच्च तापमान पर, विघटन परमाणु हाइड्रोजन, ऑक्सीजन और हाइड्रोक्साइल समूहों के गठन का कारण बन सकता है। इसके अलावा, गैस जलते समय, नाइट्रोजन ऑक्साइड की एक निश्चित मात्रा हमेशा बनाई जाती है। ये सभी प्रतिक्रियाएं एंडोथर्मीनी हैं और दहन तापमान में कमी आ रही हैं।
सैद्धांतिक दहन तापमान निम्नलिखित सूत्र द्वारा निर्धारित किया जा सकता है:
t t \u003d (q h + q piz - q dis) / (σvc p) (8.15)
जहां क्यू डी डिसोसिएशन सीओ 2 और एच 2 ओ दहन उत्पादों, केजे / एम 3 में गर्मी की कुल लागत है; ΣVC पी - वॉल्यूम की मात्रा और दहन उत्पादों की औसत गर्मी क्षमता का योग, गैस के 1 मीटर 3 द्वारा पृथक्करण को ध्यान में रखते हुए।
तालिका 8.8। आंशिक दबाव के आधार पर जल वाष्प एच 2 ओ और कार्बन डाइऑक्साइड सीओ 2 के विघटन की डिग्री
| तापमान, ° С | आंशिक दबाव, एमपीए | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,004 | 0,006 | 0,008 | 0,010 | 0,012 | 0,014 | 0,016 | 0,018 | 0,020 | 0,025 | 0,030 | 0,040 | |
| जल वाष्प एच 2 ओ | ||||||||||||
| 1600 | 0,85 | 0,75 | 0,65 | 0,60 | 0,58 | 0,56 | 0,54 | 0,52 | 0,50 | 0,48 | 0,46 | 0,42 |
| 1700 | 1,45 | 1,27 | 1,16 | 1,08 | 1,02 | 0,95 | 0,90 | 0,85 | 0,8 | 0,76 | 0,73 | 0,67 |
| 1800 | 2,40 | 2,10 | 1,90 | 1,80 | 1,70 | 1,60 | 1,53 | 1,46 | 1,40 | 1,30 | 1,25 | 1,15 |
| 1900 | 4,05 | 3,60 | 3,25 | 3,0 | 2,85 | 2,70 | 2,65 | 2,50 | 2,40 | 2,20 | 2,10 | 1,9 |
| 2000 | 5,75 | 5,05 | 4,60 | 4,30 | 4,0 | 3,80 | 3,55 | 3,50 | 3,40 | 3,15 | 2,95 | 2,65 |
| 2100 | 8,55 | 7,50 | 6,80 | 6,35 | 6,0 | 5,70 | 5,45 | 5,25 | 5,10 | 4,80 | 4,55 | 4,10 |
| 2200 | 12,3 | 10,8 | 9,90 | 9,90 | 8,80 | 8,35 | 7,95 | 7,65 | 7,40 | 6,90 | 6,50 | 5,90 |
| 2300 | 16,0 | 15,0 | 13,7 | 12,9 | 12,2 | 11,6 | 11,1 | 10,7 | 10,4 | 9,6 | 9,1 | 8,4 |
| 2400 | 22,5 | 20,0 | 18,4 | 17,2 | 16,3 | 15,6 | 15,0 | 14,4 | 13,9 | 13,0 | 12,2 | 11,2 |
| 2500 | 28,5 | 25,6 | 23,5 | 22,1 | 20,9 | 20,0 | 19,3 | 18,6 | 18,0 | 16,8 | 15,9 | 14,6 |
| 3000 | 70,6 | 66,7 | 63,8 | 61,6 | 59,6 | 58,0 | 56,5 | 55,4 | 54,3 | 51,9 | 50,0 | 47,0 |
| सीओ 2 कार्बन डाइऑक्साइड | ||||||||||||
| 1500 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,4 | 0,4 | 0,4 | 0,4 | 0,4 | – |
| 1600 | 2,0 | 1,8 | 1,6 | 1,5 | 1,45 | 1,4 | 1,35 | 1,3 | 1,25 | 1,2 | 1,1 | |
| 1700 | 3,8 | 3,3 | 3,0 | 2,8 | 2,6 | 2,5 | 2,4 | 2,3 | 2,2 | 2,0 | 1,9 | |
| 1800 | 6,3 | 5,5 | 5,0 | 4,6 | 4,4 | 4,2 | 4,0 | 3,8 | 3,7 | 3,5 | 3,3 | |
| 1900 | 10,1 | 8,9 | 8,1 | 7,6 | 7,2 | 6,8 | 6,5 | 6,3 | 6,1 | 5,6 | 5,3 | |
| 2000 | 16,5 | 14,6 | 13,4 | 12,5 | 11,8 | 11,2 | 10,8 | 10,4 | 10,0 | 9,4 | 8,8 | |
| 2100 | 23,9 | 21,3 | 19,6 | 18,3 | 17,3 | 16,5 | 15,9 | 15,3 | 14,9 | 13,9 | 13,1 | |
| 2200 | 35,1 | 31,5 | 29,2 | 27,5 | 26,1 | 25,0 | 24,1 | 23,3 | 22,6 | 21,2 | 20,1 | |
| 2300 | 44,7 | 40,7 | 37,9 | 35,9 | 34,3 | 32,9 | 31,8 | 30,9 | 30,0 | 28,2 | 26,9 | |
| 2400 | 56,0 | 51,8 | 48,8 | 46,5 | 44,6 | 43,1 | 41,8 | 40,6 | 39,6 | 37,5 | 35,8 | |
| 2500 | 66,3 | 62,2 | 59,3 | 56,9 | 55,0 | 53,4 | 52,0 | 50,7 | 49,7 | 47,3 | 45,4 | |
| 3000 | 94,9 | 93,9 | 93,1 | 92,3 | 91,7 | 90,6 | 90,1 | 89,6 | 88,5 | 87,6 | 86,8 | |
जैसा कि तालिका से देखा जा सकता है। 8.8, 1600 डिग्री सेल्सियस तक के तापमान पर, पृथक्करण की डिग्री को ध्यान में नहीं रखा जा सकता है, और सैद्धांतिक दहन तापमान कैलोरीमेट्रिक के बराबर लिया जा सकता है। उच्च तापमान पर, विघटन की डिग्री कार्यक्षेत्र में तापमान को काफी कम कर सकती है। व्यावहारिक रूप से, इसके लिए कोई विशेष आवश्यकता नहीं है, सैद्धांतिक दहन तापमान केवल एक पूर्ववर्ती हवा (उदाहरण के लिए, मेनेंस) पर चल रहे उच्च तापमान भट्टियों के लिए निर्धारित किया जाना चाहिए। बॉयलर संयंत्रों के लिए कोई ज़रूरत नहीं है।
तालिका 8.9। ज्यादा से ज्यादा
तापमान उत्पन्न होता है
मुक्त लौ, ° с में
दहन उत्पादों का मान्य (गणना) तापमान टी डी - मशाल के सबसे गर्म बिंदु में वास्तविक परिस्थितियों में प्राप्त तापमान। यह सैद्धांतिक से नीचे है और पर्यावरण में गर्मी के नुकसान पर निर्भर करता है, विकिरण द्वारा जलते हुए क्षेत्र से पुनरावर्तन गर्मी की डिग्री, समय पर जलने की प्रक्रिया को खींचता है, आदि। भट्टियों और बॉयलर की भट्टियों में वास्तविक औसत तापमान है द्वारा निर्धारित थर्मल संतुलन या लगभग सैद्धांतिक या कैलोरीमेट्रिक दहन तापमान पर विशेष रूप से स्थापित सुधार गुणांक के परिचय के साथ भट्टियों में तापमान के आधार पर:
टी डी \u003d टी टी η (8.16)
जहां η- पायरोमेट्रिक गुणांक भीतर ढेर:
- थर्मल इन्सुलेशन के साथ उच्च गुणवत्ता वाले थर्मल और हीटिंग स्टोव के लिए - 0.75-0.85;
- गर्मी इन्सुलेशन के बिना हेमेटिक फर्नेस के लिए - 0.70-0.75;
- बॉयलर के ढाल वाले फर्श के लिए - 0.60-0.75।
व्यावहारिक रूप से, न केवल उपर्युक्त एडियाबेटिक दहन तापमान, बल्कि आग की लपटों में उत्पन्न अधिकतम तापमान भी। उनके अनुमानित मान आमतौर पर स्पेक्ट्रोग्राफी विधियों द्वारा प्रयोगात्मक रूप से स्थापित होते हैं। दहन के शंकु के सामने से 5-10 मिमी की दूरी पर मुक्त लौ में उत्पन्न होने वाले अधिकतम तापमान तालिका में दिखाए जाते हैं। 8.9। दिए गए डेटा के विश्लेषण से पता चलता है कि लौ में अधिकतम तापमान गर्मी उत्पादन से कम है (एच 2 ओ और सीओ 2 के विघटन की लागत के कारण और लौ क्षेत्र से गर्मी को हटाने)।
8.4। स्व-इग्निन तापमान
दहन प्रतिक्रियाओं को शुरू करने के लिए, ऑक्सीकरण एजेंट के साथ ईंधन मिश्रण की इग्निशन की स्थितियों की आवश्यकता होती है। सूजन सहज और मजबूर (इग्निशन) हो सकती है।
स्व-इग्निन तापमान - न्यूनतम तापमान जिसमें सहज (यानी बाहरी ताप आपूर्ति के बिना) गर्म गैस-वायु मिश्रण में शुरू होता है), गैस कणों को जलाने से गर्मी को अलग करके।
स्व-इग्निशन तापमान इस गैस के लिए तय नहीं है और कई मानकों पर निर्भर करता है: गैस-वायु मिश्रण में इसकी सामग्री, मिश्रण, आकार और जहाज के आकार की एकरूपता की डिग्री, जिसमें मिश्रण गर्म हो जाता है, गति और इसके हीटिंग का तरीका, पोत की दीवार का उत्प्रेरक प्रभाव, दबाव जिसके तहत मिश्रण स्थित है। सूचीबद्ध कारकों का सटीक लेखांकन बहुत जटिल है, इसलिए, अभ्यास में, उदाहरण के लिए, विस्फोट के खतरे का मूल्यांकन करते समय, प्रयोगात्मक डेटा का उपयोग करें (तालिका 8.10 देखें)।
तालिका 8.10। वायुमंडलीय दबाव में हवा के मिश्रण में कुछ गैसों और वाष्पों की आत्म-इग्निशन का सबसे छोटा मापा तापमान
ऑक्सीजन में स्व-इग्निशन दहन गैसों का तापमान हवा की तुलना में थोड़ा कम है। गिट्टी अशुद्धता (नाइट्रोजन और कार्बन डाइऑक्साइड) गैसों की शुरूआत स्वयं-इग्निशन तापमान में वृद्धि की ओर ले जाती है। स्व-इग्निशन के कम तापमान वाले घटकों की जटिल गैसों में उपस्थिति मिश्रण की आत्म-इग्निशन के तापमान में कमी की ओर ले जाती है।
मजबूर इग्निशन (इग्निशन) एक उच्च तापमान स्रोत के साथ एक या कई बिंदुओं में मिश्रण को उजागर करके किया जाता है - खुली लौ या फ्लू वॉल्यूम में बर्नर के अग्नि चैनलों से गैस के प्रस्थान के बिंदु पर विद्युत स्पार्क। इग्निशन इस तथ्य से आत्म-इग्निशन से अलग होता है कि ईंधन मिश्रण को लौ की उपस्थिति में लाया जाता है, लेकिन केवल इसके एक छोटे से हिस्से में। गर्म क्षेत्र से गर्मी सिंक की आवश्यकता होती है कि इग्निशन स्रोत की गर्मी अपव्यय तीव्रता इस गर्मी हटाने से अधिक हो जाती है। इग्निशन के बाद, इग्निशन स्रोत हटा दिया जाता है, और दहन लौ मोर्चे के प्रसार के कारण होता है।
8.5। ज्वलनशीलता सीमाएं और विस्फोट
गैस-उच्च मिश्रण केवल तभी उत्तेजित हो सकते हैं (विस्फोट) केवल जब मिश्रण में गैस सामग्री निश्चित रूप से (प्रत्येक गैस के लिए) सीमाएं हो सकती है। इस संबंध में, निचले और ऊपरी हैं एकाग्रता सीमा ज्वलनशीलता। निचली सीमा न्यूनतम, और ऊपरी - मिश्रण में गैस की अधिकतम मात्रा से मेल खाती है, जिसमें उनकी इग्निशन होती है (जब जलती हुई) और सहज (गर्मी सेवन के बिना) लौ (आत्म-इग्निशन) का प्रसार होता है। ये सीमाएं गैस-एयर मिश्रणों के विस्फोट की स्थितियों के अनुरूप हैं।
यदि गैस-ग्रेड मिश्रण में गैस सामग्री ज्वलनशीलता की निचली सीमा से कम है, तो इस तरह का मिश्रण जलाया जाता है और विस्फोट होता है, क्योंकि स्रोत के पास जारी गर्मी की गर्मी इग्निशन तापमान में मिश्रण को गर्म करने के लिए पर्याप्त नहीं है। यदि मिश्रण में गैस सामग्री ज्वलनशीलता के निचले और ऊपरी सीमाओं के बीच होती है, तो प्रस्तावित मिश्रण ज्वलनशील है और इग्निशन स्रोत के पास और जब इसे हटा दिया जाता है। यह मिश्रण विस्फोटक है। व्यापक रूप से ज्वलनशीलता सीमाएं (विस्फोट सीमा भी कहा जाता है) और निचली सीमा के नीचे, अधिक विस्फोटक गैस होगी। और अंत में, यदि मिश्रण में गैस सामग्री ज्वलनशीलता की ऊपरी सीमा से अधिक है, तो मिश्रण में हवा की मात्रा गैस के पूर्ण दहन के लिए पर्याप्त नहीं है।
ज्वलनशीलता सीमाओं का अस्तित्व दहन के दौरान थर्मल हानि के कारण होता है। वायु, ऑक्सीजन या गैस के साथ एक दहनशील मिश्रण को कम करते समय, थर्मल घाटे में वृद्धि होती है, लौ प्रसार दर कम हो जाती है, और दहन इग्निशन स्रोत को हटाने के बाद बंद हो जाता है।
तालिका 8.11। गैस के साथ एक मिश्रण में गैस ज्वलनशीलता सीमा (टी \u003d 20 डिग्री सेल्सियस और पी \u003d 101.3 केपीए पर)
| गैस | गैस-एयर मिश्रण में गैस सामग्री, के बारे में। % | ज्यादा से ज्यादा |
इग्निशन सीमाओं के साथ आउटलेट वायु गुणांक α | ||||
|---|---|---|---|---|---|---|---|
| ज्वलनशीलता की सीमा के साथ | मिश्रण की stoichiometric संरचना के साथ | मिश्रण की संरचना के तहत जो अधिकतम विस्फोट दबाव देता है | |||||
| निज़नी | अपर | निज़नी | अपर | ||||
| हाइड्रोजन | 4,0 | 75,0 | 29,5 | 32,3 | 0,739 | 9,8 | 0,15 |
| कार्बन ऑक्साइड | 12,5 | 74,0 | 29,5 | – | – | 2,9 | 0,15 |
| मीथेन | 5,0 | 15,0 | 9,5 | 9,8 | 0,717 | 1,8 | 0,65 |
| एटैन | 3,2 | 12,5 | 5,68 | 6,28 | 0,725 | 1,9 | 0,42 |
| प्रोपेन | 2,3 | 9,5 | 4,04 | 4,60 | 0,858 | 1,7 | 0,40 |
| एन-बोधिन | 1,7 | 8,5 | 3,14 | 3,6 | 0,858 | 1,7 | 0,35 |
| आइसोबुटन | 1,8 | 8,4 | 3,14 | – | – | ~1,8 | 0,35 |
| एन-पेंटन | 1,4 | 7,8 | 2,56 | 3,0 | 0,865 | 1,8 | 0,31 |
| ईथीलीन | 3,0 | 16,0 | 6,5 | 8,0 | 0,886 | 2,2 | 0,17 |
| प्रोपिलीन | 2,4 | 10,0 | 4,5 | ~5,1 | ~0,89 | 1,9 | 0,37 |
| बुटीलीन | 1,7 | 9,0 | 3,4 | ~4,0 | ~0,88 | 1,7 | 0,35 |
| एसिटिलीन | 2,5 | 80,0 | 7,75 | 14,5 | 1,03 | 3,3 | 0,019 |
तालिका 8.12। गैस ज्वलनशीलता ऑक्सीजन के साथ मिश्रण में (टी \u003d 20 डिग्री सेल्सियस और पी \u003d 101.3 केपीए पर)
हवा और ऑक्सीजन के साथ मिश्रण में आम गैसों के लिए ज्वलनशीलता की सीमा तालिका में दिखाए जाते हैं। 8.11-8.12। मिश्रण के तापमान में वृद्धि के साथ, ज्वलनशीलता सीमाएं विस्तारित की जाती हैं, और आत्म-इग्निशन के तापमान से अधिक तापमान पर, वायु या ऑक्सीजन के साथ गैस का मिश्रण किसी भी थोक अनुपात के साथ जलाया जाता है।
ज्वलनशीलता की सीमा न केवल दहनशील गैसों के प्रकारों पर निर्भर करती है, बल्कि प्रयोगों को पूरा करने के लिए शर्तों पर भी निर्भर करती है (पोत क्षमता, इग्निशन स्रोत का ताप स्रोत, मिश्रण का तापमान, लौ प्रचार, नीचे, क्षैतिज, आदि ।)। यह विभिन्न साहित्यिक स्रोतों में एक-दूसरे से अलग इन सीमाओं के महत्व को बताता है। टैब में। 8.11-8.12 कमरे के तापमान और वायुमंडलीय दबाव पर प्राप्त अपेक्षाकृत विश्वसनीय डेटा जब लौ में नीचे से 50 मिमी और अधिक व्यास के साथ नीचे से फैलता है। जब लौ ऊपर से नीचे या क्षैतिज रूप से फैलती है, तो निचली सीमा थोड़ा बढ़ जाती है, और ऊपरी घट जाती है। जटिल दहनशील गैसों की ज्वलनशीलता की सीमाएं जिनमें गिट्टी अशुद्धता नहीं होती है, यह एडिटिविटी के नियम द्वारा निर्धारित की जाती है:
एल जी \u003d (आर 1 + आर 2 + ... + आर एन) / (आर 1 / एल 1 + आर 2 / एल 2 + ... + आर एन / एल एन) (8.17)
जहां एल जी गैस-वायु या गैस कण मिश्रण में जटिल गैस की ज्वलनशीलता की निचली या ऊपरी सीमा है। %; आर 1, आर 2, ..., आर एन - जटिल गैस में व्यक्तिगत घटकों की सामग्री के बारे में। %; आर 1 + आर 2 + ... + आर एन \u003d 100%; एल 1, एल 2, ..., एल एन टेबल के अनुसार गैस-एयर या गैस कण मिश्रण में व्यक्तिगत घटकों की ज्वलनशीलता की नीचे या ऊपरी सीमा है। 8.11 या 8.12, के बारे में। %।
यदि गैस में गिट्टी अशुद्धता है, तो ज्वलनशीलता सीमा सूत्र द्वारा निर्धारित की जा सकती है:
एल बी \u003d एल जी / (8.18)
जहां एल बी गिट्टी अशुद्धियों के साथ मिश्रण की ज्वलनशीलता की ऊपरी और निचली सीमा है। %; एल जी एक दहनशील मिश्रण की ज्वलनशीलता की ऊपरी और निचली सीमा है। %; बी - गिट्टी अशुद्धता की संख्या, इकाई के शेयर।
गणना के दौरान, अक्सर ज्वलनशीलता की विभिन्न सीमाओं के तहत अतिरिक्त वायु गुणांक α को जानना आवश्यक होता है (तालिका देखें। 8.11), साथ ही गैस-एयर मिश्रण के विस्फोट से उत्पन्न दबाव भी। ज्वलनशीलता की ऊपरी या निचली सीमा के अनुरूप अतिरिक्त वायु गुणांक सूत्र द्वारा निर्धारित किया जा सकता है
α \u003d (100 / l - 1) (1 / v t) (8.19)
गैस-एयर मिश्रणों के विस्फोट से उत्पन्न होने वाले दबाव को निम्नलिखित सूत्रों के अनुसार पर्याप्त अनुमान के साथ निर्धारित किया जा सकता है:
हवा के साथ सरल गैस के stoichiometric अनुपात के लिए:
Rz \u003d p h (1 + βt k) (m / n) (8.20)
हवा के साथ जटिल गैस के किसी भी अनुपात के लिए:
Rz \u003d r (1 + βt k) v vlps / (1 + αV मीटर) (8.21)
जहां आरजेड विस्फोट से उत्पन्न होने वाला दबाव है, एमपीए; आर - प्रारंभिक दबाव (विस्फोट से पहले), एमपीए; β - गैसों के वॉल्यूम विस्तार का गुणांक, संख्यात्मक रूप से दबाव गुणांक (1/273) के बराबर; टी के - कैलोरीमेट्रिक दहन तापमान, डिग्री सेल्सियस; एम - विस्फोट के बाद मोल की संख्या, हवा में गैस जलती प्रतिक्रिया द्वारा निर्धारित; पी - दहन प्रतिक्रिया में शामिल विस्फोट के लिए मोल की संख्या; वी वीएलपी - गीले दहन उत्पादों की मात्रा 1 मीटर 3 गैस, एम 3; वी टी - सैद्धांतिक वायु प्रवाह, एम 3 / एम 3।
तालिका 8.13। रीसेट गुणांक के शनि और सुरक्षात्मक उपकरण के प्रकार के आधार पर प्रोपेन मिश्रण के विस्फोट से उत्पन्न होने वाला दबाव
| सुरक्षात्मक उपकरण का प्रकार | राहत गुणांक के सैट, एम 2 / एम 3 | ||
|---|---|---|---|
| 0,063 | 0,033 | 0,019 | |
| ग्लास 3 मिमी मोटी के आउटडोर बन्धन के साथ एकल बहरा ग्लेज़िंग | 0,005 | 0,009 | 0,019 |
| आउटडोर ग्लास फास्टनिंग 3 मिमी मोटी के साथ डबल बहरा ग्लेज़िंग | 0,007 | 0,015 | 0,029 |
| स्विवेल सिंगल विंडो लोड 5 एमपीए / एम 2 पर एक बड़े हिंग और स्प्रिंग लॉक के साथ बाध्यकारी | 0,002 | – | – |
| स्विवेल सिंगल विंडो लोड 5 एमपीए / एम 2 पर टॉप हिंग और स्प्रिंग लॉक के साथ बाध्यकारी | 0,003 | – | – |
| स्लैब ओवरलैप द्रव्यमान पर स्वतंत्र रूप से झूठ बोलते हुए, किलो / एम 2: | |||
| 0,023 | |||
| 0,005 | |||
| 0,018 | |||
मेज में दिखाया गया विस्फोट दबाव। 8.13 या सूत्रों द्वारा परिभाषित केवल तभी हो सकता है जब गैस टैंक के अंदर पूरी तरह से दहन हो और इसकी दीवारों की गणना इन दबावों पर की जाती है। अन्यथा, वे दीवारों की ताकत या उनके सबसे आसानी से ढहने वाले हिस्सों तक सीमित हैं - दबाव दालें ध्वनि की गति पर मिश्रण की गैर-ऑप्टिकल मात्रा पर प्रचार करती हैं और लौ के सामने की तुलना में बहुत तेज बाड़ लगाने तक पहुंचती हैं।
यह सुविधा ज्वाला और दबाव दालों (सदमे की लहर) की स्प्रेडशीट दरों में अंतर है - व्यापक रूप से सुरक्षा के लिए अभ्यास में उपयोग की जाती है गैस उपकरण और विस्फोट के दौरान विनाश से परिसर। ऐसा करने के लिए, दीवारों और ओवरलैप्स के उद्घाटन में आसानी से खुले या विनाशकारी फ्रैमुगा, फ्रेम, पैनल, वाल्व इत्यादि स्थापित किए जाते हैं। विस्फोट के दौरान परिणामस्वरूप दबाव सुरक्षा उपकरणों के डिजाइन और केआरई के रीसेट गुणांक की विशेषताओं पर निर्भर करता है, जो क्षेत्र का क्षेत्र है सुरक्षात्मक उपकरण कमरे के आकार के लिए।
8.6। निश्चित माध्यम में जल रहा है
अग्निमय क्षेत्र की आंदोलन लौ का मोर्चा है, दहन उत्पादों से प्रतिक्रिया के लिए ईंधन को अलग करने वाले क्षेत्र को इस तथ्य के कारण होता है कि थर्मल चालकता और प्रसार के कारण ठंड दहनशील मिश्रण को इग्निशन तापमान में गरम किया जाता है ठंड मिश्रण में गर्म जलती हुई उत्पाद। रैखिक गति जिसके सामने लौ के सामने एक सजातीय दहनशील मिश्रण के साथ स्थानांतरित किया जाता है उसे कहा जाता है वर्दी ज्वाला वितरण गतिगैस-वायु मिश्रण में गैस के प्रकार और इसकी सामग्री पर दोनों के आधार पर। सभी प्रकार के दहनशील गैसों के लिए न्यूनतम गति इग्निशन की निचली और ऊपरी सीमा से मेल खाती है, और अधिकतम - गैसों और वायु का अनुपात।
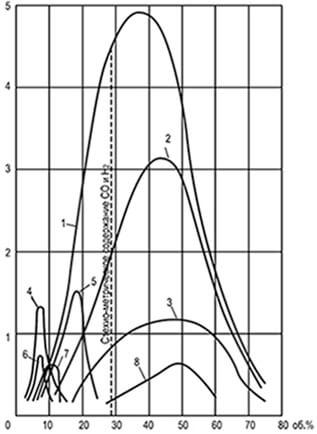
अंजीर। 8.1। वर्दी गति घटता है
ज्वाला यू एन फैलाना, परिभाषित किया गया
25.4 मिमी व्यास के साथ ट्यूब में
1-हाइड्रोजन; 2-पानी गैस; 3-कार्बन ऑक्साइड;
4-ईथिलीन; 5-कोक गैस; 6-एथन; 7-मीथेन;
8-जनरेटर गैस भाप-विमान
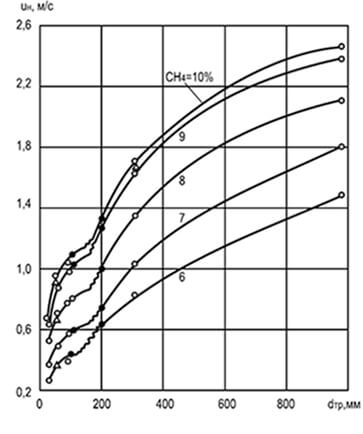
अंजीर। 8.2। व्यास डी टीआर और एकाग्रता का प्रभाव
बदलने के लिए हवा के साथ एक मिश्रण में मीथेन
ज्वाला यू एन फैलाने की समान गति
प्रयोगों में पाया गया कि लौ के प्रसार की दर बेलनाकार ट्यूब के व्यास पर निर्भर करती है, जिसके अनुसार यह वितरित करता है: अधिक व्यास, वितरण की गति जितनी अधिक होगी। ट्यूब के व्यास में वृद्धि दहन प्रक्रिया पर दीवारों के प्रभाव को कम कर देती है और लौ मोर्चे को स्थानांतरित करती है और संवहन (चित्र 8.2) को बढ़ाने में मदद करती है। इन ग्राफिक्स का विश्लेषण इंगित करता है कि ट्यूबों के बहुत छोटे आकार के साथ, ज्वाला का प्रसार संभव नहीं है (मजबूत रिश्तेदार गर्मी सिंक के कारण)। जिन ट्यूबों, चैनलों और दरारों के आयाम जिनमें लौ लागू नहीं होती है, उन्हें महत्वपूर्ण कहा जाता है।
वे विभिन्न गैसों के लिए अलग हैं:
- हवा के साथ मीथेन का ठंडा मिश्रण - 3 मिमी;
- हाइड्रोजन-वायु मिश्रण 0.9 मिमी है;
- हवा के साथ मीथेन का गर्मजोशी मिश्रण 1.2 मिमी है।
छोटे खंड चैनलों में विफलता का उपयोग फायरप्रूफर्स बनाने के लिए अभ्यास में किया जाता है: फ्लेममेकिंग ग्रिड, सिरेमिक छिद्रित डिस्क, दबाए गए धातु गेंदों से डिस्क, जुर्मानी सामग्री से भरे जहाजों, आदि); गैस-एयर मिश्रणों पर परिचालन करने वाले बर्नर के डिजाइन में फायर चैनल।
गैसों के दहनशील गुणों की तुलनात्मक विशेषताओं के लिए (ट्यूबों के आकार के बावजूद), अवधारणा "सामान्य ज्वाला वितरण गति" - यह शीत (अभी भी गैर-ज्वलनशील) मिश्रण के लिए जिम्मेदार गति है जिसके साथ लौ सामान्य रूप से इसकी सतह पर चलती है। लौ मोर्चा फ्लैट और ट्यूब के व्यास के बराबर बना दिया जाता है:
u h \u003d w p πr 2 /s(8.22)
जहां यू एन ज्वाला प्रचार की सामान्य गति है, एम / एस; डब्ल्यू पी - मापा वर्दी लौ प्रसार दर, एम / एस; आर ट्यूब त्रिज्या, एम है; एस - लौ सामने सतह क्षेत्र, एम 2।
तालिका 8.14। विभिन्न गैस-एयर मिश्रणों में लौ प्रसार वेग (टी \u003d 20 डिग्री सेल्सियस और पी \u003d 103,3 सीपीए), एम / एस
| गैस | अधिकतम सामान्य के साथ मिश्रण ज्वाला स्प्रेड स्पीड |
StoichioMetric मिश्रण | ||||
|---|---|---|---|---|---|---|
| मिश्रण में सामग्री के बारे में। % | ज्यादा से ज्यादा साधारण स्पीड वितरण |
मिश्रण में सामग्री के बारे में। % | साधारण स्पीड वितरण प्रसिद्धि |
|||
| गैस | वायु | गैस | वायु | |||
| हाइड्रोजन | 42,0 | 58,0 | 2,67 | 29,5 | 70,5 | 1,6 |
| कार्बन ऑक्साइड | 43,0 | 57,0 | 0,42 | 29,5 | 70,5 | 0,30 |
| मीथेन | 10,5 | 89,0 | 0,37 | 9,5 | 90,5 | 0,28 |
| एटैन | 6,3 | 93,7 | 0,40 | 5,7 | 94,3 | 0,32 |
| प्रोपेन | 4,3 | 95,7 | 0,38 | 4,04 | 95,96 | 0,31 |
| एन-बोधिन | 3,3 | 96,7 | 0,37 | 3,14 | 96,86 | 0,30 |
| ईथीलीन | 7,0 | 93,0 | 0,63 | 6,5 | 93,5 | 0,5 |
| प्रोपिलीन | 4,8 | 95,2 | 0,44 | 4,5 | 95,5 | 0,37 |
| बुटीलीन | 3,7 | 96,3 | 0,43 | 3,4 | 96,6 | 0,38 |
| एसिटिलीन | 10,0 | 90,0 | 1,35 | 7,75 | 92,25 | 1,0 |
जैसा कि डेटा तालिका से देखा जा सकता है। 8.14, लौ के प्रचार की अधिकतम दर ऑक्सीडेंट (स्टॉइचियोमेट्रिक नहीं) के नुकसान के साथ गैस और हवा के मिश्रण से मेल खाती है। ज्वलनशील की अधिकता में, प्रतिक्रियाशील कणों की टक्कर की प्रभावशीलता और रासायनिक प्रतिक्रियाओं की दर बढ़ जाती है।
गैस ऑक्सीजन मिश्रण के लिए लौ प्रसार गति गैस मनोरंजन के मुकाबले परिमाण का क्रम है। इस प्रकार, मीथेन-ऑक्सीजन मिश्रण की लौ के प्रसार की अधिकतम सामान्य दर 3.3 मीटर / एस है, और ऑक्सीजन के साथ प्रोपेन और ब्यूटेन के मिश्रण के लिए - 3.5-3.6 मीटर / एस।
हवा, एम / एस के साथ जटिल गैस के मिश्रण में अधिकतम सामान्य लौ प्रसार दर सूत्र द्वारा निर्धारित की जाती है:
यू एन मैक्स \u003d (आर 1 यू 1 + आर 2 यू 2 + ... + आर एन यू एन) / (आर 1 + आर 2 + ... + आर एन) (8.23)
जहां आर 1, आर 2, ... आर एन एक जटिल गैस में व्यक्तिगत घटकों की सामग्री है, के बारे में। %; यू 1, यू 2, ... यू एन - एयर, मैसर्स के साथ मिश्रण में जटिल गैस के लौ घटकों के प्रसार के लिए अधिकतम सामान्य वेग।
कम अनुपात गैसों के लिए निकट सामान्य लौ प्रसार दर के साथ उपयुक्त हैं, उदाहरण के लिए, प्राकृतिक और द्रवीकृत हाइड्रोकार्बन गैसों के लिए। ज्वाला प्रचार की तेजी से विभिन्न दरों के साथ गैसों के मिश्रण के लिए (उदाहरण के लिए, प्राकृतिक और कृत्रिम गैसों के मिश्रण के लिए, उच्च हाइड्रोजन सामग्री के साथ मिश्रण), वे केवल अनुमानित मान देते हैं।
यदि मिश्रण में गिट्टी अशुद्धता (नाइट्रोजन और कार्बन डाइऑक्साइड) होता है, तो लौ प्रसार की दर की अनुमानित गणना के लिए, सूत्र का उपयोग किया जाना चाहिए:
यू बी \u003d यू एन मैक्स (1 - 0.01 एन 2 - 0,012 एसओ 2) (8.24)
संयुक्त गैस-वायु मिश्रण की लौ प्रसार की दर में काफी वृद्धि हुई है:
और 'एन \u003d और एन (टी' / टी) (8.25)
जहां और एच - पूर्ण तापमान टी ', के के साथ गर्म मिश्रण में लौ का फैलाव; और एन - वही, तापमान टी, के के साथ एक ठंड मिश्रण में।
मिश्रण का प्री-हीटिंग अपने घनत्व को पूर्ण तापमान के विपरीत आनुपातिक परिवर्तित करता है, इसलिए इस तापमान के अनुपात में लौ प्रसार की दर बढ़ जाती है। गणना करते समय इस तथ्य को ध्यान में रखा जाना चाहिए, खासकर उन मामलों में जहां बर्नर के आग चैनल गर्म चिनाई में स्थित होते हैं या जब वे उन्हें भट्ठी, गर्म गैसों आदि के विकिरण को प्रभावित करते हैं।
निम्नलिखित स्थितियों में लौ के प्रसार की एकरूपता संभव है:
- फायर ट्यूब की एक छोटी लंबाई है;
- जलती हुई वायुमंडलीय के करीब लगातार दबाव पर फैलती है।
यदि ट्यूब की लंबाई महत्वपूर्ण है, तो कुछ मिश्रणों के लिए लौ का वर्दी वितरण कंपन में जा सकता है, और फिर एक सुपरसोनिक दहन दर (2000 मीटर या उससे अधिक) के साथ विस्फोट में, जब मिश्रण इग्निशन सदमे के कारण होता है लहर, मिश्रण को तापमान में गर्म करने, आत्म-इग्निशन तापमान से अधिक। विस्फोट ज्वाला की उच्च दर के साथ मिश्रण में होता है। विस्फोट की एकाग्रता की सीमाएं गैस-एयर और गैस कण मिश्रणों की ज्वलनशीलता की पहले से ही सीमाएं हैं। %: प्रोपेन - 3.2-37, आइसोबुटन - 2.8-31, हाइड्रोजन - 15-90। विस्फोट दहन से उत्पन्न होने वाला दबाव प्रारंभिक दस गुना से अधिक हो सकता है और उच्च दबाव के लिए डिजाइन किए गए पाइप और अन्य जहाजों के विनाश का कारण बन सकता है।
8.7। लैमिनार और अशांत प्रवाह में जल रहा है
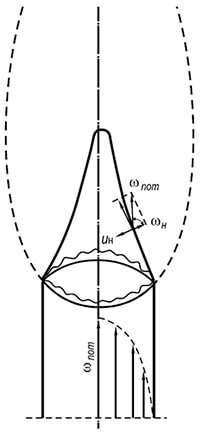
अंजीर। 8.3। जलने के सामने
गैस-वायु मिश्रण बी।
लैमिनार गति मोड
यदि आप सामान्य लौ प्रसार दर के बराबर गति से एक दहनशील मिश्रण का काउंटर आंदोलन बनाते हैं तो लौ मोर्चा को रोक दिया जा सकता है। दृश्य उदाहरण - बुन्ज़न बर्नर के आंतरिक शंकु की सतह। आंदोलन के लैमिनेर मोड के दौरान बर्नर से उत्पन्न गैस-वायु मिश्रण की संरचना के विनियमन के कारण, जलने के एक स्थिर और तेजी से उल्लिखित शंकु प्राप्त करना संभव है (चित्र 8.3)। शंकु (लौ के सामने) की तरफ की सतह, बर्नर चैनल के अग्नि किनारे के सापेक्ष तय की गई, बहने वाले गैस-एयर मिश्रण की ओर बढ़ती है, और इस मामले में लौ प्रत्येक बिंदु पर इग्निशन सतह में सामान्य फैली हुई है। लौ के शंकु की सतह पर, गति की समानता संरक्षित है - गैस-वायु मिश्रण की प्रवाह दर की सामान्य रूप से डब्ल्यूएन के सामान्य से शंकु के रूप में और लौ यू एन के प्रचार की सामान्य दर मिशेलसन के कानून द्वारा आज्ञा मानते हैं:
w h \u003d w pot cosφ \u003d u h (8.26)
जहां φ प्रवाह दिशा के बीच कोण और लौ के शंकु के सामने की सतह के लिए सामान्य है; डब्ल्यू पॉट - समय की प्रति इकाई बर्नर के माध्यम से गुजरने वाले गैस-वायु मिश्रण की औसत प्रवाह दर, एम / एस।
सामान्य लौ प्रसार दर की स्थिरता केवल शंकु लौ मोर्चे की तरफ की सतह के मुख्य भाग के लिए मान्य है। शंकु के शीर्ष में, गैस-वायु मिश्रण के हीटिंग के कारण गति बढ़ जाती है, जो लौ मोर्चे की शंकु सतह के निकटता वाले क्षेत्रों की बारीकी से स्थित है, और शंकु के आधार पर - इसे शीतलन प्रभाव के कारण कम हो जाता है बर्नर के फायर चैनल का अंत।
व्यावहारिक गणनाओं के लिए, आमतौर पर इस अंतर से उपेक्षित होता है और शंकु की पूरी सतह पर लौ निरंतर लौ निरंतर के माध्यम से मिश्रण की गति को और यू एन के बराबर होता है।
औसत सामान्य लौ प्रसार दर बराबर है
यू एच \u003d वी सेमी / एस (8.27)
जहां वी सेमी गैस-एयर मिश्रण के बर्नर के माध्यम से गुजरने वाली मात्रा है, एस लौ के शंकु के सामने का सतह क्षेत्र है।
व्यावहारिक रूप से, लौ के शंकु के सामने कोई उचित ज्यामितीय रूप नहीं है, इसलिए के लिए सटीक परिभाषा एस लौ फोटोग्राफ है, लौ के सामने कई छिद्रित शंकु में बांटा गया है। साइड सतहों का योग शंकु लौ मोर्चा की कुल सतह है। बुनज़ेन बर्नर और अन्य विधियों की विधि के रूप में परिभाषित सामान्य लौ प्रसार दरों के मूल्य तालिका में दिखाए गए सामान्य वेग के समान और समान हैं। 8.14।
ज्वाला के शंकु मोर्चे की ऊंचाई मुख्य रूप से अग्नि चैनल बर्नर के आकार पर निर्भर करती है। लौ की ऊंचाई में कमी बड़े फायरिंग चैनलों को कुचलने से कई छोटे में हासिल की जा सकती है। एक ही गैस-वायु मिश्रणों के लिए, छोटे चैनलों की लौ के शंकु मोर्चों की ऊंचाई को लगभग एकल चैनल एन के सामने की ऊंचाई पर निर्धारित किया जा सकता है:
एच \u003d एच / √N (8.28)
जहां एन छोटे चैनलों की संख्या है।
उच्च थर्मल पावर (औद्योगिक बॉयलर, भट्टियों आदि के बर्नर) के साथ बर्नर के लिए, एक नियम के रूप में जलन, एक अशांत धारा में होता है - भंवर गति और पल्सेशन के कारण लौ के एक चिकनी शंकु सामने धुंधला होता है और स्पष्ट शंकुधारी खो देता है रूपरेखा। उसी समय, छोटे पैमाने पर अशांति के अनुरूप, जलने के दो विशिष्ट प्रकार मनाए जाते हैं।
अशांति के पैमाने के पैमाने के साथ लैमिनार जलने वाले क्षेत्र की मोटाई से अधिक नहीं, लौ के शंकु के सामने अपने आकार को बरकरार रखता है और चिकनी रहता है, हालांकि दहन क्षेत्र बढ़ता है। यदि अशांति का स्तर सामान्य जलने के क्षेत्र की मोटाई से अधिक है, तो लौ के शंकु की सतह की सतह असमान हो जाती है। इससे दहन के सामने की कुल सतह में वृद्धि होती है और प्रति यूनिट अधिक ईंधन मिश्रण जलती है क्रॉस सेक्शन बाढ़।
बड़े पैमाने पर अशांति के साथ, लैमिनेर जलने के क्षेत्र की मोटाई की तुलना में काफी अधिक है, लौ के मोर्चे की सतह का उत्साह गर्म मिश्रण के अलग-अलग कणों को अलग करने की ओर जाता है, बाद के लहरों को क्रोधित करता है। लौ का मोर्चा अपनी ईमानदारी खो देता है और एक दहनशील मिश्रण की धारा में बराबर, difembly और दहनशील कणों के रूप में व्यक्तिगत जलती हुई फॉसी की एक प्रणाली में बदल जाता है।
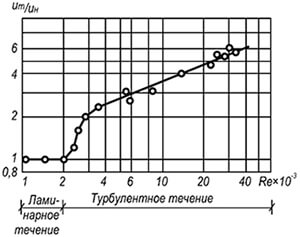
अंजीर। 8.4। सापेक्ष गति बदलें
मसालेदार कोक गैस लौ
संख्या के आधार पर हवा के साथ मिश्रण में
रेनॉल्ड्स और मोशन मोड आंदोलन
बड़े पैमाने पर अशांति के साथ, लौ मोर्चे की सतह, सभी जलने वाले कणों की सतहों से क्लैंपिंग, बढ़ जाती है, जो लौ (चित्र 8.4) के प्रसार की दर में तेज वृद्धि की ओर अग्रसर होती है। इस मामले में, न केवल सामने दहन हो सकता है, सामान्य दर वी एन पर प्रचारित, बल्कि वॉल्यूमेट्रिक भी, जो ताजा मिश्रण में गर्म जलने वाले उत्पादों की अशांत लहरों के कारण होता है। नतीजतन, बड़े पैमाने पर अशांति के तहत लौ प्रसार की कुल दर सामने और वॉल्यूमेट्रिक जलने के तत्वों के एक या एक और संयोजन द्वारा निर्धारित की जाती है।
लहरों की अनुपस्थिति में, अशांत दहन दर सामान्य लौ प्रसार दर के बराबर हो जाती है। इसके विपरीत, अगर पल्सेशन की गति सामान्य से अधिक से अधिक हो जाती है, तो अशांत जला की गति थोड़ा निर्भर हो जाती है भौतिक - रासायनिक गुण दहनशील मिश्रण। प्रयोगों ने सामान्य लौ प्रसार दर से औद्योगिक भट्टियों में α\u003e 1 के साथ विभिन्न सजातीय गैस-एयर मिश्रणों की दहन दर की एक छोटी निर्भरता दिखायी।
8.8। जलन की स्थिरता
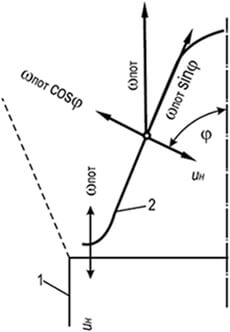
अंजीर। 8.5। प्रत्यक्ष मुआवजा योजना
लैमिनार मोशन के साथ यू एच \u003d डब्ल्यू पसीना
गैस-वायु मिश्रण
1 - बर्नर की दीवार;
2 - लौ मोर्चा
जलने की स्थिरता को प्रभावित करने वाले मुख्य कारक गैस-वायु मिश्रण की समाप्ति दर और लौ के प्रसार की समाप्ति दर हैं। जब लैमिनेर स्ट्रीम में गैस-एयर मिश्रणों का दहन, लौ के शंकु के सामने का एक स्थिर हिस्सा इसका निचला हिस्सा है। इस जगह में, ज्वाला मोर्चा वायुमंडल में बहने वाले गैस-एयर मिश्रण के विस्तार के कारण और चैनल की दीवार को ब्रेक लगाना क्षैतिज में तैनात किया जाता है और चैनल के किनारे पर लौ के किनारे पर उठाया जाता है (अंजीर। 8.5)।
सामने के इस खंड में, लौ प्रसार की गैस-वायु प्रवाह दर की गति का एक पूर्ण मुआवजा यू एन \u003d डब्ल्यू पसीना होता है। लौ के मोर्चे के बाकी शंकुधारी में, मुआवजे में आंशिक चरित्र होता है और केवल दिशा में किया जाता है, सामान्य दहन के लिए सामान्य: यू एच \u003d डब्ल्यू पसीना कोस। पॉट सिनस असंतुलित रहता है और शंकु के आधार से अपने शीर्ष तक इग्निशन बिंदु को ध्वस्त करता है। लौ के शंकु के मोर्चे की स्थिरता को आधार पर अंगूठी बेल्ट द्वारा एक इग्निशन स्रोत के रूप में कार्य किया जाता है, जिसके बिना बाकी के सामने गैस-वायु मिश्रण के प्रवाह से ध्वस्त हो जाएगा।
यदि मिश्रण की समाप्ति की दर लौ प्रसार की दर से अधिक है, तो इग्निशन बेल्ट की चौड़ाई तब तक घट जाती है जब तक यह नगण्य न हो जाए। इस मामले में, लौ मोर्चे की स्थिरता टूट गई है, और मशाल को बर्नर से अलग किया जाता है। यदि कणिका दीवार क्षेत्र (दीवार पर नहीं) में लौ के प्रसार की दर गैस-वायु मिश्रण की समाप्ति की दर से अधिक हो जाएगी, तो लौ बर्नर मिक्सर (छोड़ें) के अंदर खींची गई है।
जब अलग हो जाता है:
- बर्नर और उसके विलुप्त होने के साथ लौ टूटना;
- आग चैनल के किनारे से अलग होने पर लौ पर धारा में एक नई पर्याप्त स्थिर स्थिति तक पहुंच जाती है;
- व्यवधान उठाया लौ और उसके विलुप्त होने;
- बर्नर के अग्नि चैनल के किनारे तक उठाया मशाल का कचरा;
- एक भारित लौ बनाना जब जेट इग्निशन बर्नर से कुछ दूरी पर होता है।
इन सभी घटनाओं की अनुमति नहीं है, क्योंकि वे आसपास के वातावरण में या असंतुलित गैस की भट्टी में संचय करते हैं।
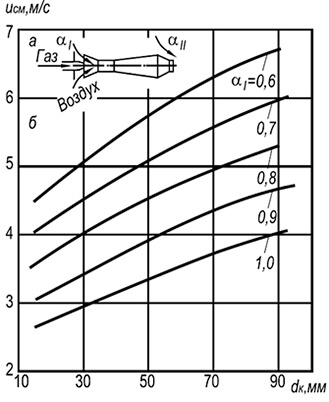
अंजीर। 8.6। एकान्त के पृथक्करण की गति की निर्भरता
प्राकृतिक मिश्रणों के खुले वातावरण में लौ
अग्नि नहर के आकार से हवा के साथ गैस और
प्राथमिक हवा की सामग्री।
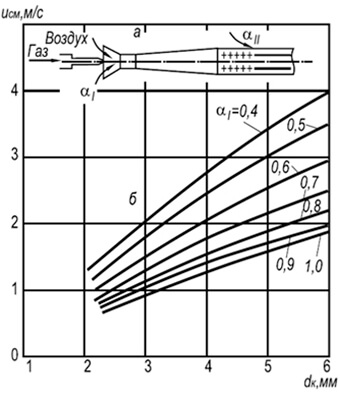
अंजीर। 8.7। अलगाव की गति की निर्भरता
एक खुले वातावरण में multifacelle लौ
आकार से हवा के साथ प्राकृतिक गैस मिश्रण
अग्नि चैनल और प्राथमिक वायु सामग्री।
ए - बर्नर योजना; बी - लौ ओपन वक्र
अंजीर में। 8.6 इंजेक्शन के फायरवॉल के किनारों से प्रायोगिक लपटें सिंगल-पैकिंग बर्नर एयर के साथ ठंडे गैस के मिश्रण पर चल रहे हैं। सीमा पर और इन घटता के ऊपर, लौ पीटा जाता है, और घटता के नीचे - टिकाऊ जलती हुई।
व्यावहारिक रूप से, 2-6 मिमी व्यास वाले फायरिंग चैनलों के साथ मल्टीफैसेल इंजेक्शन बर्नर व्यापक हैं (चित्र 8.7)। ऐसे बर्नर के लिए डब्ल्यू ओटीपी की आग की गति की स्थापना निम्नलिखित सूत्र के अनुसार की जा सकती है:
डब्ल्यू ओटीआर \u003d 3.5 10 -3 डी के टी 2 (1 + वी टी) / (1 + α 1 वी टी) (8.2 9)
जहां डी के आग चैनल का व्यास है, एम; α 1 प्राथमिक वायु गुणांक से अधिक है; टी - गैस-एयर मिश्रण का पूर्ण तापमान, के।
सूत्र के अनुसार, यह देखा जा सकता है कि जलती स्थिरता अग्नि चैनलों और तापमान के व्यास में वृद्धि के साथ बढ़ती है और प्राथमिक वायु अतिरिक्त गुणांक की अधिक वृद्धि के साथ घट जाती है। ज्वाला के पारस्परिक प्रभाव के कारण जलती स्थिरता भी बढ़ रही है।
अन्य कारणों से आग चैनलों से लौ का पृथक्करण हो सकता है। बर्नर और जलने वाले उत्पादों के चैनलों के गलत स्थान के साथ, वे बर्नर इंजेक्टर में प्रवेश कर सकते हैं और लौ पृथक्करण के लिए नेतृत्व कर सकते हैं (निष्क्रिय गैसों के साथ पतला गैस-वायु मिश्रण में लौ प्रसार दर में कमी के कारण)। इसके अलावा, अलगाव का कारण अग्नि चैनलों से लौ को उड़ाने वाली द्वितीयक हवा की उच्च गति हो सकती है।
तालिका 8.15। प्राकृतिक के एक सजातीय मिश्रण की गति
हवा के साथ गैस जिस पर एक पर्ची है
लौ, एम / एस (मिश्रण का तापमान 20 डिग्री सेल्सियस)
| व्यास आग चैनल |
प्राथमिक वायु अतिरिक्त गुणांक | |||||
|---|---|---|---|---|---|---|
| 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | 1,1 | |
| 3,5 | 0,05 | 0,10 | 0,18 | 0,22 | 0,23 | 0,21 |
| 4,0 | 0,08 | 0,12 | 0,22 | 0,25 | 0,26 | 0,20 |
| 5,0 | 0,09 | 0,16 | 0,27 | 0,31 | 0,31 | 2,23 |
| 6,0 | 0,11 | 0,18 | 0,32 | 0,38 | 0,39 | 0,26 |
| 7,0 | 0,13 | 0,22 | 0,38 | 0,44 | 0,45 | 0,30 |
| 8,0 | 0,15 | 0,25 | 0,43 | 0,50 | 0,52 | 0,35 |
| 9,0 | 0,17 | 0,28 | 0,48 | 0,57 | 0,58 | 0,39 |
| 10,0 | 0,20 | 0,30 | 0,54 | 0,64 | 0,65 | 0,43 |
बर्नर मिक्सर के अंदर भी अनुचित आग, आमतौर पर कपास के साथ। स्क्वायर या तो लौ की आबादी और कमरे या फ़ायरबॉक्स में एक असंतुलित मिश्रण की रिहाई, या बर्नर के अंदर मिश्रण को जलाने के लिए ले जाता है। फिसलन की ज्वाला की प्रवृत्ति गैस के प्रकार, लौ की सामान्य फैल दर, गैस-वायु मिश्रण में प्राथमिक हवा की सामग्री, अग्नि चैनलों का आकार, मिश्रण या दीवारों का तापमान चैनल। लौ स्पॉक पर प्रभाव उन सामग्रियों की थर्मल चालकता का गुणांक भी होता है जिनसे फायर चैनल बनाए जाते हैं, उनके आकार, गहराई और निर्माण की गुणवत्ता, विस्फोट की उपस्थिति, किनारों की बग इत्यादि।
मेज में एलईडी। 8.15 हवा के साथ प्राकृतिक गैसों के सजातीय मिश्रणों के वेगों के मूल्यों, जिस पर एक पर्ची है, अन्य गैसों के लिए उपयोग की जा सकती है, संशोधन को ध्यान में रखते हुए:
डब्ल्यू "पीआर \u003d डब्ल्यू पीआर यू" एन / यू एन (8.30)
जहां डब्ल्यू पीआर एक और गैस, एम / एस के लिए एक लौ फिसलन की दर है; डब्ल्यू पीआर - प्राकृतिक गैस के लिए वेग दर (तालिका 8.15 के अनुसार), एम / एस; यू 'एच एक और गैस के लिए एक सामान्य लौ प्रसार दर है, एम / एस; यू एच मीथेन, मैसर्स में लौ प्रसार की दर है।
फिसलन की अधिकतम गति अनुमानित सूत्र द्वारा गणना की जा सकती है:
डब्ल्यू पीआर \u003d 0.73 10 -3 डी के टी 2 (8.31)
पर्याप्त सन्निकटन के साथ एक ही सूत्र को अन्य गैसों के लिए लौ की पीकपोपॉक्टेचर की सामान्य दर में बदलाव के लिए संशोधन की शुरूआत के साथ निर्देशित किया जा सकता है। कई प्रयोगों के आधार पर, आप निम्नलिखित निष्कर्ष निकाल सकते हैं: बर्नर के स्थिर संचालन की सीमा ज्वाला के अलगाव और स्लीप्पॉइंट की गति तक ही सीमित है।
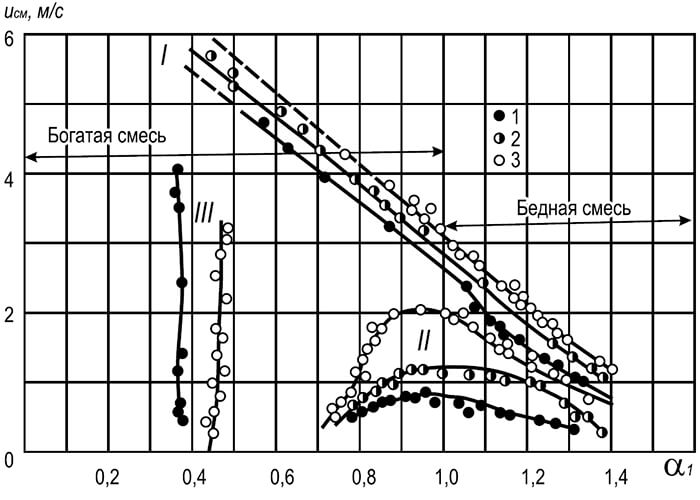
अंजीर। 8.8। गैस-एयर मिश्रण की गति की निर्भरता जिस पर लौ अलग हो जाती है और स्पाइक, प्राथमिक वायु गुणांक से अधिक से
मैं - लौ का पतन; II - लौ स्क्वर्ट; III - लौ के पीले किनारों;
1-3 फायर चैनल बर्नर के व्यास, मिमी: 1 - 25, 2 - 25, 3 - 32
अंजीर में। 8.8 घटता दिखाया गया है कि हवा के साथ प्राकृतिक गैस के मिश्रण की प्रवाह दर की विशेषता है जिसके अंतर्गत लौ का मार्जिन होता है। वक्र की प्रकृति ज्वाला प्रतिरोध में तेज कमी दर्शाती है क्योंकि प्राथमिक वायु मिश्रण में सामग्री बढ़ जाती है। लौ की स्थिरता में वृद्धि तब होती है जब प्राथमिक हवा की सामग्री कम हो जाती है और अधिकतम तक पहुंच जाती है जब यह शून्य हो जाती है (प्रसार जलती हुई)। हालांकि, कई मामलों में हाइड्रोकार्बन गैसों की इस तरह की भूकंप अस्वीकार्य है, क्योंकि इससे पीले रंग की आग की उपस्थिति होती है जो इसमें ऋषि कणों की उपस्थिति को दर्शाती है।
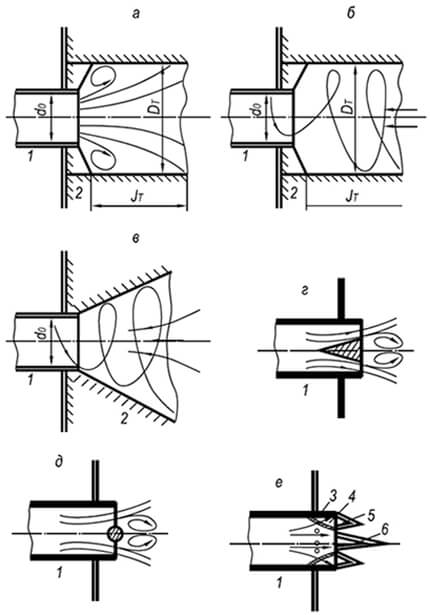
अंजीर। 8.9। सामान्य दहन स्टेबिलाइजर्स
ए - क्षेत्र के अचानक विस्तार के साथ बेलनाकार सुरंग;
बी - वही, जब धारा घूमती है;
बी एक शंकुधारी सुरंग है जब धारा घूम रही है;
जी - एक शंकु शरीर के रूप में स्टेबलाइज़र;
डी - वही, एक गोल रॉड के रूप में;
ई - एक ही, एक स्थिर अंगूठी लौ के रूप में
1 - बर्नर आग नोजल; 2 - सुरंग; 3 - साइड ओपनिंग;
4 - अंगूठी चैनल; 5 - अंगूठी लौ;
6 - गैस-एयर मिश्रण की मुख्य धारा की लौ
अभ्यास में, किसी भी दहनशील गैस-एयर मिश्रणों की जलती स्थिरता की सीमा का विस्तार करने के लिए, प्रवाह दर अलगाव की गति से कई गुना अधिक स्वीकार की जाती है। ज्वाला को अलग करने की रोकथाम दहन स्टेबिलाइजर्स (चित्र 8.9) के उपयोग से हासिल की जाती है।
इंजेक्शन और अन्य बर्नर की ज्वाला को स्थिर करने के लिए एक्सिसिमेट्रिक गैस-एयर जेट्स जारी करने के लिए, अपवर्तक बेलनाकार सुरंगों का उपयोग उनके क्रॉस सेक्शन के अचानक विस्तार के साथ किया जाता है। ऐसी सुरंग का प्रभाव लुढ़का हुआ जेट से उत्पन्न गर्म दहन उत्पादों के भाग के परिधीय परिसंचरण पर आधारित है।
बर्नर की लौ को स्थिर करने के लिए, एक घुमावदार गैस-वायु मिश्रण बकाया, दोनों बेलनाकार और शंकुधारी सुरंगों का उपयोग प्रकटीकरण के कोण के साथ 30-60 डिग्री के साथ किया जाता है। जब सुरंग की परिधि पर धारा घूमती है बड़ा दबावइसके मध्य भाग की तुलना में। इससे गर्म दहन उत्पादों के हिस्से का तेजी से रीसाइक्लिंग होता है और ठंडे गैस-वायु मिश्रण की सुरंग में बहने वाले ठंडे गैस-वायु मिश्रण की इग्निशन।
जब सुरंगों की सेटिंग संभव नहीं है, तो खराब सुव्यवस्थित रूप के निकायों का उपयोग बर्नर के अग्नि चैनल से गैस-एयर मिश्रण के प्रवाह में स्थित लौ को स्थिर करने के लिए किया जाता है। मिश्रण की इग्निशन स्टेबलाइज़र की परिधि पर होती है, जो अंदर से दहनशील मिश्रण को जलाने, गर्म गैसों का आंशिक रीसाइक्लिंग उत्पन्न करती है। ऐसे उपकरणों का स्थिरीकरण प्रभाव सुरंगों से कम है।
इंजेक्शन इकाई में, एक विशेष अग्नि नोजल के रूप में दहन के स्टेबिलाइजर्स का व्यापक रूप से एक या मल्टीफैसेल बर्नर के इंजेक्शन में उपयोग किया जाता है। इस डिवाइस का स्थिरीकरण प्रभाव अतिरिक्त हवा के साथ मशाल की जड़ पर मुख्य धारा को कमजोर पड़ने पर आधारित है, जो इसकी स्थिरता की सीमा को संकुचित करता है, साथ ही साथ अपनी परिधि में मुख्य प्रवाह की अंगूठी लौ को गर्म और उजागर करता है । अलगाव के दौरान अंगूठी की लौ की स्थिरता अग्नि अंगूठी और साइड छेद के पार अनुभागों के इस अनुपात के कारण हासिल की जाती है, जिसमें कणिका गुहा में गैस-वायु मिश्रण की गति सामान्य फैल दर से अधिक नहीं होती है ज्योति। बर्नर मिक्सर में लौ पर्ची को रोकने के लिए, अंगूठी की लौ बनाने वाले साइड छेद का आकार छोटे महत्वपूर्ण द्वारा स्वीकार किया जाता है।
8.9। फायरप्रूफर्स की योजनाएं
वायु या ऑक्सीजन, गैस पाइपलाइन को मारने, विस्फोटक मिश्रण बना सकते हैं, इसलिए पाइपलाइनों को हवा या ऑक्सीजन के प्रवेश से रोकना आवश्यक है। सभी खतरनाक उद्योगों को ऐसी स्थितियों को बनाना चाहिए जो आवेगों को जलाने की संभावना को बाहर कर देते हैं। इग्निशन के स्रोत, जिसके परिणामस्वरूप विस्फोट के लिए गैस-एयर मिश्रण होते हैं, वे हैं:
- खुली लौ;
- मौजूदा विद्युत उपकरणों के विद्युत निर्वहन;
- विद्युत तारों में शॉर्ट सर्किट;
- विद्युत उपकरणों में स्प्रिंग्स;
- खुले फ़्यूज़ का बांध;
- स्थैतिक बिजली निर्वहन।
विस्फोट सुरक्षा विभिन्न फायरप्रोज़र द्वारा प्रदान की जाती है। पाइपलाइनों में, टैंक पर, शुद्ध गैस पाइपलाइनों, मोमबत्तियों और अन्य प्रणालियों पर स्थापित, जहां विस्फोट का खतरा है।
एक दहनशील मिश्रण से भरे चैनल में लौ जनसंख्या केवल न्यूनतम चैनल व्यास के साथ होती है, इस पर निर्भर करती है रासायनिक संरचना और मिश्रण का दबाव, और प्रतिक्रिया क्षेत्र से चैनल दीवारों तक गर्मी के नुकसान के कारण है। चैनल के व्यास में कमी के साथ, इसकी सतह प्रतिक्रियाशील मिश्रण के द्रव्यमान की एक इकाई द्वारा बढ़ जाती है, यानी गर्मी की कमी बढ़ रही है। जब वे एक महत्वपूर्ण मूल्य तक पहुंचते हैं, तो दहन प्रतिक्रिया की दर इतनी कम हो जाती है कि लौ का आगे फैलाव असंभव हो जाता है।
फायरप्रोसेसर की फ्लेविंग क्षमता मुख्य रूप से क्वेंचिंग चैनलों के व्यास पर निर्भर करती है और बहुत कम - उनकी लंबाई से, और परिणामी चैनलों के माध्यम से लौ के प्रवेश की संभावना मुख्य रूप से दहनशील मिश्रण और दबाव की संपत्तियों और संरचना पर निर्भर करती है। सामान्य लौ प्रचार दर प्राथमिक मूल्य है जो क्वेंचिंग चैनलों की मात्रा का आकार निर्धारित करती है और फायरप्रोसेसर प्रकार की पसंद: यह और अधिक कैसे है, छोटे चैनल को लौ को साफ करने के लिए आवश्यक है। इसके अलावा, क्वेंचिंग चैनल के आकार दहनशील मिश्रण के प्रारंभिक दबाव पर निर्भर करते हैं। फायरप्रोज़र की ज्वाला बनाने की क्षमता का आकलन करने के लिए, तथाकथित। पाकले का मानदंड:
Re \u003d w cm dc p p / (rt 0 λ 0) (8.32)
लौ कटाई फॉर्मूला की सीमा में, पेकलेट मानदंड फॉर्म लेता है:
Rec \u003d w cm d cr c p p cr / (rt 0 λ 0) (8.33)
जहां डब्ल्यू सीएम सामान्य लौ प्रसार दर है; डी - विभाजन चैनल का व्यास; डी केपी - तलाक चैनल का महत्वपूर्ण व्यास; सी पी - विशिष्ट गर्मी गर्मी क्षमता 0 डिग्री सेल्सियस और निरंतर दबाव पर; पी - गैस दबाव; आर सीआर - गंभीर गैस दबाव; आर एक सार्वभौमिक गैस स्थिर है; टी 0 गैस का पूर्ण तापमान है; λ 0 - प्रारंभिक मिश्रण की थर्मल चालकता।
इस प्रकार, फायरप्रोसेवर की बेकार क्षमता की गणना के लिए, निम्न स्रोत डेटा आवश्यक है:
- दहनशील गैस मिश्रण की लपटों के प्रसार की सामान्य गति;
- इस फायरप्रोसेसर के अधिकतम क्वेंचिंग चैनलों का वास्तविक आकार।
यदि प्राप्त मूल्य आरईसी \u003d 65 से अधिक है, तो फायरप्रोसेसर इस दहनशील मिश्रण की लौ के प्रसार को रोक नहीं देगा, और इसके विपरीत, यदि फिर से< 65, огнепреградитель задержит распространение пламени. Запас надежности огнепреградителя, который находят из отношения Ре кр к вычисленному значению Ре, должен составлять не менее 2:
पी \u003d आरई सीआर / डी \u003d 65 / पुन: 2.0 (8.34)
लौ क्वेंचिंग की सीमा पर पीछे की स्थिरता के तथ्य का उपयोग करके, किसी भी दहनशील मिश्रण के लिए चैनलों के अनुमानित महत्वपूर्ण व्यास की गणना करना संभव है, यदि लौ प्रसार दर ज्ञात है, साथ ही गर्मी क्षमता और थर्मल चालकता गैस प्रणाली। क्वेंचिंग नहर के निम्नलिखित महत्वपूर्ण व्यास की सिफारिश की जाती है, मिमी:
- गैस-एयर मिश्रण जलते समय - मीथेन के लिए 2.9 और प्रोपेन और ईथेन के लिए 2.2;
- पाइप में ऑक्सीजन मिश्रण जलते समय (दहन उत्पादों के मुक्त विस्तार की निःशुल्क विस्तार की स्थितियों में 0.1 एमपीए के पूर्ण दबाव पर) - मीथेन के लिए 1.66 और प्रोपेन और इथेन के लिए 0.39।
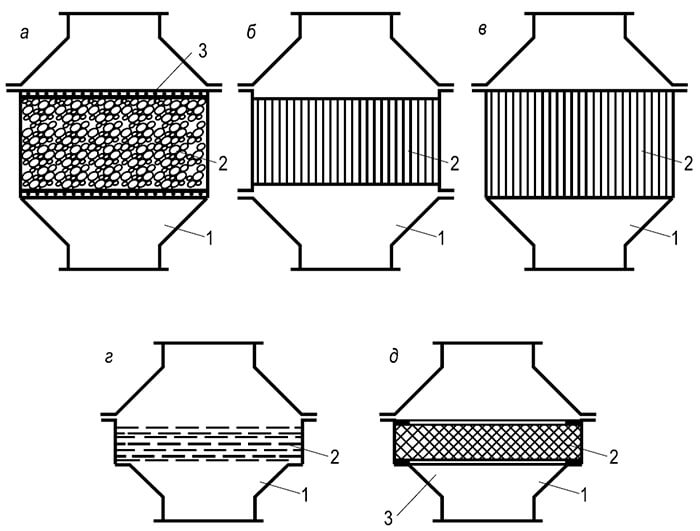
अंजीर। 8.10। फायरप्रोसेसर के प्रकार:
ए - नोजल; बी - कैसेट; में - लैमेलर; जी - जाल; डी - धातु सिरेमिक
रचनात्मक रूप से फायरप्रोसेसर चार प्रकार (चित्र 8.10) में विभाजित हैं:
- दानेदार सामग्री से नोजल के साथ;
- सीधे चैनलों के साथ;
- धातु सिरेमिक या धातु फाइबर से;
- जाल।
स्थापना विधि द्वारा - तीन प्रकारों पर: वायुमंडल में या मशाल में गैसों के उत्सर्जन के लिए पाइप पर; संचार पर; गैस पिघलने वाले उपकरणों से पहले।
जाली के बीच घुड़सवार फायरप्रोसेसर के आवास में फिलर (ग्लास या चीनी मिट्टी के बरतन गेंदों, बजरी, कोरंडम और अन्य ग्रेन्युल के साथ नोजल है टिकाऊ सामग्री)। कैसेट फायरप्रोसेसर एक आवास है जिसमें नालीदार और फ्लैट धातु टेप से एक आतिशबाजी-पीसने वाला कैसेट, कसकर एक रोल में बरकरार रखा गया। प्लेट फायरप्रोसेसर के आवास में, विमान-समांतर धातु प्लेटों का एक पैकेज उनके बीच सख्ती से परिभाषित दूरी के साथ। जाल फायरप्रोसेसर के पास कसकर संपीड़ित का एक पैकेज होता है धातु जाल। धातु-सिरेमिक फायरप्रोसेसर एक आवास है जिसमें एक छिद्रपूर्ण धातु-सिरेमिक प्लेट को एक फ्लैट डिस्क या ट्यूब के रूप में स्थापित किया जाता है।
अक्सर एप्लाइड मेष आतिशबाजी (वे मेरे विस्फोटों को रोकने के लिए माइनिंग दीपक (देवी की दीपक) में xix शताब्दी की शुरुआत में स्थापित होने लगे)। इन आतिशबाजी को उन प्रतिष्ठानों की रक्षा करने की सिफारिश की जाती है जिसमें गैस ईंधन जला दिया जाता है। आतिशबाजी तत्व में 0.25 मिमी के सेल आकार के साथ पीतल जाल की कई परतें होती हैं, जो दो छिद्रित प्लेटों के बीच सैंडविच होती हैं। ग्रिड पैकेज को हटाने योग्य क्लिप में प्रबलित किया जाता है।
फायरप्रोसेसर हाउसिंग कास्ट आयरन या एल्यूमीनियम मिश्र धातु से बना है और उनके बीच स्थित एक हटाने योग्य क्लिप के साथ एक बोल्ट से जुड़े दो समान भागों होते हैं। सूखे फ्लेमर्स, तरल सुरक्षा शटर के अलावा, धातुओं के गैस-बहने में एक विस्फोटक लहर और लौ के प्रवेश से गैस पाइपलाइनों को रोकते हुए, साथ ही साथ पाइपलाइन और उपकरण गैस से भरे हुए ऑक्सीजन और हवा में प्रवेश करने से।
तरल द्वार चाहिए:
- रिवर्स स्ट्राइक के दौरान और गैस इग्निशन के दौरान एक विस्फोटक लहर के प्रसार को रोकें;
- ऑक्सीजन और वायु से गैस पाइपलाइन को सुरक्षित रखें;
- गैस प्रवाह के पारित होने के लिए न्यूनतम हाइड्रोलिक प्रतिरोध प्रदान करें। इसके अलावा, शटर से तरल को ध्यान देने योग्य मात्रा में बूंदों के रूप में नहीं किया जाना चाहिए।
8.10। जलने के सिद्धांत
गैस जलने की प्रक्रियाओं का आधार - सिद्धांतों, पारंपरिक रूप से काइनेटिक और प्रसार के रूप में जाना जाता है। उसी समय, कुछ अतिरिक्त हवा के साथ एक सजातीय मिश्रण दहन की शुरुआत से पहले बनाया जाता है। इस तरह के मिश्रण का दहन सूट कणों की लौ में शिक्षा के बिना एक लघु पारदर्शी मशाल में होता है। गतिशील सिद्धांत के साथ गैस जलाने के लिए, विशेष मिक्सर या इंजेक्शन बर्नर का उपयोग किया जाता है, एक अतिरिक्त वायु गुणांक α 1 \u003d 1.02: 1.05 के साथ एक सजातीय गैस-एयर मिश्रण तैयार करना।
गतिशील सिद्धांत पर प्राथमिक हवा की एक छोटी सामग्री के साथ, गैस के साथ मिश्रण में ऑक्सीजन के उपयोग से पहले, केवल जलने का प्रारंभिक चरण आगे बढ़ाया जाता है। ऑक्सीजन (द्वितीयक वायु) के बाहरी प्रसार के कारण शेष गैसों और अपूर्ण दहन उत्पादों को जला दिया जाता है, यानी सिद्धांत में डी और एफ एफ यू एस और ओ एन ओ एम के लिए। Α 1 पर।< 1 у факела есть два видимых фронта горения: внутренний, возникающий за счет первичного воздуха, и наружный, образующийся за счет диффузии кислорода из व्यापक। लौ की कुल ऊंचाई इतनी जलती हुई है, और तापमान कुछ हद तक घट रहा है। लौ और इसकी पारदर्शिता की स्थिरता मिश्रण में प्राथमिक हवा की सामग्री पर निर्भर करती है: उच्च, लौ की स्थिरता कम, अधिक पारदर्शिता, और इसके विपरीत।
Α 1 के साथ गैस जलती हुई सिद्धांत< 1,0 является п р о м е ж у т о ч н ы м (между кинетическим и диффузионным). С учетом этого принципа конструируются все गैस वाहनों इंजेक्शन बर्नर के साथ। ऐसे बर्नर में, मिश्रण में प्राथमिक हवा की सामग्री गैस के प्रकार के आधार पर की जाती है ताकि:
- लौ में कोई ऋषि कण नहीं थे;
- प्रैक्टिस में आवश्यक किसी भी सीमा में थर्मल पावर को बदलते समय दहन स्थिरता सुनिश्चित की गई थी।
एक प्रसार सिद्धांत (α 1 \u003d 0) के साथ, दहन और मिश्रण प्रक्रिया समानांतर में विकसित हो रही है। चूंकि मिश्रण प्रक्रियाओं में काफी धीमी गति से दहन प्रक्रियाएं होती हैं, इसलिए दहन की गति और पूर्णता गैस और वायु मिश्रण की गति और पूर्णता से निर्धारित की जाती है। हवा के साथ गैस का मिश्रण प्रसार (या धीमी आणविक या अशांत, अंतिम चरण के रूप में आणविक सहित) द्वारा हो सकता है। तदनुसार, दहन दर और प्रसार ज्वाला संरचना अलग-अलग है।
इस तरह की जलन की विशेषताएं:
- पृथक्करण की शर्तों के तहत शून्य से थर्मल पावर को शून्य से बदलते समय लौ प्रतिरोध;
- लौ की पूरी ऊंचाई पर तापमान की स्थिरता;
- बड़ी मनमानी सतहों के लिए इसे वितरित करने की क्षमता;
- बर्नर की कॉम्पैक्टनेस और उनके निर्माण की सादगी;
- लौ की एक महत्वपूर्ण ऊंचाई और पायरोलिटिक प्रक्रियाओं की अनिवार्यता एक उज्ज्वल ऋषि लौ के गठन की ओर अग्रसर है।
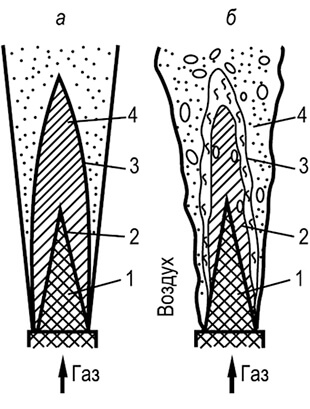
अंजीर। 8.11। ढीली लपटों की संरचना:
ए - लैमिनार लौ; बी - अशांत लौ
यदि मिश्रण दहन प्रक्रियाओं से आगे होगा तो डिफ्यूजन दहन को एक गतिशील या मध्यवर्ती में अनुवादित किया जा सकता है। व्यावहारिक रूप से, इसे एक पारदर्शी मशाल में संयोजन, α 1\u003e 1.0 के साथ अर्ध-सजातीय गैस-एयर मिश्रण के गठन के लिए मजबूर वायु आपूर्ति हासिल की जा सकती है।
अंजीर में दहन सिद्धांतों को चित्रित करने के लिए। 8.11। मुफ्त मशालों की योजनाएं दिखायी जाती हैं: लैमिनार और अशांत। गैमिनार मशाल गैस और हवा के पारस्परिक आणविक प्रसार के कारण उठता है। शंकु कर्नेल के अंदर 1 लैमिनेर प्रवाह मोड के दौरान ट्यूब से बहने वाली शुद्ध गैस है। जोन 2 में - जोन 3 में गैस और दहन उत्पादों का मिश्रण - दहन और वायु उत्पादों का मिश्रण। सीमा 4 लौ का एक चिकनी शंकु मोर्चा है, जिसके लिए वायु अणु बाहर फैलते हैं, और अंदर से - गैस अणु। दहन उत्पाद आंशिक रूप से गैस से मिलने के लिए फैलता है, इसे निलंबन क्षेत्र में गहन रूप से हीटिंग करता है। यह हाइड्रोकार्बन के पायरोलिसिस और ऋषि कणों के गठन की ओर जाता है जो लपटों को उज्ज्वल चमकता देता है।
मिक्सिंग प्रवाह के तर्बुलाइजेशन के कारण दहन को तेज किया जा सकता है। एक अशांत मशाल में कोई स्पष्ट शंकु जलती हुई नहीं है, यह अलग-अलग कणों पर लहरों के साथ "धुंधला" और खंडित है।
लौ की संरचना में शुद्ध गैस 1 का एक कोर होता है, अपेक्षाकृत धीमी जलती हुई 2 का क्षेत्र, सबसे तीव्र दहन 3 का धुंधला क्षेत्र दहन उत्पादों की उच्च सामग्री और एक दहन क्षेत्र 4 के साथ एक दहन क्षेत्र 4 के साथ इसमें हवा के एक प्रमुखता के साथ होता है । ज़ोन के बीच स्पष्ट रूप से स्पष्ट सीमाएं नहीं हैं, वे प्रवाह तर्बलीकरण की डिग्री के आधार पर लगातार स्थानांतरित हो जाते हैं। एक अशांत मशाल की विशिष्टताएं हैं:
- जलने की प्रक्रिया का प्रवाह लगभग सभी मात्रा में है;
- बढ़ती जलती हुई तीव्रता;
- बड़ी लौ पारदर्शिता;
- पृथक्करण की ओर इसकी स्थिरता को बागर करें।
अशांत गैस जलने का व्यापक रूप से विभिन्न बॉयलर और स्टोव की भट्टियों में उपयोग किया जाता है। दहन प्रक्रिया को तेज करने के लिए, प्राकृतिक (गति बढ़ाने के द्वारा) और कृत्रिम, प्रवाह के उग्रकरण, जैसे वायु प्रवाह की घुमावदार और विभिन्न कोणों में पतली गैस जेट्स के विभिन्न कोणों पर इसे आपूर्ति करना।
8.11। अपूर्ण दहन उत्पादों के गठन के लिए शर्तें और हानिकारक पदार्थों की एकाग्रता में कमी
जब दहनशील गैसों का दहन, दहन उत्पादों में पूर्ण (कार्बन डाइऑक्साइड और जल वाष्प) और अपूर्ण दहन (कार्बन मोनोऑक्साइड, हाइड्रोजन, असंतृप्त, संतृप्त, सुगंधित, सुगंधित हाइड्रोकार्बन और ऋषि कण) दोनों के घटक हो सकते हैं। इसके अलावा, नाइट्रोजन ऑक्साइड हमेशा दहन उत्पादों में पाया जाता है। महत्वपूर्ण सांद्रता में अपूर्ण दहन उत्पादों की उपस्थिति अस्वीकार्य है, क्योंकि यह वायुमंडल विषाक्त पदार्थों के प्रदूषण की ओर जाता है और गैस ईंधन पर चल रहे प्रतिष्ठानों की दक्षता में कमी आती है।
उनकी बड़ी सामग्री के मुख्य कारण:
- अपर्याप्त हवा के साथ गैसों को जलाना;
- जलने की प्रक्रिया से पहले और अंदर दहनशील गैसों और हवा का खराब मिश्रण;
- जब तक दहन प्रतिक्रिया पूरी नहीं हो जाती तब तक अत्यधिक लौ शीतलन।
मीथेन दहन प्रतिक्रिया के लिए (प्रतिक्रियाशील मिश्रण में ऑक्सीजन एकाग्रता के आधार पर) निम्नलिखित समीकरणों द्वारा वर्णित किया जा सकता है:
सीएच 4 + 2 ओ 2 \u003d सीओ 2 + 2 एन 2 ओ + 800.9 एमजे / एमओएल
एक stoichiometric अनुपात के साथ या ऑक्सीडेंट के अतिरिक्त में;
सीएच 4 + ओ 2 \u003d सीओ + एच 2 + एच 2 ओ + क्यू और सीएच 4 + 0.5o 2 \u003d सीओ + 2 एन 2 ओ + क्यू
ऑक्सीडेंट के नुकसान के साथ।
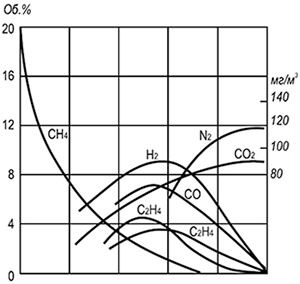
अंजीर। 8.12। इंटरमीडिएट दहन उत्पाद
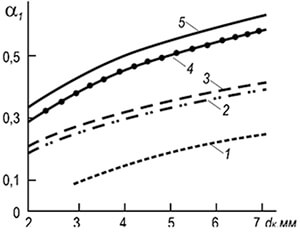
अंजीर। 8.13। प्राथमिक वायु सामग्री
जिसमें शिक्षा को रोका जाता है
लौ में पीले रंग की भाषाएं
गैस: 1 - कोक;
2 - प्राकृतिक गैस जमा;
3 - तेल जमा;
4 - प्रोपेन; 5 - भूटान
अंजीर में। 8.12 कुछ मध्यवर्ती यौगिकों की अनुमानित औसत संरचना - हाइड्रोजन, कार्बन ऑक्साइड, ईथिलीन, एसिटिलीन और अपेक्षाकृत छोटी संख्या संतृप्त और सरल सुगंधित यौगिकों की एक अपेक्षाकृत छोटी संख्या दिखाती है - और प्राकृतिक गैस (9 7%) के प्रसार जलने के साथ लौ में उत्पन्न कार्बन डाइऑक्साइड। गैस जलने का उत्पादन एक लैमिनेर मशाल में किया गया था, गैस 12 मिमी व्यास के साथ एक पाइप से बहती थी। कुल लौ ऊंचाई 130-140 मिमी।
ज्वाला की लगभग एक ऊंचाई पर हाइड्रोजन और एसिटिलीन की अधिकतम एकाग्रता हासिल की जाती है, वे लौ चमकते क्षेत्र के शीर्ष पर लगभग एक साथ गायब हो जाते हैं। लौ में बने सभी मध्यवर्ती यौगिकों में से (ऋषि कणों को छोड़कर) कार्बन ऑक्साइड आखिरी गायब हो जाता है। यह गैस दहन की पूर्णता पर अपने सूचकांक का न्याय करने का कारण देता है। दहन उत्पादों में, नाइट्रोजन ऑक्साइड हमेशा मौजूद होते हैं, अधिकतम एकाग्रता कार्बन मोनोऑक्साइड और हाइड्रोजन के गहन बर्नआउट के क्षेत्रों में होती है।
ऑक्सीडाइज़र के नुकसान के साथ हाइड्रोकार्बन गैसों की जलन सूट के कणों के गठन की ओर ले जाती है जो लौ पीले रंग का रंग देती है। साबुन जलती हुई प्रक्रिया स्टेडियम और अपेक्षाकृत धीमी हो जाती है। कभी-कभी कालिख के परिणामी कणों के बर्नआउट में देरी हो जाती है और इसे मशाल के निम्न तापमान वाले क्षेत्र के प्रवेश द्वार पर पूरी तरह से बंद किया जा सकता है या जब लौ गर्मी विनिमय सतहों की लौ से धोया जाता है। इस प्रकार, एक चमकदार लौ की उपस्थिति हमेशा पायरोलिटिक प्रक्रियाओं के प्रवाह और दहन की रासायनिक अपूर्णता की संभावना को दर्शाती है, खासकर बॉयलर के छोटे आकार के ढाल वाले फ़ायरबॉक्स में।
ऋषि कणों के गठन को रोकना हाइड्रोकार्बन गैसों के प्रारंभिक मिश्रण द्वारा पर्याप्त मात्रा में ऑक्सीकरण एजेंट के साथ हासिल किया जाता है। मिश्रण में प्राथमिक वायु सामग्री जिसमें पारदर्शी लौ होती है, यह न केवल हाइड्रोकार्बन के प्रकार पर निर्भर करती है, बल्कि द्वितीयक हवा (बर्नर के अग्नि चैनलों के व्यास) के साथ मिश्रण की शर्तों पर भी निर्भर करती है (चित्र 8.13 )। सीमा पर और लौ के घटता के ऊपर पारदर्शी रूप से, और घटता के नीचे पीले रंग की जीभ होती है। वक्र दिखाते हैं कि मिश्रण में प्राथमिक हवा की सामग्री अणु में कार्बन परमाणुओं की संख्या और बर्नर के अग्नि चैनलों के व्यास को बढ़ाने के साथ बढ़ जाती है। मिश्रण में प्राथमिक वायु गुणांक α 1 की अतिरिक्त, जिसमें निर्दिष्ट कारकों के आधार पर पीले रंग की लपटें गायब हो जाती हैं, बर्नर के छोटे फायर चैनलों के लिए निर्धारित की जा सकती हैं:
α 1 \u003d 0.12 (एम + एन / 4) 0.5 (डी के / डी 0) 0.25 (8.35)
जहां एम और एन अणु में कार्बन और हाइड्रोजन परमाणुओं की संख्या या जटिल गैस के लिए औसत संख्या; डी के - बर्नर, मिमी के आग चैनल का व्यास; डी 0 - बर्नर चैनल (1 मिमी) का संदर्भ व्यास।
में पूर्ण दहन सुनिश्चित करना व्यावहारिक स्थितियां - न केवल जलने वाले गैस के सिद्धांत पर बल्कि घुमावदार मात्रा में लौ के विकास की स्थितियों पर भी काफी जटिल है। दहन की पूर्णता पर उच्चतम मांग प्रस्तुत की जाती है घरेलू तंत्र और अन्य प्रतिष्ठान दहन उत्पादों को वायुमंडल में छोड़ देते हैं। ऐसी प्रतिष्ठानों में गैस का दहन सबसे कठिन है, क्योंकि यह ठंड गर्मी विनिमय सतहों की लौ के साथ धोने से जुड़ा हुआ है। घरेलू प्लेटों में गैस जलाने के लिए, इंजेक्शन मल्टीफैसेल बर्नर का उपयोग किया जाता है, जिसमें अतिरिक्त प्राथमिक वायु α 1 के गुणांक के साथ एक सजातीय मिश्रण बनाते हैं< 1. Недостающий для сгорания газа воздух поступает за счет диффузии из окружающей атмосферы.
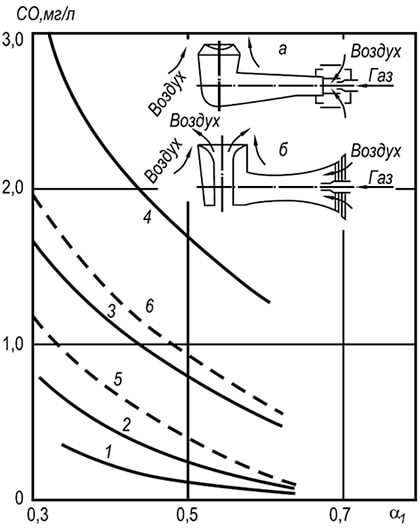
अंजीर। 8.14। कार्बन ऑक्साइड की एकाग्रता
एक गैस स्टोव में दहन उत्पादों में
एक - द्वितीयक हवा की परिधीय आपूर्ति के साथ बर्नर;
बी - द्वितीयक हवा के केंद्रीय और परिधीय भोजन के साथ
1 - प्राकृतिक गैस, परिधीय के साथ बर्नर
माध्यमिक हवा, व्यंजनों के नीचे की दूरी 25 मिमी;
2-4 - प्राकृतिक गैस, परिचयी के साथ बर्नर और
द्वितीयक हवा, दूरी की केंद्रीय पनडुब्बी
बर्तन के नीचे, मिमी: 2 - 25, 3 - 18, 4 - 10;
5 – द्रवीभूत गैस, केंद्रीय और परिधीय के साथ बर्नर
माध्यमिक हवा की पनडुब्बी, व्यंजनों के नीचे की दूरी 25 मिमी;
6 - तरलीकृत गैस, परिधीय के साथ बर्नर
अंजीर में। 8.14 घर के लिए 2-कोरिफ़ोरस बर्नर के सर्किट दिखाता है गैस प्लेट्स और नाममात्र थर्मल पावर के साथ बर्नर के संचालन के दौरान प्राकृतिक मीथेन (वॉल्यूम द्वारा 95%) और प्रोपेन (वॉल्यूम द्वारा 93%) के दहन उत्पादों में कार्बन ऑक्साइड कंपनी की औसत एकाग्रता। बर्नर में अंतर यह है कि द्वितीयक हवा केवल परिधि से, और दूसरी तरफ परिधि से और केंद्रीय चैनल से प्रदान की जाती है।
गैस दहन की पूर्णता मिश्रण में प्राथमिक हवा की अधिकता पर निर्भर करती है, बर्नर के अग्नि चैनलों की दूरी पर व्यंजनों के नीचे, ईंधन गैस का रूप, द्वितीयक हवा की आपूर्ति करने की विधि। साथ ही, मिश्रण में प्राथमिक हवा की सामग्री में वृद्धि के साथ-साथ बर्नर से दूरी तक की वृद्धि के साथ-साथ व्यंजनों के नीचे तक की वृद्धि से दहन उत्पादों में कार्बन ऑक्साइड की एकाग्रता में कमी आती है। कार्बन ऑक्साइड की न्यूनतम एकाग्रता अतिरिक्त प्राथमिक वायु α 1 \u003d 0.6 और ऊपर के गुणांक से मेल खाती है और बर्नर से दूरी 25 मिमी के व्यंजनों के नीचे तक, और अधिकतम - α 1 \u003d 0.3 और नीचे और दूरी से संबंधित है बर्नर 10 मिमी व्यंजन के नीचे। इसके अलावा, गैस के दबाव को बढ़ाकर 15-20% तक बर्नर की थर्मल पावर में वृद्धि 1.2-1.3 गुना के दहन उत्पादों में कार्बन ऑक्साइड की एकाग्रता में वृद्धि की ओर बढ़ती है, और गर्मी के कारण गैस का दहन - 1.5-2 बार में।
सुगंधित यौगिकों के दहन की प्रक्रिया में उपस्थिति पर - बेंजीन, पॉलीसाइक्लिक बेंजपीरिन, गैर-कानून, आदि - विशेष ध्यान दिया जाना चाहिए, क्योंकि उनमें से कुछ कैंसरजन्य हैं। उनके गठन की प्रक्रिया बहुत जटिल है और स्टेडियम आय है। पहले चरण में, एसिटिलीन और इसके डेरिवेटिव दिखाई देते हैं। लौ क्षेत्र में, ये पदार्थ ट्रिपल कार्बन संबंधों के पुनर्गठन के साथ श्रृंखला को बढ़ाने की प्रक्रियाओं से गुजरते हैं। चक्रवात और निर्जलीकरण के परिणामस्वरूप, पॉलीसाइक्लिक समेत विभिन्न सुगंधित यौगिकों के उद्भव की ओर अग्रसर होता है।
तालिका 8.16। कार्बन मोनोऑक्साइड और बेंज (ए) के दहन उत्पादों में औसत एकाग्रता, पाइरेन के प्रकार के आधार पर, बर्नर का प्रकार और प्राथमिक वायु (थर्मल बर्नर लोड - 1600 किलो कैल / एच, द दूरी से बर्नर के नीचे बर्नर - 24-26 मिमी)
| बर्नर का प्रकार | औसत सांद्रता | |
|---|---|---|
| कार्बन ऑक्साइड, एमजी / एल (α \u003d 1.0 के संदर्भ में) |
बेंज (ए) पाइरेन, μg / 100 मीटर 3 |
|
| प्राकृतिक गैस | ||
α i \u003d 0.60 ÷ 0,70 पर |
0,10 | नहीं मिला |
α i \u003d 0.30 ÷ 0.35 पर |
1,20 | निशान |
α i \u003d 0.60 ÷ 0,70 पर |
0,50 | नहीं मिला |
α i \u003d 0.30 ÷ 0.35 पर |
0,12 | नहीं मिला |
| तरलीकृत हाइड्रोकार्बन गैस | ||
| द्वितीयक हवा के परिधीय पनडुब्बी के साथ बर्नर: | ||
α i \u003d 0.60 ÷ 0,70 पर |
0,30 | 0,03 |
α i \u003d 0.30 ÷ 0.35 पर |
1,20 | 1,10 |
| द्वितीयक हवा के केंद्रीय और परिधीय पनडुब्बियों के साथ बर्नर: | ||
α i \u003d 0.60 ÷ 0,70 पर |
0,07 | 0,02 |
α i \u003d 0.30 ÷ 0.35 पर |
1,00 | 0,045 |
विवरण सारणी। 8.16 से पता चलता है कि प्राथमिक वायु गुणांक α 1 \u003d 0.6 और अधिक प्रकार के बर्नर पर अधिक के साथ प्राकृतिक गैसों को जलाते समय, दहन उत्पादों के कार्बन ऑक्साइड की एकाग्रता गोस्ट 5542-87 की आवश्यकताओं को पूरा करती है।
तालिका 8.17। इंजेक्शन सिंगल-पंक्ति बर्नर के फायर चैनलों के किनारों के बीच की दूरी, उनके आकार और ओवरटाइम वायु गुणांक के आधार पर
| फायर चैनल व्यास, मिमी | चैनलों के किनारों के बीच दूरी, एमएम जब विभिन्न मूल्य आउटलेट एयर गुणांक α 1 | ||||
|---|---|---|---|---|---|
| 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | |
| 2,0 | 11 | 8 | 6 | 5 | 4 |
| 3,0 | 15 | 12 | 9 | 7 | 5 |
| 4,0 | 16 | 14 | 11 | 9 | 7 |
| 5,0 | 18 | 15 | 14 | 12 | 10 |
| 6,0 | 20 | 18 | 16 | 14 | 12 |
अध्ययनों से पता चला है कि फायरवेस्टर्स के किनारों के बीच की दूरी, लौ का तेजी से फैलती है, जिससे उनके विलय को रोकना उनके आकार और मिश्रण में प्राथमिक हवा की सामग्री पर निर्भर करता है, इसकी वृद्धि के साथ घटता है। इष्टतम दूरी चैनलों के किनारों के बीच, गैस के दहन और लौ के तेज़ फैलाव की पर्याप्त पूर्णता प्रदान करने, तालिका में दिखाए जाते हैं। 8.17। जब एक चेकर आदेश में दो पंक्तियों में आग चैनल व्यवस्थित होते हैं, तो किनारों के बीच की दूरी एक ही तालिका के साथ स्वीकार की जा सकती है। पंक्तियों के बीच की दूरी चैनलों के बीच की दूरी 2-3 गुना होनी चाहिए।
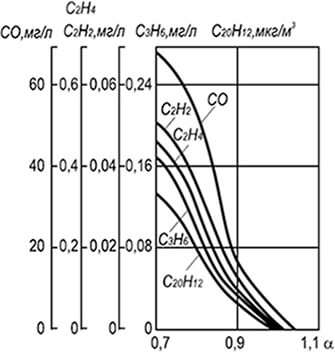
अंजीर। 8.15। कार्बन ऑक्साइड एकाग्रता, एसिटिलीन,
दहन उत्पादों में इथेन, ईथिलीन और बेंज (ए) पाइरेन
इंजेक्शन बर्नर में मध्य दबाव गैस
कई प्रयोगात्मक डेटा के सामान्यीकरण ने विभिन्न घटकों के दहन उत्पादों में औसत एकाग्रता घटता प्राप्त करना संभव बना दिया, जो गुणात्मक रूप से गुणात्मक रूप से और दहन प्रक्रिया को मापता है (चित्र 8.15)। सजातीय गैस-वायु मिश्रण का पूर्ण दहन केवल प्राथमिक वायु गुणांक α \u003d 1.05 और उच्चतम के साथ ही हासिल किया जाता है। मिश्रण में हवा की मात्रा में कमी के साथ, विशेष रूप से जब α< 1,0, возрастает концентрация оксида углерода СО, ацетилена С 2 Н 2 , этилена С 2 Н 4 , пропилена С 3 Н 6 и пропана С 3 Н 8 , а также бенз(а)-пирена С 20 Н 9 . Также возрастает концентрация и других компонентов - водорода, бензола и др.
चर्चा किए गए दहन उत्पादों के अलावा, हमेशा नाइट्रोजन ऑक्साइड की कुछ मात्रा होती है, जो मुख्य दहन प्रतिक्रियाओं और दहन प्रक्रिया में पूरा होने के बाद दोनों उच्च तापमान में होती है। नो एक्स की अधिकतम एकाग्रता गैस के बर्नआउट और हाइड्रोजन और कार्बन ऑक्साइड के रूप में मध्यवर्ती उत्पादों के गहन दहन के लिए अंतिम चरणों में होती है।
प्राथमिक यौगिक जब गैस-एयर मिश्रणों का दहन - नाइट्रोजन ऑक्साइड। श्रृंखला प्रतिक्रिया की शुरुआत आणविक ऑक्सीजन के विघटन के कारण उच्च तापमान में उत्पन्न परमाणु ऑक्सीजन से जुड़ी होती है:
ओ 2 -\u003e 2 ओ - 4 9 0 केजे / एमओएल (8.36)
ओ + एन 2 -\u003e नहीं + एन - 300 केजे / एमओएल (8.37)
N + O 2 -\u003e 2NO + 145 KJ / MOL (8.38)
संतुलन प्रतिक्रिया
N 2 + O 2 -\u003e 2NO - 177 KJ / MOL (8.39)
परमाणु ऑक्सीजन का गठन दहन उत्पादों के आंशिक विघटन के दौरान होता है: तापमान और ऑक्सीजन में कमी के साथ, गठित नाइट्रोजन ऑक्साइड (मात्रा द्वारा 1-3%) का एक हिस्सा नाइट्रोजन डाइऑक्साइड संख्या 2 तक ऑक्सीकरण किया जाता है। नाइट्रोजन ऑक्साइड के वातावरण में रिलीज के बाद सबसे तीव्र प्रतिक्रिया आगे बढ़ती है। मूल प्रभाव कारक:
- प्रतिक्रिया क्षेत्रों में तापमान;
- अतिरिक्त वायु गुणांक और प्रतिक्रिया घटकों के संपर्क समय।
लौ का तापमान गैस की रासायनिक संरचना, गैस-वायु मिश्रण में वायु सामग्री, इसकी एकरूपता की डिग्री और प्रतिक्रिया क्षेत्र से गर्मी सिंक की डिग्री पर निर्भर करता है। नाइट्रोजन ऑक्साइड की अधिकतम संभव एकाग्रता, के बारे में। % सूत्र द्वारा गणना की जा सकती है
कोई पी \u003d 4,6 ई -2150 / (आरटी) / 2 एन 2 (8.40)
जहां कोई पी नाइट्रोजन ऑक्साइड की संतुलन एकाग्रता नहीं है, के बारे में। %; आर एक सार्वभौमिक गैस स्थिर है; टी - पूर्ण तापमान, करने के लिए; ओ 2 और एन 2 - एकाग्रता, के बारे में। %, क्रमशः ऑक्सीजन और नाइट्रोजन।
नाइट्रोजन ऑक्साइड की उच्च सांद्रता, एक संतुलन के साथ प्रतिपूर्ति, शक्तिशाली भाप जनरेटर और उच्च तापमान मार्टन, कोक और इसी तरह की भट्टियों में भट्टियों में गैस जलती है। छोटे और मध्यम शक्ति बॉयलर में, छोटे हीटिंग और थर्मल फर्नेस में एक महत्वपूर्ण गर्मी सिंक और उच्च तापमान वाले क्षेत्रों में निवास घटकों के निम्न समय के साथ, नाइट्रोजन ऑक्साइड की उपज परिमाण का क्रम कम है। इसके अलावा, उच्च तापमान क्षेत्र में प्रतिक्रियाशील घटकों के निवास का समय छोटा, दहन उत्पादों में कम नाइट्रोजन ऑक्साइड।
विकिरण बर्नर में गैस का दहन और एक तरल पदार्थ में भी प्रभावी होता है: इन मामलों में, प्रतिक्रिया क्षेत्र से बहुत तीव्र गर्मी के साथ एक अतिरिक्त वायु गुणांक α \u003d 1.05 के साथ एक सजातीय गैस-एयर मिश्रण के माइक्रोफोकर दहन होता है। विकिरण बर्नर में गैस जलने के दौरान नाइट्रोजन ऑक्साइड की एकाग्रता लगभग 40 है, और एक तरल पदार्थ बिस्तर में - 80-100 मिलीग्राम / एम 3। तरल पदार्थ बिस्तर में मशाल और अपवर्तक अनाज उत्सर्जित करने के आग चैनलों के आकार को कम करने से नाइट्रोजन ऑक्साइड की उपज को कम करने में मदद मिलती है।
संचित डेटा ने बॉयलर-हीटिंग उपकरण के डिजाइन में कई बदलावों को संभव बनाया, न केवल अपूर्ण दहन उत्पादों की उच्च दक्षता और कम एकाग्रता प्रदान की, बल्कि नाइट्रोजन ऑक्साइड के वातावरण में कम रीसेट भी प्रदान किया। इन परिवर्तनों में शामिल हैं:
- उच्च तापमान सुरंगों की लंबाई को कम करना और भट्ठी में उन्हें जलाने को स्थानांतरित करना;
- एक खराब जोड़ा आकार या अंगूठी लौ के शरीर के रूप में जलती हुई स्टेबिलाइजर्स के सिरेमिक सुरंगों के बजाय आवेदन;
- एक फ्लैट लौ मशाल का संगठन एक बढ़ी हुई गर्मी हस्तांतरण सतह के साथ;
- बर्नर की संख्या में वृद्धि या ब्लॉक बर्नर का उपयोग करने के कारण ज्वाला फैलाव;
- प्रतिक्रिया क्षेत्र को कदमित वायु आपूर्ति;
- भट्ठी में गर्मी प्रवाह, भट्ठी की ढाल और स्क्रीन डिब्बों पर उनके अलगाव में समान वितरण;
- गैस जलने के प्रसार सिद्धांत का उपयोग (प्रसार दहन केवल उन मामलों में अनुमत है जहां लौ के मुक्त विकास हीट एक्सचेंज सतहों को धोने के बिना प्रदान किए जा सकते हैं)।
कई तरीकों का उपयोग करते समय नाइट्रोजन ऑक्साइड उपज में सबसे प्रभावी कमी हासिल की जाती है।
गैस जलती निम्नलिखित प्रक्रियाओं का एक संयोजन है:
· हवा के साथ एक दहनशील गैस मिलाकर,
गर्म मिश्रण,
दहनशील घटकों की थर्मल अपघटन,
· टॉर्च और गहन गर्मी उत्पादन के गठन के साथ एयर ऑक्सीजन के साथ सूजन और रासायनिक यौगिक दहनशील घटक।
प्रतिक्रिया द्वारा मीथेन जलती हुई होती है:
सीएच 4 + 2 ओ 2 \u003d सीओ 2 + 2 एन 2
गैस के दहन के लिए आवश्यक शर्तें:
· दहनशील गैस और हवा के आवश्यक दहन को सुनिश्चित करना,
· इग्निशन तापमान के लिए हीटिंग।
यदि गैस-वायु गैस मिश्रण में इग्निशन की निचली सीमा से कम है, तो यह जला नहीं जाएगा।
यदि इग्निशन की ऊपरी सीमा की तुलना में गैस-एयर मिश्रण में अधिक गैस है, तो इसे पूरी तरह से जलाया नहीं जाएगा।
गैस के पूर्ण दहन के उत्पादों की संरचना:
सीओ 2 - कार्बन डाइऑक्साइड
· एच 2 ओ - पानी के जोड़ों
* एन 2 - नाइट्रोजन (यह जलने के दौरान ऑक्सीजन के साथ प्रतिक्रिया नहीं करता है)
गैस के अपूर्ण दहन के उत्पादों की संरचना:
· सह - कार्बन मोनोऑक्साइड
सी - कालिख।
प्राकृतिक गैस के 1 मीटर 3 के दहन के लिए, 9.5 मीटर 3 हवा की आवश्यकता है। लगभग वायु प्रवाह हमेशा अधिक होता है।
रवैया वैध प्रवाहसैद्धांतिक रूप से हवा आवश्यक प्रवाहइसे एक अतिरिक्त वायु गुणांक कहा जाता है: α \u003d l / l t।,
कहाँ: एल - मान्य प्रवाह;
एल टी - सैद्धांतिक रूप से आवश्यक खपत।
अतिरिक्त वायु गुणांक हमेशा एक से अधिक होता है। प्राकृतिक गैस के लिए, यह 1.05 - 1.2 है।
2. बहने वाले पानी के हीटर की उद्देश्य, डिवाइस और मुख्य विशेषताएं.
गैस वॉटर हीटर बहती है। पानी हीटिंग के लिए बनाया गया है विशिष्ट तापमान एक जल उपचार के साथ .. फ्लो वॉटर हीटर थर्मल पावर द्वारा विभाजित हैं: 33600, 75600, 105000 केजे, स्वचालन की डिग्री के अनुसार - उच्चतम और प्रथम श्रेणी में। केपीडी। वॉटर हीटर 80%, 0.05% से अधिक की ऑक्साइड सामग्री, 180 0 सी से कम के बोझ के लिए दहन उत्पादों का तापमान। सिद्धांत पानी आधारित अवधि के दौरान गर्मी हीटिंग पर आधारित है।
बहने वाले पानी के हीटर के मुख्य नोड्स हैं: एक गैस-पिघलने वाला उपकरण, हीट एक्सचेंजर, स्वचालन प्रणाली और एक गैस फ़ीड। गैस कम दबाव इंजेक्शन बर्नर में सेवा की। दहन उत्पाद हीट एक्सचेंजर के माध्यम से गुजरते हैं और चिमनी में छुट्टी दी जाती हैं। दहन की गर्मी हीट एक्सचेंजर के माध्यम से बहने वाले पानी के माध्यम से फैलती है। ठंडा करने के लिए आग कक्ष एक तार के रूप में कार्य करता है, जिसके माध्यम से पानी कैनोरियर के माध्यम से फैलता है। गैस बहने वाले पानी के हीटर गैस खिलाने वाले उपकरणों और बोझ से लैस होते हैं, जो अल्पकालिक उल्लंघन के मामले में, कर्षण गैस पिघलने वाले डिवाइस की लौ को रोकते हैं। चिमनी में शामिल होने के लिए धूम्रपान नोजल है।
गैस बहती वॉटर हीटर -VPG।आवरण की अगली दीवार पर हैं: एक गैस क्रेन नियंत्रण घुंडी, एक विद्युत चुम्बकीय वाल्व स्विचिंग बटन और फास्टनर और मुख्य बर्नर की आग की निगरानी के लिए एक अवलोकन विंडो। डिवाइस के शीर्ष पर एक चिमनी डिवाइस है, गैस और जल प्रणाली में उपकरण को संलग्न करने के लिए निचले पाइप होते हैं। गैस प्रवेश करती है। सोलेनोइड वाल्वपानी गैस-पिघला हुआ ब्लॉक का गैस लॉकिंग वाल्व इग्निशन बर्नर और मुख्य बर्नर को गैस की आपूर्ति पर अनुक्रमिक स्विचिंग प्रदान करता है।
मुख्य बर्नर को गैस रसीद को अवरुद्ध करना, जब अनिवार्य कार्य Stobnant Thermocouple से ऑपरेटिंग एक विद्युत चुम्बकीय वाल्व करता है। पानी के उपचार की उपस्थिति के आधार पर मुख्य बर्नर को गैस की आपूर्ति को अवरुद्ध करना, एक वाल्व द्वारा पानी ब्लॉक झिल्ली से एक रॉड के माध्यम से ड्राइव किया जाता है।