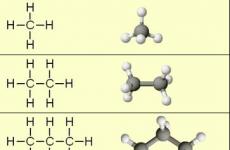
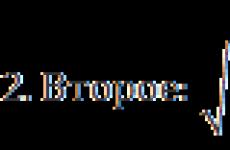Охорона праці в авіації. Елементи теорії самозаймання. Температура самонагрівання. Відмінність самозаймання від самозаймання і запалювання - Вогнегасні склади
Згідно теплової теорії, під температурою самозаймання розуміють найнижчу температуру речовини (матеріалу, суміші), при якій відбувається різке збільшення швидкості екзотермічних реакцій, що закінчуються виникненням полум'яного горіння. На рис. 2.3 такою температурою є температура Т з, Відповідна точці В, В якій лінія тепловідведення q 2 стосується лінії тепловиділення.
Вимірювання температури Т з практично дуже складно, що зумовлено великими швидкостями зміни температури суміші при її самонагрівання. Тому за температуру самозаймання приймають ту найменшу температуру стінки судини або довкілля, При якій в даних умовах відбувається самозаймання речовини, тобто Т 0. Це не тягне за собою занадто великої помилки.
Час з моменту встановлення в пальному речовині температури Т 0 до досягнення температури Т з називається періодом індукції або часом запізнювання самозапалювання. Період індукції для одного і того ж речовини неоднаковий і сильно залежить від складу горючої суміші, температури і тиску. Чим нижче температура нагріву пального речовини при самозаймання, тим більше період індукції. за
цього часто за температуру самозаймання приймають ту температуру навколишнього середовища або стінок посудини, при якій період індукції найбільший.
Нижче показано зміна періоду індукції сумішей метану з повітрям в залежності від їх складу і температури судини:
|
Період індукції, з |
|||
|
при 775 0 С ................................................... |
|||
|
при 825 0 С ................................................... |
|||
|
при 875 0 С ................................................... |
|||
При визначенні температури самозаймання неможливо виміряти період індукції, тому за період індукції приймають час з моменту нагріву речовини до появи полум'я. період індукції має практичне значення при дії на пальне речовина малопотужних джерел займання (іскри). При попаданні іскри в горючу суміш парів або газів з повітрям деякий обсяг суміші нагрівається і в той же час охолоджується іскра. Займання суміші в цьому випадку залежить від співвідношення періоду індукції суміші і часу охолодження іскри. Якщо період індукції більше часу охолодження іскри до температури, яка нижча за температуру самозаймання, то займання суміші не відбувається. Якщо ж період індукції менше часу охолодження іскри, суміш запалюється. Таким чином, іскра невеликої потужності може запалити суміш з малим періодом індукції і може не запалити суміш з великим періодом індукції.
період індукції твердих речовин відрізняється від періоду індукції газових і пилових сумішей. Якщо період індукції для газових сумішей складає десятки і сотні секунд, то період індукції для твердих горючих речовин може складати години, дні і місяці. При температурі самозаймання речовини горіння ще не виникає. Воно виникає і розвивається при температурі горіння (полум'я), що значно перевищує температуру самозаймання. Наприклад, температура самозаймання бензину 260 0 С, а температура його полум'я 1200 - 1300 0 С. Стрибок у підйомі температури з 260 до 1200 0 С - результат самонагревания суміші парів бензину з повітрям.
Температура самозаймання горючої речовини не є постійною величиною. Згідно теплової теорії самозаймання, ця температура залежить від швидкості тепловиділення і швидкості тепловідводу, які, в свою чергу, залежать від обсягу горючої речовини, його концентрації, тиску та інших факторів.
У дослідах з визначення температури самозаймання встановлено, що вона змінюється не тільки зі зміною обсягу горючої речовини, а й від форми посудини (тари), в якому речовина знаходиться. Пояснюється це тим, що зі зміною форми або розміру судини змінюється питома поверхня тепловідведення S/ V. В однакових за формою судинах вона тим менше, чим більше обсяг судини. Отже, зі збільшенням обсягу судини швидкість тепловідведення зменшується і відповідно до цього температура самозаймання повинна знижуватися. Наведені нижче температури самозаймання парів рідин в посудинах різного об'єму підтверджують це припущення:
|
Обсяг судини, л .................. .. |
||||||||
|
температура самовоспламе- |
||||||||
|
ацетону ........................... |
||||||||
|
бензолу ........................... |
||||||||
|
бензину ........................... |
||||||||
|
діетилового ефіру ............ .. |
||||||||
|
гасу ......................... |
||||||||
|
метилового спирту ............ .. |
||||||||
|
сірковуглецю .................. .. |
||||||||
|
толуолу ........................... |
||||||||
температура самозаймання при збільшенні обсягу знижується до тих пір, поки об'єм не досягне деякого значення (форма посудини не змінюється); при подальшому збільшенні обсягу температура самозаймання залишається постійною.
Так, експеримент показує, що при обсязі понад 12 л температура самозаймання горючої суміші змінюється незначно. Пояснюється це тим, що у великих обсягах горюча суміш самозаймається не в усьому обсязі одночасно, а в частині його, в якій створилися найбільш оптимальні умови. Тому в малому обсязі горючої речовини зміна тепловідведення через зовнішні поверхні впливає на зміну температури самозаймання, а в великому обсязі - немає.
Підвищення температури самозаймання горючої речовини при зменшенні обсягу також не безкінечне. При дуже малому обсязі питома поверхня тепловідведення стає такою великою, що швидкість виділення тепла за рахунок окислення горючої суміші навіть при дуже високих температурах не може перевищити швидкість тепловідведення, і самозаймання не відбувається. На цьому принципі сконструйовані і працюють багато пристроїв, призначені для запобігання поширенню горіння по газовим сумішам (вогнеперепинювачів).
Найпростішим Вогнеперепинювачів є захисна сітка, що поміщається в горючу газову суміш, яка розбивається сіткою на дрібні обсяги. При цьому самозаймання статися не може. Захисну сітку застосовують в шахтарських лампах, а також в трубопроводах невеликого діаметру, по яких транспортується суміш повітря з парами нафтопродуктів. Захисну сітку можна застосовувати для сумішей повітря з воднем, ацетиленом, парами сірковуглецю, спиртами, ефірами та іншими речовинами, що мають або низьку температуру самозаймання, або високу теплоту згоряння. В таких умовах палаюча суміш при проходженні через палаючу сітки не охолоджується нижче температури самозаймання і продовжує горіти за сіткою.
Велику питому поверхню тепловідведення можна отримати не тільки в результаті зменшення обсягу судини, але і наданням йому відповідної форми. На рис. 2.4 зображені судини різної форми, Які вміщують однакові кількості горючої суміші.
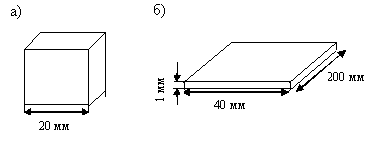
Мал. 2.4. Судини однаковою ємності з різною швидкістю відводу тепла
У першому посудині (куб) (рис. 2.4, а) При нагріванні відбувається самозаймання суміші, в другому, що представляє собою тонку щілину (рис. 2.4, б), Суміш не займається. Пояснюється це тим, що другий посудину має в кілька разів більшу поверхню тепловідведення, ніж перший.
\u003e Елементи теорії самозаймання. Температура самонагрівання. Відмінність самозаймання від самозаймання та запалювання
правильна організація протипожежних заходів і гасіння пожеж неможлива без розуміння сутності хімічних і фізичних процесів, які відбуваються при горінні. Знання цих процесів дає можливість успішно боротися з вогнем.
горіння- це хімічна реакція окислення, що супроводжується виділенням великої кількості тепла і зазвичай світінням. Окислювачем в процесі горіння може бути кисень, а також хлор, бром та інші речовини.
У більшості випадків під час пожежі окислення горючих речовин відбувається киснем повітря. Горіння можливо при наявності речовини, здатного горіти, кисню (повітря) і джерела запалювання. При цьому необхідно, щоб горюча речовина і кисень знаходилися в певних кількісних співвідношеннях, а джерело запалювання мав необхідний запас теплової енергії.
Відомо, що в повітрі міститься близько 21% кисню. Горіння більшості речовин стає неможливим, коли вміст кисню в повітрі знижується до 14-18%, і тільки деякі горючі речовини (водень, етилен, ацетилен і ін.) Можуть горіти при вмісті кисню в повітрі до 10% і менше. При подальшому зменшенні вмісту кисню горіння більшості речовин припиняється.
Горючою речовиною і кисень є реагують речовинами і складають горючу систему, а джерело запалювання викликає в ній реакцію горіння. Джерелом запалювання може бути палаюче пли розжарене тіло, а також електричний розряд, що володіє запасом енергії, достатнім для виникнення горіння та ін. Самозаймання запалювання огнетушащий
Горючі системи підрозділяються на однорідні і неоднорідні. Однорідними є системи, в яких горюча речовина і повітря рівномірно перемішані один з одним (суміші горючих газів, парів з повітрям). Горіння таких систем називають горінням кінетичним. Швидкість його визначається швидкістю хімічної реакції, Значною при високій температурі. При певних умовах таке горіння може носити характер вибуху або детонації. Неоднорідними є системи, в яких горюча речовина і повітря не перемішані один з одним і мають поверхні розділу (тверді горючі матеріали і нераспиленние рідини). У процесі горіння неоднорідних горючих систем кисень повітря проникає (дифундує) крізь продукти горіння до пального речовини і вступає з ним у реакцію. Таке горіння називають дифузійним горінням,так як його швидкість визначається головним чином порівняно повільно протікає процесом-дифузією.
Для загоряння тепло джерела запалювання повинно бути достатнім для перетворення горючих речовин в пари і гази і для нагріву їх до температури самозаймання. За співвідношенням пального і окислювача розрізняють процеси горіння бідних і багатих горючих сумішей. Бідні суміші містять в надлишку окислювач і мають недолік пального компонента. Багаті суміші, навпаки, мають в надлишку горючий компонент і в нестачі окислювач.
Виникнення горіння пов'язано з обов'язковим самоускорением реакції в системі. Процес самоускорения реакції окислення з переходом її в горіння називається самозаймання. Самоускорением хімічної реакції при горінні підрозділяється на три основних види: тепловою, ланцюговою і комбінований - цепочечную-теплової. За теплової теорії процес самозаймання пояснюється активізацією процесу окислення зі зростанням швидкості хімічної реакції. За ланцюгової теорії процес самозаймання пояснюється розгалуженням ланцюгів хімічної реакції. Практично процеси горіння здійснюються переважно з комбінованого цепочечную-тепловому механізму.
Від згоряння розрізняють повне і неповне. При повному згорянні утворюються продукти, які не здатні більше горіти: вуглекислий газ, сірчистий газ, пари води. Неповне згоряння відбувається, коли до зони горіння утруднений доступ кисню повітря, в результаті чого утворюються продукти неповного згоряння: окис вуглецю, спирти, альдегіди та ін.
Орієнтовно кількість повітря (м3), необхідне для згоряння 1 кг речовини (або 1 м3 газу),
Теплота згоряння деяких речовин: бензину-47 000 кДж / кг; деревини повітряно-сухої -14 600 кДж / кг; ацетилену - 54400 кДж / м3; метану - 39400 кДж / м3; окису вуглецю - 12600 кДж / м3.
За теплотою згоряння горючої речовини можна визначити, яка кількість тепла виділяється при його згорянні, температуру горіння, тиск при вибуху в замкнутому просторі і інші дані.
Температура горіння речовини визначається як теоретична, так і справжня. Теоретичною називається температура горіння, до якої нагріваються продукти згоряння, в припущенні, що все тепло, що виділяється при горінні, йде на їх нагрівання.
Дійсна температура горіння на 30-50% нижче теоретичної, так як значна частина тепла, що виділяється при горінні, розсіюється в навколишнє середовище.
Висока температура горіння сприяє поширенню пожежі, при ній велика кількість тепла випромінюється в навколишнє середовище, і йде інтенсивна підготовка горючих речовин до горіння. Гасіння пожежі при високій температурі горіння може.
При розгляді процесів горіння слід розрізняти такі його види: спалах, спалах, займання, самозаймання, самозаймання, вибух.
спалах- це швидке згоряння горючої суміші, що не супроводжується утворенням стислих газів.
займання- виникнення горіння під впливом джерела запалювання.
займання- загоряння, що супроводжується появою полум'я.
Возгораемость- здатність загорятися (запалюватися) під впливом джерела запалювання.
самозаймання- це явище різкого збільшення швидкості екзотермічних реакцій, що приводить до виникнення горіння речовин (матеріалу, суміші) при відсутності джерела запалювання.
самозаймання- це самозаймання, що супроводжується появою полум'я.
вибухомназивається надзвичайно швидке хімічне (вибухове) перетворення речовини, що супроводжується виділенням енергії і утворенням стислих газів, здатних виробляти механічну роботу.
Необхідно розуміти різницю між процесами загоряння (запалення) і самозаймання (самозаймання). Для того щоб виникло займання, необхідно внести в горючу систему теплової імпульс, який має температуру, що перевищує температуру самозаймання речовини. Виникнення ж горіння при температурах нижче температури самозаймання відносять до процесу самозаймання (самозаймання).
Горіння при цьому виникає без внесення джерела запалювання - за рахунок теплового або мікробіологічного самозаймання.
теплове самозайманняречовини виникає в результаті самонагрівання під впливом прихованого або зовнішнього джерела нагрівання. Самозаймання можливо тільки в тому випадку, якщо кількість тепла, що виділяється в процесі самоокисления, буде перевищувати віддачу тепла в навколишнє середовище.
мікробіологічне самозаймання виникає в результаті самонагрівання під впливом життєдіяльності мікроорганізмів в масі речовини (матеріалу, суміші). Температура самозаймання є важливою характеристикою горючої речовини.
температура самозаймання - це сама низька температура речовини, при якій відбувається різке збільшення швидкості екзотермічних реакцій, який закінчується виникненням полум'яного горіння.
Температури самозаймання деяких рідин, газів і твердих речовин, що мають застосування в машинобудівній промисловості, наведені в табл. 1.
Таблиця 1 Температури самозаймання деяких рідин
Крім температури самозаймання, горючі речовини характеризуються періодом індукції або часом запізнювання самозапалювання. Періодом індукції називають проміжок часу, протягом якого відбувається саморазогреванія до займання. Період індукції для одного і того ж горючої речовини неоднаковий і залежить від складу суміші, початкових температури і тиску.
Період індукції має практичне значення при дії на пальне речовина малопотужних джерел займання (іскри). Іскра, потрапляючи в горючу суміш парів або газів з повітрям, нагріває деякий обсяг суміші, і в той же час відбувається охолодження іскри. Займання суміші залежить від співвідношення періоду індукції суміші і часу охолодження іскри. При цьому, якщо період індукції більше часу охолодження іскри, то займання суміші не відбудеться.
Період індукції прийнятий в основу класифікації газових сумішей за ступенем їх небезпеки щодо займання. Період індукції пилових сумішей залежить від розміру пилинок, кількості летючих речовин, вологості та інших факторів.
Деякі речовини можуть самозайматися, перебуваючи при звичайній температурі. Це в основному тверді пористі речовини здебільшого органічного походження (тирса, торф, викопне вугілля та ін.). Схильні до самозаймання та масла, розподілені тонким шаром по великій поверхні. Цим обумовлена \u200b\u200bможливість самозаймання промасленим дрантя. Причиною самозаймання промаслених волокнистих матеріалів є розподіл жирових речовин тонким шаром на їх поверхні і поглинання кисню з повітря. Окислення масла киснем повітря супроводжується виділенням тепла. У разі, коли кількість що утворюється тепла перевищує тепловтрати в навколишнє середовище, можливе виникнення пожежі.
Пожежна небезпека речовин, схильних до самозаймання, дуже велика, оскільки вони можуть загорятися без всякого підведення тепла при температурі навколишнього середовища нижче температури самозаймання речовин, а період індукції самовозгорающихся речовин може становити кілька годин, днів і навіть місяців. Розпочатий процес прискорення окислення (розігрівання речовини) можна зупинити лише при виявленні небезпечного наростання температури, що вказує на велике значення пожежно-профілактичних заходів.
На машинобудівних підприємствах застосовуються багато речовин, здатні до самозаймання. Самозайматися при взаємодії з повітрям можуть сульфіди заліза, сажа, алюмінієва і цинкова пудра і ін. Самозайматися при взаємодії з водою можуть лужні метали, Карбіди металів і ін. Карбід кальцію (СаС2), реагуючи з водою, утворює ацетилен (С2Н2).
Горінням називають екзотермічну реакцію, яка відбувається в умовах її прогресивного самоускорения. Горіння може відбуватися як в результаті хімічної реакції з'єднання, так і розпаду речовин не тільки при поєднанні з киснем повітря, але і з речовинами, які містять його в собі (наприклад, вапно). Горіння багатьох речовин може відбуватися в середовищі хлору, парів брому, сірки.
Горіння поділяють на кілька видів: спалахи, займання, запалення, самозаймання, самозаймання.
Температура спалаху - це найменша температура концентрованої речовини, при якій в умовах спеціальних випробувань над її поверхнею утворюється пара, здатна спалахувати в повітрі від джерела запалювання; стійке горіння при цьому не виникає.
Займання - це швидке згоряння горючої речовини, яка не супроводжується утворенням стисненого газу.
Нижче температури займання рідина не представляє пожежної небезпеки в разі короткочасної дії полум'я, іскри або розпеченого тіла. Якщо рідина нагріта до температури спалаху і вище, то навіть короткочасна дія на ЇЇ пару полум'я або іскри неминуче викличе її займання, і за певних умов може виникнути пожежа. Беручи це до уваги, температуру спалаху взято за основу класифікації рідин за ступенем пожежної безпеки. Рідини, здатні горіти, діляться на легкозаймисті (ЛЗР) і горючі (ГР) *.
Вогненебезпечні речовини, які найчастіше зустрічаються в авіації, мають такі температури спалаху (в градусах Цельсія):
* До легкозаймистих рідин відносяться горючі рідини з температурою спалаху, що не перевищує 61 ° С при визначенні в закритому тиглі, або 66 ° С - при визначенні у відкритому тиглі. Рідини з температурою спалаху вище зазначеної відносяться до горючих.
Залежно від температури спалаху необхідно вибирати безпечні методи транспортування, зберігання і застосування рідини для різних цілей. При температурі спалаху стійке горіння не виникає, а згорає тільки утворена над рідиною суміш парів з повітрям. Якщо температура рідини трохи вище температури спалаху, швидкість випаровування її з відкритої поверхні підвищується, і в момент спалаху суміші рідина здатна виділяти безперервно пару в достатній кількості для стійкого горіння. Таку температуру називають температурою займання. Це - найменша температура речовини, при якій в умовах спеціальних випробувань речовина виділяє горючу пару і гази з такою швидкістю, що при впливі на них джерела енергії відбувається їх запалювання.
Запалення - це загоряння, що супроводжується появою полум'я.
У легкозаймистих рідин температура займання вище температури спалаху на 1-5 ° С, до того ж, чим нижче температура спалаху рідини, тим менше ця різниця. Так, в бензолу, ацетону, що мають температуру спалаху нижче нуля, ця різниця дорівнює 1 ° С, в горючих рідин - ця різниця доходить до 30 ° С і вище.
самозаймання - це різке збільшення швидкості екзотермічних об'ємних реакцій, що призводить до різкого підвищення температури і до виникнення горіння речовин при відсутності джерела запалювання.
Теплова теорія самозаймання була вперше розроблена С.М. Семеновим і надалі докладніше розвинена Д. А. Франк-Каменецьким і А. Н. Тодес.
Основні положення цієї теорії можна розглянути на прикладі самозаймання суміші горючих парів або газів з повітрям. При низькій температурі Т0 (наприклад, плюс 20 ° С) реакція між гасом і киснем повітря в суміші практично не протікає, так як відсутні активні молекули кисню. Для того щоб вони з'явилися і почалася реакція окислення, суміш треба нагріти до більш високої температури Т1. Для цього поміщають посуд з сумішшю в середу, має температуру Т1 (рис 15,1, а). Через деякий час посуд і суміш в ньому нагріються до температури Т1 і в суміші виникне процес окислення з виділенням тепла. Виділене тепло q1 передається горючої суміші, нагріється до температури Т1. Однак, як тільки температура суміші перевищить температуру стінок посуду і зовнішнього середовища, почнеться тепловідвідвід суміші до стінок посуду і далі - до зовнішньому середовищі. Кількість відведеного тепла позначимо через q2.

Мал. 15.1. Схема, яка пояснює процес самозаймання спалимої суміші:
а- нагрівання суміші за рахунок підведеної до неї теплової енергії; б - теплова рівновага; в - самонагревания суміші і висновок від неї тепла в навколишнє середовище
Подальше нагрівання суміші буде залежати від співвідношення швидкостей тепловиділення і тепловідведення. Якщо q1\u003e q2 то суміш, окислюючись, буде нагріватися, а якщо q1 \u003d q2, то суміш буде окислюватися при будь постійної температури, При якій виникло це співвідношення. Припустимо, що швидкість виділення тепла за рахунок окислення суміші перевищує швидкість тепловідведення. Однак цього ще недостатньо, щоб суміш продовжувала нагріватися і подалі, так як з підвищенням температури горючої суміші швидкість виділення тепла і тепловідведення збільшується не однаково. І якщо зі збільшенням температури суміші швидкість тепловідведення буде рости швидше, ніж тепловиділення, то при деякій температурі суміші вони стануть рівними (91 \u003d 92) і в подальшому нагрів призупиниться. Це зазвичай відбувається при малій швидкості окислення горючої речовини або при великому теплоотводе.
Наприклад, сталеві стружки і тирса також окислюються, тому відбувається виділення тепла, але в зв'язку з малою швидкістю окислення це не завжди призводить до горіння. У плівці олійної фарби на пофарбованої поверхні відбувається процес окислення, але через дуже велику поверхню посилення тепловідведення нагріву її не спостерігається.
Отже, суміш, нагріта до температури Т2 за рахунок реакції, окислення, буде поступово остигати до температури Т1 (як тільки концентрація реагуючих речовин в суміші почне зменшуватися). З цього випливає, що процес окислення горючої суміші, нагрітої до температури Т, не може перейти в горіння через малу швидкість реакції.
Збільшимо швидкість окислення суміші, нагріваючи її до температури Т3. Швидкість відводу тепла при цьому залишиться незмінною, тому що поверхня судини не змінилася. Це може привести до того, що при температурі горючої суміші Ту швидкість виділення тепла постійно буде перевищувати швидкість тепловідведення і суміш отримає можливість самонагріватіся до високої температури. Коли температура суміші досягне температури горіння, з'явиться полум'я і виникне горіння. Отже, обов'язковою умовою протікання процесу самозаймання є перевищення швидкості виділення тепла в суміші над швидкістю відводу тепла.
Отже, теплове самозаймання називають процес виникнення горіння, який відбувається в результаті самонагрівання речовин, нагрітих до стану, в процесі якого швидкість виділення тепла за рахунок реакції окислення перевищує швидкість тепловідведення. Температури самозаймання зазвичай беруть температуру стінок посудини, при якій в даних умовах відбувається самозаймання.
Процес теплового самозаймання можна розглядати в залежності від часу (рис. 15.2).
Помістимо горюча речовина в повітря, нагріте нижче температури окислення. Температура речовини в цьому випадку буде повільно підвищуватися (крива 1) і через деякий час буде дорівнювати температурі повітря Т0. Тому що Т0 нижче температури окислення, горюча речовина буде вести себе так, як негорюча. Якщо повітря нагріти до температури Т1, яка буде вища за температуру окислення цієї речовини, відбудеться розігрів горючої речовини (крива 2) до температури, більшої за Т1 але потім температура почне знижуватися.

Мал. 15.2. Графік зміни температури горючих речовин при нагріванні
Розігріємо повітря до температури Тs\u003e Т1. Природно, що швидкість реакції окислення в цьому випадку буде набагато вище, ніж в попередньому, і температура речовини підніметься вище температури повітря Ts, досягаючи значення Tв, після чого відбудеться швидке підвищення температури речовини до температури горіння. Розглянуто процес самозаймання на прикладі газової суміші характерний не тільки для горючих парів і газів. Він поширюється на тверді речовини.
Температура самозаймання не є постійною величиною для однієї і тієї ж горючої речовини. Вона залежить від швидкостей тепловиділення і тепловідведення, які в свою чергу залежать від обсягу і форми горючої речовини, склад її в одиниці об'єму, тиску та інших факторів. Межі температури самозаймання (в градусах Цельсія) деяких легкозаймистих і горючих речовин наступні:

Крім теплового (з зовнішнім нагріванням), самозаймання ще буває мікробіологічним і хімічним.
Мікробіологічне самозаймання виникає внаслідок самонагрівання в масі речовини під дією мікроорганізмів. Це явище спостерігається при зберіганні зерна, сіна, торфу, вугілля і т.
Хімічне самозаймання відбувається в результаті хімічної взаємодії речовин при впливі на них повітря і води (рослинна олія та тваринні жири, масла) при наявності великої поверхні окислення і малої тепловіддачі в навколишнє середовище.
Температура самозаймання в деяких горючих речовин може перевищувати 500 ° С, а в інших - бути нижче 16 ° С. Всі горючі речовини з температурою самозаймання умовно можна розділити на дві групи: речовини, які мають температуру самозаймання вище звичайної (16-25 ° С) і нижче. Речовини першої групи здатні самозайматися тільки при нагріванні їх до тієї чи іншої температури, речовини другої групи - самовозгораются без додаткового нагріву, оскільки навколишнє середовище вже нагріло їх до температури займання. Горючі речовини являють собою підвищену пожежну небезпеку, оскільки не виключена можливість їх запалювання при певних умовах. Наприклад, алюміній у вигляді пудри в результаті окислення здатний на самонагревания до виникнення горіння. Самонагрівання може початися при звичайній температурі навколишнього середовища і навіть нижче, а завершитися горінням. якщо тонку тканину, Просочену оліфою, скласти щільно, то тепло, яке утворюється при окисленні, не встигне розсіятися в повітрі і запалить тканину. Однак, якщо ту ж тканину розкласти, а не звертаючи, то самозаймання не відбудеться, оскільки тепло, яке виділяється при швидко протікає процесу окислення, буде розсіюватися в навколишньому середовищі зі швидкістю, що перевищує швидкість його утворення.
Отже, дуже важливо знати речовини, які належать до другої групи, оскільки це дозволяє поставити до умов їх зберігання і транспортування особливі вимоги, Які унеможливлюють виникнення пожежі.
Наприклад, як відомо, існують мінеральні, рослинні і тваринні масла. мінеральні масла окислюються на повітрі тільки при високій температурі, а тому не самовозгораются. Відомі випадки самозаймання ганчірки, змоченою мінеральними авіаційними маслами, які виникали в результаті попадання в нього домішок рослинних масел. Жири та олії, що містять органічні сполуки, здатні до самозаймання.
Про здатність до самозаймання можна судити по йодного числа - кількістю грамів йоду, яка вступає в з'єднання з 100 г масла. Чим більше в маслі з'єднань, тим воно більше приєднує йоду і, отже, має велику здатність до самозаймання.
Оліфа з доданими для прискорення висихання сиккативами, нанесена на волокнисті матеріали, здатна до самозаймання. напівнатуральні і штучні оліфи малоспроможні або можуть самозайматися. Масла, жири або оліфи, які знаходяться в будь-який закритій тарі, самозайматися не можуть, оскільки поверхня дотику їх з повітрям дуже мала. Здатність олій і жирів до самозаймання значно зростає, коли поверхня окислення значно більше поверхні тепловіддачі. Такі умови створюються, коли промаслені матеріали складені в купи, штабелі, пакети і прилеглих близько один до одного. Самозаймання масел і жирів залежить від щільності упаковки промасленим матеріалу. Здатність його до самозаймання збільшується в разі ущільнення до певної межі, після якого починає зменшуватися.
Важливу роль в процесі самозаймання відіграє і температура навколишнього середовища. Чим вище температура повітря, тим менше обсяг промасленим матеріалу здатного до самозаймання, при цьому і масел потрібно менше. Імовірність виникнення пожежі в цьому випадку зростає в кілька разів.
Найменша температура, при: який спостерігається самозаймання масел і жирів, дорівнює 10-15 ° С. Бавовняні відходи, просочені рослинними оліями (Обтиральні кінці тканини), можуть самозайматися в залежності від умов в різні терміни (Від декількох годин до декількох діб).
Період індукції (період запізнювання самозапалювання) речовин, які здатні самозайматися, в газів і рідин, окислюються в газоподібному середовищі, дуже короткий. Майже такий же період і в твердих речовин, які знаходяться в стані аерозолів.
Період індукції твердих речовин у вигляді грудок різного розміру може бути тривалим, оскільки поверхня окислення в даному випадку мала. Невелика також і швидкість дифузії повітря на поверхню окислення.
Самозаймання називається самозаймання, що супроводжується появою полум'я. Горіння може супроводжуватися пожежею і вибухом.
За горючості речовини і матеріали поділяються на три групи: - вогнетривкими є матеріали і конструкції, які під дією вогню або високої температури не займаються, не тліють і не обвуглюються (наприклад, окислювачі або речовини, що виділяють горючі продукти при взаємодії з водою, киснем повітря або один з другом);
Важкогорючих є матеріали і конструкції, які під дією вогню або високої температури займаються, тліють або обвуглюються і продовжують горіти і обвуглюватися при наявності джерела запалювання, а після його видалення ці процеси припиняються.
До них відносяться штучні матеріали, Які, крім негорючих мінеральних речовин, Мають більше 80% по масі органічних наповнювачів; конструкції, виготовлені з важкогорючих матеріалів, а також з горючих, захищених від вогню і високих температур вогнетривкими матеріалами (дерево, вкрите азбестом і покрівельним залізом)
Спалимими вважають такі матеріали і конструкції, які під дією вогню або високої температури горять, тліють або обвуглюються і горять після видалення джерела воспламенителя. До них відносять всі органічні матеріали, не захищені від вогню або високих температур.
Більшість горючих речовин незалежно від їх початкового агрегатного стану (тверді, рідкі, газоподібні) при нагріванні переходять в газоподібні продукти і утворюють з повітрям горючі суміші. Підготовленість до займання визначається складом (концентрації) в них парів, пилу або газоподібних продуктів. Існують мінімальні і максимальні концентрації горючих речовин в повітрі, нижче і вище яких загоряння неможливо.
Ці концентрації відповідно називають нижньої і верхньої концентраційними межами займистості.
Спаленні гази і тверді подрібнені речовини (пил) можуть утворювати горючі суміші при будь-якій температурі. Тверді речовини, а також рідини утворюють горючі суміші тільки при певних температурах. Якщо горючих суміш підготовлена \u200b\u200bз дотриманням вищевказаних умов, то можна вважати, що вона підготовлена \u200b\u200bдо спалаху, яке може виникнути в разі появи джерела запалювання.
Температурними межами поширення полум'я (запалення) називають такі температури речовини, при яких його насичиний пар створює в окислювальному середовищі концентрації, рівні відповідно нижній (нижня температурна межа) і верхньої (верхня температурна межа) концентраційним межам поширення полум'я.
Значення температурних меж поширення полум'я застосовують: при розробці заходів щодо забезпечення пожежо- та вибухобезпеки об'єкта; для розрахунку пожежо і вибухонебезпечних температурних режимів роботи технологічного обладнання; оцінки аварійних ситуацій, Пов'язаних з розливом горючих рідин; розрахунку концентраційних меж поширення полум'я. Значення температурних меж необхідно включати в стандарти або в технічні умови на горючі речовини. Можливість виникнення горіння в основному характеризується температурами спалаху, запалювання, самозаймання та самозаймання.
самозаймання, Виникнення в результаті самонагрівання горючих твердих матеріалів, викликаного самоускорением в них екзотерміч. реакцій. Самозаймання відбувається через те, що тепловиділення в ході реакцій більше тепловідведення в навколишнє середовище.
Початок самозаймання характеризується температурою самонагревания ( T сн), що представляє собою мінімальну в умовах досвіду температуру, при якій виявляється тепловиділення.
При досягненні в процесі самонагрівання певної температури, Званої температурою самозаймання ( T звезення), виникає горіння матеріалу, що виявляється або тлінням, або полум'яним горінням. В останньому випадку T звезення адекватна температурі ( T св), під яким в пожежному справі розуміють виникнення і при нагріванні до певної критичної температури. (Див. В пожежному справі) .
В принципі самозаймання та самозаймання з фізичної сутності подібні і розрізняються лише видом горіння, самозаймання виникає тільки у вигляді полум'яного горіння.
У разі самонагрівання (предвзривной розігрів) розвивається в межах всього декількох градусів і тому не враховується при оцінці пожежовибухонебезпеки і рідин. При самозаймання область самонагревания може досягати декількох сотень градусів (наприклад, для торфу від 70 до 225 ° С). Внаслідок цього явище самонагрівання завжди враховується при визначенні схильності твердих речовин до самозаймання
Самозаймання вивчають шляхом термостатування досліджуваного матеріалу при заданій температурі і встановлення залежності між температурою, при якій виникає горіння, розмірами зразка та часом його нагрівання в термостаті.
Процеси, що відбуваються при самозаймання зразків пального матеріалу, зображені на малюнку. При температурах до T сн (напр., T 1) матеріал нагрівається без змін (тепловиділення відсутня). при досягненні T сн в матеріалі відбуваються екзотермічні реакції. Останні в залежності від умов накопичення теплоти (маса матеріалу, щільність упаковки його атомів і молекул, тривалість процесу і т. Д.) Можуть після періоду невеликого самонагревания після вичерпання здатних саморазогреваться компонентів матеріалу завершитися охолодженням зразка до початкової температури термостата (крива 1) або продовжувати самонагрівається аж до T звезення (крива 2). область між Т сн і T звезення потенційно пожежонебезпечна, нижче T сн -
безпечна.
зміна температури Тв часі т в термостатірованних зразках горючого матеріалу.
Можливість самозаймання матеріалу, що знаходиться в потенційно пожежонебезпечної області, встановлюють за допомогою рівнянь:
де T окр-температура навколишнього середовища, ° С; l-визначати розмір (зазвичай товщина) матеріалу; т-час, протягом якого може статися самозаймання; A 1 , n 1 і А 2 , n 2-коефіцієнт, що визначаються для кожного матеріалу по досвідченим даним (див. Табл.).
За рівняння (1) при заданому l знаходять T окр, при якій може виникнути самозаймання даного матеріалу, За рівнянням (2) -за відомої Т окр величину т. При температурі, нижче обчисленої T окр, або при т, меншому, ніж час, розраховане за рівнянням (2), самозаймання не відбудеться.
Залежно від природи первинного процесу, що викликав самонагрівання матеріалу, і значень T сн розрізняють хімічну, мікробіологічне та теплове самозаймання

До хімічного самозаймання відносяться екзотермічне взаємодія речовин (наприклад, при попаданні концентрованої HNО 3 на папір, деревна тирса та ін.). Найбільш типовий і поширений приклад такого процесу - самозаймання промасленим дрантя або інших волокнистих матеріалів з розвиненою поверхнею. Особливо небезпечні масла, що містять сполуки з ненасиченими хімічними зв'язками і характеризуються високим йодним числом (бавовняне, соняшникова, джутове і т.д.).
До явищ хімічного самозаймання відноситься також загоряння ряду речовин (наприклад, мелкораздробленного Аl і Fe, гідриди Si, В і деяких металів, металоорганічних сполук - алюмінійорганіческіх і ін.) При контакті їх з повітрям під час відсутності нагріву. Здатність речовин до самозаймання в таких умовах називають пірофорність. Особливість пірофорних речовин полягає в тому, що їх T звезення (або T св) нижче кімнатної температури: - 200 ° С для SiH 4, - 80 ° С для А1 (С 2 Н 5) 3. Для попередження хімічного самозаймання порядок спільного зберігання горючих речовин і матеріалів суворо регламентований.
Схильністю до мікробіологічного самозаймання мають горючі матеріали, особливо зволожені, що служать живильним середовищем для мікроорганізмів, життєдіяльність яких пов'язана з виділенням теплоти (торф, тирса та ін.). З цієї причини велика кількість пожеж і вибухів відбувається при зберіганні сільськогосподарських продуктів (наприклад, силос, зволожене сіно) в елеваторах. Для мікробіологічного і хімічного самозаймання характерно те, що T сн не перевищує звичайних значень Т окр і може бути негативною. Матеріали, що мають T сн вище кімнатної температури, здатні до теплового самозаймання
Взагалі схильністю до всіх видів самозаймання мають багато тверді матеріали з розвиненою поверхнею (наприклад, волокнисті), а також деякі рідкі і плавляться речовини, що містять у своєму складі ненасичені сполуки, нанесені на розвинену (в тому числі негорючую) поверхню. Розрахунок критичних умов для хімічного, мікробіологічного та теплового самозаймання здійснюється за рівнянням (1) і (2). Методи експериментального визначення Т
Правильна організація протипожежних заходів і гасіння пожеж неможлива без розуміння сутності хімічних і фізичних процесів, які відбуваються при горінні. Знання цих процесів дає можливість успішно боротися з вогнем.
Горіння - це хімічна реакція окислення, що супроводжується виділенням великої кількості тепла і зазвичай світінням. Окислювачем в процесі горіння може бути кисень, а також хлор, бром та інші речовини.
У більшості випадків під час пожежі окислення горючих речовин відбувається киснем повітря. Цей вид окислювача і прийнятий в подальшому викладі. Горіння можливо при наявності речовини, здатного горіти, кисню (повітря) і джерела запалювання. При цьому необхідно, щоб горюча речовина і кисень знаходилися в певних кількісних співвідношеннях, а джерело запалювання мав необхідний запас теплової енергії.
Відомо, що в повітрі міститься близько 21% кисню. Горіння більшості речовин стає неможливим, коли вміст кисню в повітрі знижується до 14-18%, і тільки деякі горючі речовини (водень, етилен, ацетилен і ін.) Можуть горіти при вмісті кисню в повітрі до 10% і менше. При подальшому зменшенні вмісту кисню горіння більшості речовин припиняється.
Горючою речовиною і кисень є реагують речовинами і складають горючу систему, а джерело запалювання викликає в ній реакцію горіння. Джерелом запалювання може бути палаюче пли розжарене тіло, а також електричний розряд, що володіє запасом енергії, достатнім для виникнення горіння та ін.
Горючі системи підрозділяються на однорідні і неоднорідні. Однорідними є системи, в яких горюча речовина і повітря рівномірно перемішані один з одним (суміші горючих газів, парів з повітрям). Горіння таких систем називають горінням кінетичним. Швидкість його визначається швидкістю хімічної реакції, значною при високій температурі. При певних умовах таке горіння може носити характер вибуху або детонації. Неоднорідними є системи, в яких горюча речовина і повітря не перемішані один з одним і мають поверхні розділу (тверді горючі матеріали і нераспиленние рідини). У процесі горіння неоднорідних горючих систем кисень повітря проникає (дифундує) крізь продукти горіння до пального речовини і вступає з ним у реакцію. Таке горіння називають дифузійним горінням, так як його швидкість визначається головним чином порівняно повільно протікає процесом-дифузією.
Для загоряння тепло джерела запалювання повинно бути достатнім для перетворення горючих речовин в пари і гази і для нагріву їх до температури самозаймання. За співвідношенням пального і окислювача розрізняють процеси горіння бідних і багатих горючих сумішей. Бідні суміші містять в надлишку окислювач і мають недолік пального компонента. Багаті суміші, навпаки, мають в надлишку горючий компонент і в нестачі окислювач.
Виникнення горіння пов'язано з обов'язковим самоускорением реакції в системі. Процес самоускорения реакції окислення з переходом її в горіння називається самозаймання. Самоускорением хімічної реакції при горінні підрозділяється на три основних види: тепловою, ланцюговою і комбінований - цепочечную-теплової. За теплової теорії процес самозаймання пояснюється активізацією процесу окислення зі зростанням швидкості хімічної реакції. За ланцюгової теорії процес самозаймання пояснюється розгалуженням ланцюгів хімічної реакції. Практично процеси горіння здійснюються переважно з комбінованого цепочечную-тепловому механізму.
Від згоряння розрізняють повне і неповне. При повному згорянні утворюються продукти, які не здатні більше горіти: вуглекислий газ, сірчистий газ, пари води. Неповне згоряння відбувається, коли до зони горіння утруднений доступ кисню повітря, в результаті чого утворюються продукти неповного згоряння: окис вуглецю, спирти, альдегіди та ін.
Орієнтовно кількість повітря (м 3), необхідне для згоряння 1 кг речовини (або 1 м 3 газу),
де Q - теплота згоряння, кДж / кг, або кДж / м 3.
Теплота згоряння деяких речовин: бензину-47 000 кДж / кг; деревини повітряно-сухої -14 600 кДж / кг; ацетилену - 54400 кДж / м 3; метану - 39400 кДж / м 3; окису вуглецю - 12600 кДж / м 3.
За теплотою згоряння горючої речовини можна визначити, яка кількість тепла виділяється при його згорянні, температуру горіння, тиск при вибуху в замкнутому просторі і інші дані.
Температура горіння речовини визначається як теоретична, так і справжня. Теоретичною називається температура горіння, до якої нагріваються продукти згоряння, в припущенні, що все тепло, що виділяється при горінні, йде на їх нагрівання.
Теоретична температура горіння
де m - кількість продуктів горіння, що утворюються при згорянні 1 кг речовини; с - теплоємність продуктів горіння, кДж / (кг * К); θ - температура повітря, К; Q - теплота згоряння, кДж / кг.
Дійсна температура горіння на 30-50% нижче теоретичної, так як значна частина тепла, що виділяється при горінні, розсіюється в навколишнє середовище.
Висока температура горіння сприяє поширенню пожежі, при ній велику кількість тепла випромінюється в навколишнє середовище, і йде інтенсивна підготовка горючих речовин до горіння. Гасіння пожежі при високій температурі горіння може.
При розгляді процесів горіння слід розрізняти такі його види: спалах, спалах, займання, самозаймання, самозаймання, вибух.
Спалах - це швидке згоряння горючої суміші, що не супроводжується утворенням стислих газів.
Займання - виникнення горіння під впливом джерела запалювання.
Займання - загоряння, що супроводжується появою полум'я.
Возгораемость - здатність загорятися (запалюватися) під впливом джерела запалювання.
Самозаймання - це явище різкого збільшення швидкості екзотермічних реакцій, що приводить до виникнення горіння речовин (матеріалу, суміші) при відсутності джерела запалювання.
Самозаймання - це самозаймання, що супроводжується появою полум'я.
Вибухом називається надзвичайно швидке хімічне (вибухове) перетворення речовини, що супроводжується виділенням енергії і утворенням стислих газів, здатних виробляти механічну роботу.
Необхідно розуміти різницю між процесами загоряння (запалення) і самозаймання (самозаймання). Для того щоб виникло займання, необхідно внести в горючу систему теплової імпульс, який має температуру, що перевищує температуру самозаймання речовини. Виникнення ж горіння при температурах нижче температури самозаймання відносять до процесу самозаймання (самозаймання).
Горіння при цьому виникає без внесення джерела запалювання - за рахунок теплового або мікробіологічного самозаймання.
теплове самозайманняречовини виникає в результаті самонагрівання під впливом прихованого або зовнішнього джерела нагрівання. Самозаймання можливо тільки в тому випадку, якщо кількість тепла, що виділяється в процесі самоокисления, буде перевищувати віддачу тепла в навколишнє середовище.
мікробіологічне самозаймання виникає в результаті самонагрівання під впливом життєдіяльності мікроорганізмів в масі речовини (матеріалу, суміші). Температура самозаймання є важливою характеристикою горючої речовини.
Температура самозаймання - це найнижча температура речовини, при якій відбувається різке збільшення швидкості екзотермічних реакцій, який закінчується виникненням полум'яного горіння.
Температури самозаймання деяких рідин, газів і твердих речовин, що мають застосування в машинобудівній промисловості, наведені в табл. 28.
Таблиця 28 Температури самозаймання деяких рідин
| речовина | Температура самозаймання, ° С |
фосфор білий |
20 |
сірковуглець |
112 |
целулоїд |
140-180 |
сірководень |
246 |
масла нафтові |
250-400 |
| 250 | |
Бензин А-76 |
255 |
| 380-420 | |
Кам'яне вугілля |
400 |
ацетилен |
406 |
Етиловий спирт |
421 |
Деревне вугілля |
450 |
нітробензол |
482 |
| 530 | |
| 612 | |
| 625 | |
Окис вуглецю |
644 |
| 700 |
Крім температури самозаймання, горючі речовини характеризуються періодом індукції або часом запізнювання самозапалювання. Періодом індукції називають проміжок часу,
протягом якого відбувається саморазогреванія до займання. Період індукції для одного і того ж горючої речовини неоднаковий і залежить від складу суміші, початкових температури і тиску.
Період індукції має практичне значення при дії на пальне речовина малопотужних джерел займання (іскри). Іскра, потрапляючи в горючу суміш парів або газів з повітрям, нагріває деякий обсяг суміші, і в той же час відбувається охолодження іскри. Займання суміші залежить від співвідношення періоду індукції суміші і часу охолодження іскри. При цьому, якщо період індукції більше часу охолодження іскри, то займання суміші не відбудеться.
Період індукції прийнятий в основу класифікації газових сумішей за ступенем їх небезпеки щодо займання. Період індукції пилових сумішей залежить від розміру пилинок, кількості летючих речовин, вологості та інших факторів.
Деякі речовини можуть самозайматися, перебуваючи при звичайній температурі. Це в основному тверді пористі речовини здебільшого органічного походження (тирса, торф, викопне вугілля та ін.). Схильні до самозаймання та масла, розподілені тонким шаром по великій поверхні. Цим обумовлена \u200b\u200bможливість самозаймання промасленим дрантя. Причиною самозаймання промаслених волокнистих матеріалів є розподіл жирових речовин тонким шаром на їх поверхні і поглинання кисню з повітря. Окислення масла киснем повітря супроводжується виділенням тепла. У разі, коли кількість що утворюється тепла перевищує тепловтрати в навколишнє середовище, можливе виникнення пожежі.
Пожежна небезпека речовин, схильних до самозаймання, дуже велика, оскільки вони можуть загорятися без всякого підведення тепла при температурі навколишнього середовища нижче температури самозаймання речовин, а період індукції самовозгорающихся речовин може становити кілька годин, днів і навіть місяців. Розпочатий процес прискорення окислення (розігрівання речовини) можна зупинити лише при виявленні небезпечного наростання температури, що вказує на велике значення пожежно-профілактичних заходів.
На машинобудівних підприємствах застосовуються багато речовин, здатні до самозаймання. Самозайматися при взаємодії з повітрям можуть сульфіди заліза, сажа, алюмінієва і цинкова пудра і ін. Самозайматися при взаємодії з водою можуть лужні метали, карбіди металів і ін. Карбід кальцію (Сас 2), реагуючи з водою, утворює ацетилен (С 2 Н 2 ).